Бронхиальная астма классифицируется на виды, формы, фазы по нескольким признакам (причине, степени контролируемости, степени проявления бронхиальной обструкции). Но одной из наиболее важных классификаций, предопределяющих лечение заболевания, является классификация по степени тяжести течения. В соответствии с ней выделяют четыре формы бронхиальной астмы, наиболее опасной из которых является тяжелая персистирующая.
Степень тяжести течения бронхиальной астмы определяется по:
- Количеству приступов в неделю в ночное время;
- Количеству приступов в неделю в дневное время;
- Частоту и продолжительность применения препаратов бета2-агонистов короткого действия;
- Показатели пиковой скорости выдоха, ее суточные изменения;
1. Эпизодическую бронхиальную астму, или астму легкого интермиттирующего течения;
Эта форма заболевания характеризуется эпизодическими короткими обострениями (от нескольких часов до нескольких дней). Приступы удушья (одышки или кашля) днем случаются не чаще 1 раза в неделю, ночью – 2 раз в месяц. Пиковая скорость выдоха составляет 80% от должного показателя, за сутки она колеблется не более чем на 20%.
В период между обострениями бронхиальная астма легкой формы не проявляется никакими симптомами, легкие человека функционируют нормально.
К сожалению, выявить болезнь в этой форме получается не всегда. Во-первых, влияние ее на жизнь человека мало, он попросту может игнорировать симптомы и не обращаться к врачу. Во-вторых, признаки астмы эпизодического течения схожи с признаками других болезней органов дыхания, например, хронического бронхита. В-третьих, чаще всего эпизодическая астма смешанная, то есть в ее возникновении одинаковую роль играют аллергический и инфекционно-зависимый факторы. Недуг может возникать у взрослых при контакте с аллергенами, у детей – во время инфекционных болезней нижних дыхательных путей.
Для подтверждения диагноза больного обследуют:
- Возьмут у него общие анализы крови и мочи;
- Сделают кожные аллергопробы;
- Проведут рентгенологическое исследование органов грудной клетки;
- Исследуют функцию внешнего дыхания с бета2-агонистом.
Адекватное лечение, предпринятое еще тогда, когда болезнь не набрала обороты, поможет сдержать ее и добиться стойкой ремиссии. Оно включает в себя прием бета2-агонистов короткого действия и теофиллинов короткого действия с целью купировать эпизодические приступы или не допустить их (лекарства принимаются ингаляционно или перорально перед физической нагрузкой, возможным контактом с аллергенами). Людям с астмой легкого интермиттирующего течения также необходимо придерживаться режима, установленного для астматических больных. Лечение противовоспалительными препаратами им, обычно, не требуется.
2. Бронхиальную астму персистирующего (постоянного) течения. В свою очередь, постоянная астма может быть легкой, среднетяжелой и тяжелой формы.
Если недуг протекает в легкой персистирующей форме, пиковая скорость выдоха у больного составляет 80% от должного, в течение суток может колебаться на 20-30%. Приступы кашля, одышки, удушья случаются у него днем от 1 раза в день до 1 раза в неделю. Приступы в ночное время повторяются чаще 2 раз в месяц. Симптомы болезни во время обострения сказываются на качестве жизни больного, из-за них могут страдать его дневная активность или ночной сон.
Больному с астмой легкой персистирующей формы необходимо ежедневное лечение. Для профилактики приступов ему необходимо использовать ингаляционные кортикостероиды, кромогликат натрия, недокромил, а также теофиллины. Изначально кортикостероиды назначаются в дозе 200-500 мкг в сутки, если же бронхиальная астма прогрессирует, их целесообразно увеличить до 750-800 мкг в сутки. Перед сном рекомендуется применить бронходилататор пролонгированного действия, например, Кленбутерол, Салметерол или Формотерол.
Бронхиальная астма персистирующая среднетяжелого течения характеризуется частым проявлением симптомов, которые существенно нарушают дневную активность больного и его ночной сон. Ночью приступы кашля, удушья, одышки случаются 1 раз в неделю и чаще. Показатель пиковой скорости выдоха колеблется между 60% и 80% от должного.
Если у человека диагностирована эта форма астмы, он нуждается в ежедневном приеме бета2-агонистов и противовоспалительных препаратов, только таким образом удается контролировать болезнь. Рекомендован беклометазона дипропионат или аналоговый ингаляционный кортикостероид в дозе 800-2000 мкг. Дополнительно к нему необходим прием бронходилататоров длительного действия, а, особенно, если приступы часто случаются ночью. Обычно, применяются теофиллины, например, Теофил.
Персистирующая астма тяжелого течения часто смешанная. Частые обострения, повторяющиеся ежедневно и практически еженощно приступы, провоцируются триггерами астмы аллергического и инфекционного характера. Пиковая скорость выдоха у больного составляет менее 60% от должного, колеблется на 30% и более. Из-за тяжелого состояния он вынужден ограничить собственную физическую активность.
Персистирующая бронхиальная астма тяжелого течения контролируется с трудом либо вовсе не контролируется. Чтобы оценить тяжесть состояния больного, необходима ежедневная пикфлуометрия.
Лечение этой формы болезни проводится с целью минимизации проявления симптомов.
Больному ежедневно показаны высокие дозы кортикостероидов (именно поэтому персистирующая астма тяжелого течения иногда называется стероидозависимой). Принимать их он может через ингалятор или спейсер.
Спейсер представляет собой колбу (резервуар), используемую дополнительно к аэрозольному ингалятору с целью усиления эффективности его воздействия. Используя карманный баллончик со спейсером, больной даже с тяжелым приступом удушья сможет оказать себе помощь. Ему не нужно будет координировать вдох и нажатие. Детям лучше применять спейсер с маской.
Человеку, у которого диагностирована персистирующая бронхиальная астма тяжелой степени, рекомендовано:
- Лечение высокой дозой кортикостероидов.
При этом наименьшей является та, которая позволяет контролировать симптомы недуга. Как только лечение возымеет эффект, дозу можно будет снизить. Системные глюкокортикостероиды, которыми возможно лечение тяжелой астмы, это Дексазон, Дексакорт, Дипроспан, Гидрокортизон, Будесонид, Преднизолон, Фликсотид. Они могут быть в форме ингаляционных аэрозолей, таблеток, капельных растворов. - Лечение бронхолитиками.
К таким относятся метилксантины (Аминофиллин, Эуфиллин, Теопек, Неотеопек, Теотард), бета2-агонисты (Серевент, Вентолин, Сальбутомол, Беротек), холинолитики (Атровент, Беродуал). - Лечение нестероидными противовоспалительными.
Если бронхиальная астма смешанная, ее приступы провоцируются не только аллергенами, но также физическим усилием, вдыханием холодного воздуха, больным рекомендовано лечение препаратами на основе кромогликата натрия или недокромила натрия. Чаще всего назначают Интал или Тайлед Минт.
Очевидно, что больной с тяжелой степенью постоянной астмы вынужден принимать огромное количество контролирующих ее симптомы препаратов. К сожалению, эффективны они не всегда, а вот побочные эффекты от их приема наблюдаются довольно часто. Тяжелая смешанная астма преимущественно лечится в стационаре, поэтому медикаментозная терапия подбирается исключительно опытным врачом. Любая самодеятельность в лечении исключена, так как чревата усугублением состояния вплоть до летального исхода.
После того, как началось лечение, и оно дает результат, у больного определяется смешанная клиника болезни, так как в ответ на терапию ее симптомы смазываются. Но сменить диагноз с персистирующей астмы тяжелого течения на течение среднетяжелое можно будет только тогда, когда больной начнет получать медикаментозную терапию, характерную для данной степени тяжести.
источник
Чтобы избавиться от симптомов астмы, врачи подбирают схемы терапии для достижения контроля над патологическими процессами. Одним из подходов является ступенчатое лечение бронхиальной астмы.
Благодаря такой тактике удается облегчит состояние астматика и контролировать в дальнейшем болезнь.
Ступенчатое лечение астмы представляет собой процесс, при котором увеличивают количество и дозировку препаратов, если не получается уменьшить интенсивность проявлений заболевания и контролировать болезнь.
Изначально врач определяет степень тяжести патологии. Легкая степень соответствует первой ступени терапии, при тяжелых патологических процессах лечение начинают с 3-й или 4-й ступени.
Благодаря индивидуальному подходу удается контролировать течение болезни, используя минимальное количество лекарств.
В процессе приема лекарств проводят непрерывную оценку их эффективности и по показаниям корректируют назначения. Если выбранная тактика не приносит желаемых результатов и состояние больного ухудшается, дозировки увеличивают (переходят на ступень выше). Так делают до стабилизации или улучшения состояния астматика.
Составляющие процесса лечения астмы:
- Оценка контроля над болезнью.
- Терапия, которая направляется на достижение контроля.
- Наблюдение за пациентом.
При бронхиальной астме целями ступенчатой терапии являются:
- уменьшение бронхиальной обструкции;
- снижение необходимости в бронхолитических препаратах;
- повышение активности пациентов и их улучшение качества жизни;
- улучшение показателей внешнего дыхания;
- предотвращение приступов;
- устранение факторов, провоцирующих обострение болезни.
Состояние больных оценивают перед курсом терапии, чтобы определить дозировки и схему приема препаратов. Это необходимо для предупреждения приступов удушья.
Если удается добиться эффективного контроля бронхиальной астмы на протяжении не менее трех месяцев от начала курса, дозировки снижают.
При ступенчатом подходе к лечению врач учитывает состояние пациента, частоту приступов, а затем прописывает медикаменты. Если назначения обеспечивают контроль над астмой, постепенно снижают объем прописанных препаратов или их дозировки.
При частичном контроле патологии рассматривают вопрос об увеличении доз лекарственных средств или добавлении других препаратов.
Для больных с прогрессирующей астмой, ранее не получавших адекватного лечения, курс начинают со второй ступени. Если приступы бронхоспазма возникают ежедневно, астматику показано лечение сразу с третьей ступени.
На каждом этапе терапии больные используют лекарства неотложной помощи в зависимости от потребностей, чтобы быстро купировать симптомы удушья.
Эффективность лечения возрастает от 1 ступени. Врач подбирает тактику в зависимости от степени тяжести бронхиальной астмы:
- Легкая интермиттирующая, или эпизодическая. Наблюдают не более двух приступов бронхоспазма в месяц только после воздействия провоцирующих факторов. В периоды ремиссии самочувствие человека удовлетворительное. Больной не нуждается в длительном лечении. Назначают лекарства только для профилактики приступов.
- Легкая персистирующая. Приступы чаще 1 раза в неделю. У астматика возникают бронхоспазмы ночью (не более 2 раз в месяц). В период обострений снижается физическая активность и нарушается сон.
- Персистирующая средней степени. У пациентов возникают ежедневные приступы днем и ночью (не более 1 раза в неделю). Активность астматиков снижена. Необходим постоянный контроль над патологией.
- Персистирующая тяжелая. Ежедневные приступы днем и в ночное время (более 1 раза в неделю) с ухудшением качества жизни. Обострения развиваются еженедельно.
Лечение бронхиальной астмы по ступеням позволяет устранить симптоматику заболевания и увеличить межприступные периоды.
Тактику подбирают в зависимости от степени тяжести болезни.
Предполагает прием только препаратов неотложной помощи. Тактику выбирают для тех больных, которые не получают поддерживающего лечения и периодически испытывают признаки астмы днем.
Обычно обострение происходит не чаще двух раз в месяц. Лекарствами для купирования удушья являются аэрозольные β2-агонисты с быстрым действием. Уже через 3 минуты средства купируют симптоматику, расширяя бронхи.
Возможными альтернативными медикаментами являются β2-агонисты для перорального применения или теофиллины короткого действия, ингаляционные антихолинергические лекарства. Но эффект от этих средств наступает медленнее.
Если приступ удушья возникает на фоне физической нагрузки, назначают ингаляционные средства короткого или быстрого действия в качестве профилактики.
Можно также применять эти лекарства и после нагрузки, если возникают признаки астмы. В качестве альтернативных препаратов используют кромоны – лекарства от аллергии.
Пациентам также рекомендуют увеличивать продолжительность разминки перед физической нагрузкой, чтобы снизить риск бронхоспазма. При интермиттирующей форме не назначают медикаменты для долговременного лечения. Однако если частота приступов увеличивается, врач переходит на вторую ступень.
Тактика подбирается для людей с легкой персистирующей формой болезни. Астматикам приходится принимать ежедневно лекарственные средства для профилактики бронхоспазмов и контроля над патологией.
В первую очередь врач прописывает противовоспалительные кортикостероидные препараты в низких дозировках для приема 1 раз в сутки. Для устранения бронхоспазма применяют быстродействующие медикаменты.
В качестве альтернативных средств в случае отказа пациента от гормонов могут назначить антилейкотриеновые препараты, снимающие воспаление.
Такие медикаменты показаны также при аллергических реакциях (ринит) и возникновении нежелательных эффектов от приема глюкокортикоидов. Если удушье возникает ночью, прописывают один из бронходилататоров пролонгированного действия.
Возможно назначение и других препаратов — теофиллинов и кромонов. Однако их действия для поддерживающей терапии недостаточно. Помимо этого, у лекарств есть побочные эффекты, которые ухудшают состояние пациента. При неэффективности терапии переходят на следующую ступень.
При болезни средней тяжести назначают лекарства для устранения приступа и один или два препарата для контроля течения патологии. Обычно врач прописывает следующую комбинацию:
- ингаляционные глюкокортикоиды в небольших дозах;
- β2-агонист пролонгированного действия.
При таком сочетании пациент получает гормональные препараты в более низких дозировках, а эффект терапии не снижается. Если же контроль над болезнью не был достигнут в течение трех месяцев лечения, дозу аэрозольных гормональных средств увеличивают.
Приступ бронхоспазма рекомендуют купировать пролонгированными β2-агонистами с быстрым эффектом, например. Препаратами, содержащими формотерол. Для усиления терапевтического действия сочетают это вещество с будесонидом.
В качестве альтернативного лечения предлагают больным такую комбинацию медикаментов:
- ингаляционные глюкокортикоиды в низких дозах;
- антилейкотриеновые лекарства или малые дозы теофиллинов.
Пациентам рекомендуют использовать ингаляторы со спейсерами, которые помогают равномерно распределить лекарство.
Если требуется дополнительное лечение пероральными кортикостероидами, а симптоматика усиливается, переходят к следующему шагу терапии.
На 4 ступени обязательно назначают средства неотложной помощи и несколько лекарств для поддерживающей терапии. Выбор медикаментов зависит от лечения на предыдущих этапах. Врачи предпочитают следующую комбинацию:
- ингаляционные глюкокортикоиды в средних или высоких дозах;
- ингаляционные β2-агонисты пролонгированного действия;
- один из препаратов при необходимости: теофиллин замедленного действия, антилейкотриеновые лекарства, пероральный β2-агонист пролонгированного действия, пероральный кортикостероид.
Увеличение дозировок гормональных препаратов необходимо в качестве временного лечения. Если спустя полгода эффекта нет, дозу снижают из-за риска развития нежелательных действий.
Повышают эффективность лечения следующие комбинации:
- антилейкотриеновые препараты с гормонами в средних и малых дозах;
- пролонгированные бета2-агонисты с гормонами в низких дозах с добавлением теофиллинов замедленного высвобождения.
Увеличение частоты приема препаратов с будесонидом также повышает шансы на достижение контроля над болезнью. Если есть побочные действия бета2-агонистов, прописывают антихолинергическое средство, содержащее ипратропия бромид.
Тактику выбирают при тяжелой форме астмы. Чаще проводят терапию в условиях стационара. Пациентам назначают следующие препараты:
- ингаляционные лекарства для неотложной помощи;
- ингаляционные глюкокортикоиды в высоких дозах;
- β2-агонист пролонгированного действия;
- антитела к иммуноглобулину Е;
- глюкокортикоиды в пероральной форме (при неконтролируемой астме и частых обострениях);
- теофиллин.
Для всех 5 ступеней лечения бронхиальной астмы обязательным является сохранение контроля над болезнью в течение трех месяцев.
Затем врач принимает решение об уменьшении количества принимаемых препаратов или снижении их дозировки с целью установить минимальный объем терапии.
Ступенчатая терапия бронхиальной астмы любой формы у подростков и детей практически не отличается от лечения взрослых людей. Терапия начинается с установления тяжести течения болезни.
Особую роль при назначении препаратов врач уделяет их побочным действиям. Отличиями проведения лечения у детей являются:
- При персистирующей форме без отставания в росте проводят длительную терапию противовоспалительными средствами.
- При легкой стадии болезни прописывают ингаляционные глюкокортикоиды в дозах, которые не вызывают побочных действий у ребенка. В качестве альтернативы предлагают препараты, содержащие ипратропия бромид, в форме, которая соответствует возрасту.
- Препаратами второй линии являются кромоны (противоаллергические средства).
- При патологии средней тяжести назначают дозированные ингаляционные глюкокортикоиды. Рекомендуют использовать спейсеры. Другим вариантом терапии является комбинация гормонов с ингаляционными β2-агонистами длительного действия (разрешены детям с 4 лет).
- Для профилактики приступов ребенку до 4 лет назначают пероральный β2-агонист вечером.
При тяжелой форме болезни, когда симптомы беспокоят ребенка регулярно, нарушается качество сна и развивается эмфизема, назначают лечение ингаляционными гормонами.
В комплекс терапии включают ингаляции с использованием β2-симпатомиметиков пролонгированного действия (1–2 раза) и пероральные гормоны. В качестве препаратов неотложной помощи можно применять комбинацию будесонида и формотерола.
Ингаляционная терапия у новорожденных детей имеет особенности:
- Использование реактивного распылителя с компрессором. При приступе применяют препараты, содержащие фенотерол, сальбутамол, для длительной терапии – лекарства с будесонидом, кромоглициевой кислотой.
- Использование дозированных аэрозолей со спейсером и маской.
- При развитии гипоксии показана кислородная маска.
- В неотложных состояниях β2-симпатомиметики вводят внутривенно. При нарастании симптоматики вводят адреналин подкожно и переводят младенца на искусственную вентиляцию легких.
Медикаментозное лечение детей дополняют иммунотерапией. Ликвидируют также потенциальные источники аллергенов.
Системы для ингаляции должны соответствовать требованиям детского возраста. Дети с 7 лет могут переводиться на дозированный аэрозоль.
Критериями эффективной терапии бронхиальной астмы являются:
- Снижение выраженности симптоматики.
- Устранение приступов по ночам.
- Уменьшение частоты обострений заболевания.
- Снижение дозировок β2-агонистов.
- Повышение активности пациентов.
- Полный контроль над заболеванием.
- Отсутствие нежелательных эффектов от препаратов.
Врач наблюдает за пациентом после назначений и оценивает ответ организма на прописанную дозу лекарств. При необходимости дозировку корректируют.
В основе ступенчатого подхода к лечению лежит определение минимальной поддерживающей дозы препаратов.
Хорошим ответом на применение β2-агонистов при приступе является их действие на протяжении 4 часов.
При неполном ответе на действие препарата в комплекс терапии включают пероральные гормоны и ингаляции антихолинергическими средствами. В случае плохого ответа вызывают врача. Пациент доставляется в отделение интенсивной терапии.
Чтобы сделать переход на уровень ниже, пересматривают эффективность терапии каждые полгода или 3 месяца. Если контроль над патологией сохраняется, могут постепенно снижать объем назначений.
Это уменьшает риск проявления у пациентов побочных действий препаратов и улучшает восприимчивость к дальнейшей терапии.
Переходят к следующей ступени таким образом: снижают дозировку основного препарата или отменяют лекарства для поддерживающей терапии. В ходе изменения тактики лечения проводят наблюдение за пациентами.
Если нет ухудшения состояния, назначают монотерапию – переходят на 2 ступень. В дальнейшем возможен переход на первую ступень.
Лечение, которое предлагают при бронхиальной астме на каждом этапе, не является общим для всех пациентов.
Чтобы добиться контроля над заболеванием, необходимо составление индивидуального плана для каждого с учетом возраста, особенностей болезни, сопутствующих патологий.
Таким образом можно значительно снизить риск обострений, продлить периоды ремиссии, устранить или смягчить симптоматику.
Четкая схема терапии и конкретные рекомендации врачей позволяют пациенту стать физически активным человеком и вести полноценную жизнь.
источник
Лечение должно проводиться в отделении интенсивной терапии и начинаться немедленно.
Основой лечения тяжёлой острой астмы (ТОА) является многократное назначение быстродействующего ингаляционного в2-агониста,раннее назначение системных глюкокортикостероидов (ГКС) и ингаляции кислорода.
Эти лечебные методы, назначаемые параллельно, относятся к терапии первой линии.
Назначение в2-агонистов показано всем больным независимо от того, получал или нет эти препараты больной до госпитализации. Отсутствие эффекта от их применения в домашних условиях объясняется недостаточной дозировкой или неправильной техникой ингаляции. Тахикардия не является противопоказанием для назначения в2-агонистов, поскольку у больных ТОА, как правило, она связана с гипоксией и уменьшается при применении в2-агонистов.
Предпочтение отдаётся введению в2-агонистов через небулайзер: в первый час проводят 3 ингаляции по 2,5-5 мг сальбутамола или по 0,5-0,75 мг беротека каждые 20 мин.
Бронхорасширяющий эффект обычно наблюдается через 10-15 минут после первой ингаляции. Затем ингаляции проводят в той же дозе каждый час до заметного улучшения состояния и до достижения SatО2 до 92 % и более. После этого препарат назначают каждые 4-5 часов. При использовании для ингаляций тербуталина дозы должны быть в 2 раза выше.
При отсутствии небулайзера ингаляции можно проводить с использованием дозированного аэрозольного ингалятора со спейсером. Б?льшая эффективность достигается при использовании спейсера большого объёма (до 750 мл), оснащенного однонаправленным клапаном вдоха.
Однократная доза сальбутамола при использовании ингалятора со спейсером составляет 400-500 мкг (4-5 вдохов), кратность введения обычно такая же, как и при лечении через небулайзер. Эффективность такого лечения не ниже, чем при использовании небулайзера. Преимущества его заключаются в более быстром развитии бронхорасширяющего эффекта, снижении используемой дозы в2-агониста и значительной экономической эффективности.
ГКС являются наиболее эффективными препаратами для лечения тяжёлой острой астмы. Механизм их действия связан с противовоспалительным эффектом (за счёт снижения активации воспалительных клеток в просвете дыхательных путей и снижения сосудистой проницаемости), восстановлением чувствительности в2-адренорецепторов к симпатомиметикам, снижением продукции бронхиального секрета.
Эффект от назначения глюкокортикостероидов наступает не ранее, чем через 4-6 часов (в течение суток от начала применения). Поэтому рекомендуется как можно более раннее их назначение (на уровне первичной помощи). Одинаково эффективным считается как внутривенный, так и пероральный путь введения ГКС.
Отечественные авторы на начальном этапе лечения отдают предпочтение внутривенному ведению глюкокортикостероидов. Наиболее часто используются три препарата ГКС: метилпреднизолон, преднизолон и гидрокортизон, которые при ТОА обладают одинаковой клинической эффективностью, однако предпочтительнее использование метилпреднизолона, который обладает наименьшей минералокортикоидной активностью.
Рекомендуются следующие схемы лечения: по 40-125 (в среднем 60-80 мг) метилпреднизолона или 125-200 (в среднем 150-175 мг) гидрокортизона каждые 6 часов до достижения клинического улучшения (как минимум в течение 2-х суток). В дальнейшем пациент переводится на пероральный приём препарата (40-80, в среднем 60 мг в сутки).
Если у пациента имеются признаки прогрессирования ТОА (увеличение зон «немого» легкого, нарастание гипотонии и т.д.), то используются максимальные дозировки глюкокортикостероидов. Гормональная терапия обычно проводится в течение 10-14 дней. После этого ГКС сохраняют лишь у больных, имевших гормональную зависимость до развития тяжёлой острой астмы. Для повышения эффективности лечения к системным глюкокортикостероидам можно подключить ингаляционные ГКС.
Альтернативой назначения системных глюкокортикостероидов может быть применение ингаляционных глюкокортикостероидов (ИГКС), а именно суспензии пульмикорта (будесонида) через небулайзер. Однако это допустимо лишь у больных без стероидозависимой бронхиальной астмы (БА). При этом через небулайзер вводят и бронхолитики.
В молодом и среднем возрасте рекомендуется назначать в2-агонисты (беротек, сальбутамол) в указанных выше дозах; пожилым пациентам при сочетании БА с ишемической болезнбю сердца (ИБС) назначают атровент, а при сочетании с артериальной гипертензией (АГ) и хронической обструктивной болезнью легких (ХОБЛ) рекомендуется беродуал (дозы их при ингаляции через небулайзер указаны ниже). Суспензию пульмикорта назначают по 2 мг дважды в сутки через 20-30 мин после ингаляции раствора бронхолитика (суточная доза может быть увеличена до 6-8 мг).
Необходимо иметь в виду, что дозы бронхолитиков, поступающих через небулайзер, на порядок выше, чем при ингаляции с помощью дозируемых ингаляторов. В связи с этим при применении в2-агонистов возможно развитие таких осложнений, как тахикардия, ишемия миокарда вплоть до развития некоронарогенных некрозов, желудочковые экстрасистолы, связанные как с воздействием препарата на адренорецепторы миокарда, так и с развитием гипокалиемии.
Точно также введение больших доз пульмикорта через небулайзер может вызвать нежелательные явления. При этом могут развиться как системные (угнетение функции коры надпочечников, остеопороз, задержка роста у детей), так и местные (кандидоз, раздражение слизистой оболочки полости рта; дисфункция и охриплость голоса; кашель) побочные реакции.
В связи с этим небулайзерную терапию бронхолитиками и суспензией пульмикорта проводят до 5-7 дней, после чего переходят на введение этих препаратов через дозируемый ингалятор.
У подавляющего большинства больных ТОА наблюдается гипоксемия, требующая кислородотерапии. Наряду с этим кислородотерапия увеличивает эффективность фармакотерапии, в частности повышает чувствительность в2-рецепторов к в2-агонистам. При ТОА основными причинами гипоксемии являются нарушение вентиляционно-перфузионного отношения и повышенное потребление кислорода вследствие чрезмерной работы дыхательной мускулатуры.
Шунтирование крови не имеет такого значения в генезе гипоксемии, как при ХОБЛ. В связи с этим в большинстве случаев удаётся достичь достаточных насыщения крови кислородом (до 90-92 %) и напряжения артериальной крови кислородом (РаО2 > 70 мм рт. ст.) при использовании небольших доз кислорода.
Кислород назначается через носовые канюли или маску со скоростью подачи 1-4 л/мин. При этом в дыхательные пути ингалируется 24-40 % кислород. В наиболее тяжёлых случаях на начальном этапе лечения приходится увеличивать концентрацию вдыхаемого кислорода до 50-60 %, для чего соответственно увеличивается скорость подачи кислорода. Длительное введение кислорода высокой концентрации (выше 50 %) оказывает токсическое действие на слизистую оболочку бронхов и ухудшает отделение мокроты.
Помимо этого, при выраженной дыхательной недостаточности, сопровождающейся увеличением в крови РаСО2, возбудимость дыхательного центра поддерживается не только гиперкапнией, но и гипоксемией и чрезмерно быстрое устранение последней приводит к угнетению дыхательного центра, снижению вентиляции, задержке выделения углекислоты и нарастанию дыхательной недостаточности.
Во всех случаях, когда с помощью ингаляции кислорода в небольшой и средней дозировках не удаётся достичь необходимых SatO2 и РаО2, следует исключить увеличение доли шунтового механизма в генезе гипоксемии. Это может быть связано с развитием пневмонии, ателектаза, пневмоторакса, легочной эмболии, для исключения которых необходимо провести соответствующие исследования.
В наиболее тяжёлых случаях, при нарастании бронхиальной обструкции и появлении зон «немого» легкого, для борьбы с гипоксемией рекомендуется использовать гелий-кислородную смесь (гелиокс), содержащую 75 % гелия и 25 % кислорода. Благодаря низкой плотности гелия такая смесь легче проникает в плохо вентилируемые участки легких и улучшает газообмен. Гелиокс вводят с помощью маски с расходным мешком или подают в инспираторный контур пациента при проведении искусственной вентиляции лёгких (ИВЛ).
К терапии второй линии относится применение антихолинергического препарата быстрого действия ипратропиума бромида (ИБ) — атровента, препаратов теофиллина и парентеральных форм в2-агонистов.
Показанием для назначения ИБ являются рефрактерность больных к в2-агонистам. Безусловным показанием к назначению ИБ является также бронхоспазм, вызванный ошибочным приемом в2-блокаторов. ИБ рекомендуется вводить с помощью небулайзера в дозе 0,5 мг: первые 3 дозы каждые 30 мин, затем через 2-4 часа по необходимости.
При отсутствии небулайзера ИБ можно вводить с такой же кратностью с помощью дозированного ингалятора со спейсером по 0,2 мг (10 доз) на одну ингаляцию. По сравнению с в2-агонистами пик действия ИБ наступает позднее (через 0,5-1 час), а продолжительность действия составляет 4-6 часов.
Определённые преимущества имеются при комбинированной терапии ИБ с в2-агонистами. В этих случаях бронхорасширяющий эффект обеспечивается за счёт двойного механизма действия: симпатомиметического и антихолинергического. В связи с этим комбинированная терапия может вызвать более выраженную бронходилатацию, чем каждый препарат по отдельности.
Комбинированная терапия показана больным тяжёлой острой астмы с очень резко выраженной бронхиальной обструкцией (при абсолютном снижении пиковой скорости выдоха (ПСВ) 45-50 % от должного или индивидуального лучшего показателя. Лечение беродуалом должно предшествовать назначению препаратов теофиллина: последние назначаются лишь при неэффективности беродуала.
Для лечения ТОА используются только внутривенные формы теофиллина — эуфиллин и аминофиллин. Помимо слабого бронхолитического действия, у теофиллинов имеются противовоспалительные, иммуномодулирующие и бронхопротекторные свойства. Кроме того, теофиллины снижают давление в малом круге, усиливают центральную инспираторную активность, уменьшают утомление дыхательной мускулатуры и усиливают мукоцилиарный клиренс.
Многие авторы считают, что именно этими механизмами действия препаратов теофиллина, не связанными с бронхолитическим эффектом, объясняется их клиническая эффективность при ТОА. Наряду с этим, у теофиллинов имеется большое число побочных эффектов: головная боль, тошнота, бессонница, энцефалопатия, неблагоприятное действие на коронарное кровообращение у больных ИБС, электролитные расстройства, в том числе потенциально летальные (аритмии сердца, судороги). При этом токсическая концентрация теофиллина в крови вплотную примыкает к терапевтической концентрации.
В связи с этим теофиллины не относятся к основным средствам лечения тяжёлая острой астмы. Их использование может быть рекомендовано только у больных ТОА, рефрактерных к терапии первой линии, которая проводилась не менее 4 часов и при отсутствии противопоказаний для их использования. Вначале вводится струйно медленно болюсная доза эуфиллина из расчёта 5-6 мг/кг в течение 20 мин.
После этого внутривенное введение эуфиллина продолжают в поддерживающей дозе (от 0,5 до 0,9 мг/кг/ч) до улучшения клинического состояния. При этом суточная доза эуфиллина может достигать 1,5-2 г, что превышает допустимые фармакологические дозы. Поэтому лечение эуфиллином необходимо проводить под строгим врачебным контролем для своевременного выявления побочных эффектов. Крайне желательно следить за концентрацией препарата в крови (особенно в первые 6 часов от начала лечения), которая должна составлять 10-15 мг/л.
Показанием для парентерального введения в2-агонистов является отсутствие или недостаточный эффект от введения высоких доз в2-агонистов через небулайзер. В таких случаях лечение можно дополнить внутривенной капельной инфузией в течение 1 часа 0,5 мг сальбутамола или тербуталина.
Некоторые авторы в таких ситуациях рекомендуют подкожное введение адреналина (0,3 мг) или тербуталина (0,25 мг): в первый час через каждые 20 мин, в последующем — через 4-6 часов. Учитывая высокий риск развития сердечно-сосудистых осложнений, парентеральное введение в2-агонистов рекомендуется пациентам не старше 40 лет и без заболеваний сердца в анамнезе.
К терапии второй линии мы относим также восполнение дефицита жидкости в организме, который имеется у большинства больных ТОА. Такое лечение не только восстанавливает объём циркулирующей крови, устраняет сгущение крови и дефицит внеклеточной жидкости, но и нормализует электролитный баланс, способствует разжижению бронхиального секрета, улучшает отделение мокроты и проходимость бронхов.
Если больной находится в сознании, то ему рекомендуется больше употреблять жидкости. У больных с выраженной дыхательной недостаточностью и с нарушением сознания проводится инфузионная терапия. В первые сутки вводят около 3-4 л жидкости (изотонического раствора NaCl, раствора Рингера, 5 % раствора глюкозы, реополиглюкина), в последующие дни — 1,6 л/м 2 поверхности тела.
Вливания проводят через интравенозный катетер под контролем центрального венозного давления, которое не должно превышать 12 мм вод. ст. и почасового диуреза, который без применения диуретиков должен увеличиться до 80 мл.
Для улучшения реологических свойств крови и профилактики тромбоэмболических осложнений, вероятность которых повышается при наличии интравенозного катетера, рекомендуется гепарин (20 тыс. ЕД в сутки).
Применяют также отхаркивающие и муколитические препараты с учётом их переносимости (корень алтея или трава термопсиса, бромгексин, лазолван). С этой же целью назначают паракислородные ингаляции, перкуссионный и вибрационный массаж грудной клетки, «вспомогательный кашель» (аппаратное сдавливание грудной клетки синхронно с кашлевыми толчками больного). Ингаляции лекарственных средств, в частности муколитиков (ацетилцистеин и др.), нежелательны, так как могут усилить бронхиальную обструкцию.
В последние годы показано, что у больных, рефрактерных к в2-агонистам, лечебный эффект может оказать внутривенное введение (в течение 20 мин) 2 г магния сульфата. Предполагается, что магния сульфат блокирует кальциевые каналы гладкой мускулатуры бронхов и препятствует высвобождению ацетилхолина из нервных окончаний. Этими механизмами обеспечивается бронходилатирущий эффект.
Чёткие установки должны быть у врача на применение антибиотиков и диуретиков. Профилактическое применение антибиотиков недопустимо. Антибиотики применяются лишь при бактериальном обострении бронхита с выделением гнойной мокроты, а также при пневмонии, подтверждённой рентгенологически, и при синусите. Антибиотиками выбора при ТОА являются макролиды, цефалоспорины, амоксициллин. При наличии отечного синдрома, связанного с декомпенсацией легочного сердца, и при повышении центрального венозного давления до 15 см вод. ст. и выше показаны диуретики.
При развитии выраженного дыхательного ацидоза со снижением рН до 7,2-7,15 внутривенно вводят 50-100 мл и более 5 % раствора гидрокарбоната натрия, стремясь довести рН до 7,3-7,35.
При ТОА абсолютно противопоказаны наркотики (морфин, промедол) и все препараты с седативным эффектом (транквилизаторы, оксибутират натрия и др.), поскольку они угнетают дыхание, подавляют кашлевой рефлекс и ухудшают дренажную функцию бронхов.
Если консервативные методы лечения тяжёлой острой астмы оказались неэффективными, то больного интубируют и проводят ИВЛ. Определение момента для интубации налагает на врача большую ответственность. Это связано, с одной стороны, с тем, что интубация и ИВЛ сами по себе могут вызвать серьёзные осложнения и ассоциируются с высокой летальностью, с другой — задержка с респираторным пособием приводит к неизбежному летальному исходу.
Показаниями для интубации и ИВЛ при ТОА являются : остановка или резкое угнетение дыхания, прекращение сердечной деятельности, выраженное возбуждение больного, требующее применения седативной терапии, спутанность сознания или состояние комы. Если пациент находится на лечении, то вопрос об интубации рассматривается при ухудшении общего состояния, участии в дыхании вспомогательной мускулатуры, изменении реакций и речи больного, нарастании цианоза и зон «немого» легкого, учащении дыхания до 35-40 в 1 мин и более.
В таких случаях определяют ПСВ и газы крови. Величина ПСВ ниже 30 % от наилучшего индивидуального значения, резкая гипоксемия (ниже 50-55 мм рт. ст.) и особенно гиперкапния до 55-60 мм рт. ст. и выше являются показаниями для интубации и проведения ИВЛ.
Летальность при ТОА существенно зависит от того, в каком состоянии поступил больной в отделение интенсивной терапии. Летальность резко повышается у пациентов, поступивших с наличием массивных зон «немого» легкого, нарушением сознания, с выраженной гипоксемией и гиперкапнией. В остальных случаях при правильной оценке степени тяжести и адекватном лечении прогноз для жизни обычно благоприятный. Однако и здесь свою лепту в исход ТОА может внести наличие у больных (особенно пожилого возраста) тяжёлых сопутствующих заболеваний, в частности сердечно-сосудистой системы.
Причиной смерти чаще всего является асфиксия, обусловленная обтурацией бронхов вязким секретом и отёком слизистой оболочки бронхов, в меньшей степени — бронхоспазмом. Другими словами, больной умирает от тяжёлая острой астмы и связанной с ним острой дыхательной недостаточностью, которые не удалось купировать.
Значительно реже основной причиной смерти являются нарастающая легочно-сердечная недостаточность, острая коронарная недостаточность и сложные нарушения сердечного ритма, которые связаны с развитием резкой гипоксии, ацидоза и электролитных нарушений. В качестве редких причин смерти называются также массивная двусторонняя пневмония, острая надпочечниковая недостаточность, тромбоэмболия легочной артерии, развитие синдрома диссеминированного внутрисосудистого свёртывания крови.
В ряде случаев смерть больного с ТОА связана с проводимым лечением. На первом месте стоит спонтанный напряжённый пневмоторакс, который может быть непосредственным осложнением ТОА или же связан с ИВЛ и пункцией подключичной вены. Неблагоприятный исход может быть обусловлен остановкой сердца при длительной ИВЛ.
Тяжёлые нарушения сердечного ритма могут быть обусловлены применением эуфиллина, а развитие повреждений миокарда — с использованием в2-агонистов, у которых имеется небольшое кардиотоксическое действие, которое возрастает в условиях гипоксии и гиперкапнии. В этих случаях при их применении могут развиться некоронарогенные очаги некроза в миокарде.
Данная форма ТОА отличается бурным развитием и отсутствием снижения чувствительности в2-адренорецепторов к в2-агонистам. Такая форма ТОА обычно развивается совершенно неожиданно при массивном контакте с аллергенами, психоэмоциональном стрессе, а чаще — в момент введения (или вскоре после него) антибиотиков, сульфаниламидов, протеолитических ферментов, декстрана, вакцин, сывороток и других препаратов. По существу эта форма представляет собой анафилактический шок, связанный с сенсибилизацией к лекарствам.
Помимо генерализованной бронхиальной обструкции, в основном за счёт бронхоспазма, у больных наблюдается падение артериального давления, нитевидный пульс, холодный пот. Состояние катастрофически быстро ухудшается. Нарастают удушье экспираторного характера, диффузный цианоз, появляются моторное возбуждение, сменяющееся апатией и нарушением сознания, судороги и уже через несколько минут (иногда через несколько десятков минут, реже через 1-3 часа) развивается гипоксемически-гиперкапническая кома.
Генез тяжёлой острой астмы с внезапным началом не всегда аллергический. Генерализованный бронхоспазм может возникнуть при приёме нестероидных противовоспалительных препаратов (у больных аспириновой астмой), ошибочном назначении в-адреноблокаторов (особенно неселективных), вдыхании холодного воздуха, резких запахов, действующих как неспецифические раздражители, при нервно-эмоциональном стрессе.
В этих случаях патогенез ТОА связан с повышенной реактивностью бронхов к неспецифическим агентам. Высокая реактивность бронхов наблюдается у больных ТОА с медленным темпом развития во время выхода из этого состояния или вскоре после него. Описаны случаи развития в этот период генерализованного бронхоспазма, т.е. тяжёлая острая астма с внезапным началом, при ингаляции тёплого щелочного раствора, при переводе больного в палату, где имелся запах краски после недавнего ремонта, после ссоры с родственниками и т.д.
ТОА с внезапным началом представляет реальную угрозу для жизни больного и требует энергичных неотложных мероприятий.
1) ограничение поступления в организм веществ, вызвавших ТОА; так, если лекарство, вызвавшее тяжёлою острую астму, введено подкожно или внутримышечно, место инъекции обкалывают адреналином;
2) внутривенное струйное введение симпатомиметиков (0,5 мл 0,1 % раствора адреналина, 1 мл 0,05 % раствора алупента и др.), ГКС (120-150 мг преднизолона или эквивалентной дозы других препаратов), 10 мл 2,4 % эуфиллина, антигистаминных препаратов;
3) внутривенное введение противошоковых растворов;
4) при отсутствии в ближайшие минуты клинического эффекта необходимы интубация трахеи и ИВЛ.
Летальность при ТОА с внезапным началом значительно выше, чем при тяжёлой острой астме с медленным темпом развития.
Саперов В.Н., Андреева И.И., Мусалимова Г.Г.
источник
Лечение тяжелой гормонозависимой бронхиальной астмы гомеопатией требует длительного труда, терпения и взаимопонимания между врачом и пациентом.
✔️Женщина 63 лет, упитанного телосложения, среднего роста.
✔️С детства частые бронхиты, по поводу которых получала много антибиотиков.
✔️С 42 лет появились сильные приступы удушья, в основном в ночное время. Приступы ежедневные и очень часто (несколько раз в неделю) вызывает скорую помощь, так как они трудно купируются и обычными, и гормональными ингаляторами.
✔️Кроме того, 1 раз в 2 месяца получает профилактические курсы стационарного лечения (гормональную пульстерапию по поводу бронхиальной астмы тяж. лечения).
✔️Ежедневно – Полькортолон, ингаляции «Беродуала» и «Сальбутамола» минимум 2-3 раза в день.
✔️Простудных заболеваний не было очень много лет – не помнит сколько.
✔️Самые сильные приступы удушья бывают по ночам в 3-3.30. Приступ проявляется внезапно, больная просыпается с сильным удушающим кашлем, чувством удушья, страхом смерти, садится в кровати, мечется по ней, пытается принимать различные позы, чтобы облегчить дыхание, но без эффекта. Громко стонет, причитает и кричит «Умираю, помогите. ». Кричит так громко, что её соседи всегда знают и слышат, что происходит. Когда приезжает скорая помощь, то об этом знает весь подъезд.
При объективном осмотре : огромные фиолетовые кровоподтеки на теле, особенно на тыле кистей рук (сплошные фиолетово-черные пятна, с размером в ладошку или ½ ладошки).
Отмечает повышенную чувствительность к перемене погоды, особенно на сырую (но чувствительность и к холоду).
Характер: сочувствующая, веселая, болтливая, язвительная, очень работящая, скупая, хитрая. Другие врачи не могли с ней контактировать – оскорбляла насмешками и грубой критикой. Очень прямолинейная, наглая, открытая, легко сходится с людьми, завистливая. Сейчас на пенсии, но подрабатывает бухгалтером в нескольких фирмах. Часто ездит в соседнюю область помогать племяннику, который живёт бедно. Отвозит ему продукты и деньги, которые экономит от своей пенсии. Больше не помогает никому.
Живёт с мужем. Муж – инвалид с тяжелыми проблемами сердечно-сосудистой системы, скучный, но надёжный человек. Жалуется, что никогда не чувствовала с ним женщиной, так как у мужа с молодости импотенция и она научилась себя сексуально сдерживать и делает так всю жизнь. Детей нет, так как у неё первичное бесплодие.
Лечилась 5 лет у классического гомеопата без эффекта (препараты из моли, бабочки в высоких разведениях, раз в 2 недели), Сульфур, Лахезис, Ликоподиум, Кальк. карб, Туберкулинум, Карцинозинум.
Получила гомеопатический препарат, 1М 1 доза.
17.10.2005 позвонила с «благодарностью», что впервые в жизни появились судороги в бедрах и икрах (смотрим в Материя Медика и, если этот симптом принадлежит назначенному гомеопатическому препарату, то это тестовый симптом). Держались судороги 2-3 дня и прекратились. Но ингаляторами стала пользоваться реже днём. В остальном без динамики.
Переведена на тот же препарат в 30С ежедневно 3 раза с 29.10.2005 (так как идёт массивная медикаментозная терапия). Записывала только тяжелые приступы, которые требовали вызова СМП, потому что остальные сосчитать было просто нереально.
С 15 по 29 октября были приступы всего 36 раз, поэтому была изменена схема лечения. Новых симптомов нет. Тот же ГП в 35С 2-3 раза в день.
19.11.2005 – прием. А в это время было ухудшение состояния на погоду и пришлось лечь в стационар – инъекции гормонов в течение 10 дней. Реакция на гормоны стала лучше, чем раньше (повысилась чувствительность). Снижена доза гормонов, ГП 35С 2-3 раза в день.
02.12.2005 – сильных приступов не было, СМП не вызывала ни разу. Экхимозы уменьшились по площади и новых нет. Спит до утра. Тот же ГП 37С 2-3 раза в день.
17.12.2005 – за эти 2 недели 1 раз вызов СМП – тяжелый метеодень. Экхимозы с туловища ушли полностью. Каждые 10 дней смена потенции – ГП 39С,41С,43С по той же схеме.
25.01.2006 – СМП 2 раза – 1 и 13 января, но приступы слабее, чем раньше. Ощущение удушья сменилось ощущением закладывания в груди. Схема лечения та же.
27.02.2006 – за февраль 2 приступа с вызовом СМП. У пациентки с молодости сахарный диабет 2 типа. Появились приливы жара в лице и грудной клетке. Клин анализ крови – норма, глюкоза 6,9, холестерин общий 10,0. Получает тот же ГП 50С 1-2 раза в день.
В начале марта ОРВИ с температурой 38-39, Бриония 30С 2 раза в день на 5 дней, обошлось без антибиотиков. Далее прежнее назначение.
16.11.2006 – летом 2006 бежала в городе по улице, около неё на полном ходу тормозит СМП (её знали все СМП в городе) и врач выскакивает, и говорит «вы ли это, мы уже вас похоронили – столько времени вы нас не вызывали»!))) Сейчас ГП в 100С 1 раз в день. Ингаляторы очень редко, полькортолон по ½ таб. 1 раз через день. Жалуется, что немного отекают лодыжки. Хорошая работоспособность, отличное настроение.
Потом я уехала в Москву и оставила пациентку на другого врача. До сих пор всё прекрасно. Но стали побаливать суставы, продолжает получать старый ГП.
Анализ: Какие мы видим особенности в этом случае и какие надежные и интересные симптомы мы можем взять для поиска ГП?
Приступы эмоционально окрашены, что редко у пациентов с БА, истерический компонент, кричит так, что просыпается подъезд. Это сильный страх смерти с бурным двигательным беспокойством и взрывом эмоций. Как у Аконита и Кактуса. Т.Е. нам нужно искать ГП, который покрывает рубрику **истерия**.
Психоэмоциональная структура : противоречивый характер – от сочувствия до оскорбления, до скупости (всегда очень тяжело платила деньги доктору). Быстрая. Болтливая. Трудоголик (в 7 утра её уже давно нет дома). Потребность во сне небольшая.
Хуже от сырой и холодной погоды, но СМП вызывает ночью – тогда хуже всего.
С момента возникновения БА – желание лимонов. На фоне лечения оно не изменилось. За этим симптомом надо смотреть.
Её долго лечили Лахезисом, они действительно близки. Но нет ухудшений от тепла.
Все это время пациентка получала препарат Тарентула испаника .
На лечении с ней стало легче общаться, ушла злобность, БА стала протекать мягко, отпала необходимость в СМП и стационарном лечении. Пациентка продолжает получать гомеопатическое лечение. Этот случай гормонально зависимой БА тяжелого течения, осложненной сахарным диабетом и бесплодием. В таких случаях надеяться на быстрое излечение нельзя, от пациента и врача требуется много терпения и понимания, т.к. в традиционной медицине такие случаи официально признаются неизлечимыми.
источник
*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Во многих случаях смерть от астмы можно предотвратить, а задержка назначения лечения может привести к фатальному исходу
— невозможность для врача оценить тяжесть состояния с помощью объективных методов;
— недооценка тяжести состояния пациентами или родителями;
— недостаточные дозы кортикостероидов.
Следует относиться к каждому неотложному обращению пациента как к тяжелому обострению астмы, пока не будет доказано обратное.
— симптомов и ответа на самостоятельно проводимые лечебные мероприятия;
— частоты дыхания и сердечных сокращений;
— ПЭП.
У пациентов с тяжелым или угрожающим приступом может не быть приступов дыхательной недостаточности и всех перечисленных нарушений. Наличие одного из нарушений должно вызывать повышенное внимание со стороны врача
Неконтролируемая астма
ОЦЕНКА
Нормальная речь.
Пульс менее 110 в 1 мин.
ПЭП более 50% от должного или лучшего значения.
ВЕДЕНИЕ
Проводить лечение на дому, однако необходимо оценить ответ на лечение до окончания визита.
ЛЕЧЕНИЕ
Сальбутамол 5 мг или тербуталин через небулайзер
МОНИТОРИРОВАНИЕ ОТВЕТА ЧЕРЕЗ 15 30 МИН ПОСЛЕ НЕБУЛИЗАЦИИ
Если ПЭП составляет более 50 — 75% от должного или лучшего значения:
— дать преднизолон 30 — 60 мг;
— повысить ступень лечения.
Если ПЭП составляет более 75% от должного или лучшего значения:
— повысить ступень лечения.
НАБЛЮДЕНИЕ
— Мониторирование симптомов и регистрация ПЭП с построением графика.
— План самоконтроля.
— Посещение специалиста не позднее чем через 48 ч.
— При посещении — коррекция терапии в соответствии с рекомендациями по ведению тяжелой персистирующей астмы.
КРИТЕРИИ ДЛЯ ГОСПИТАЛИЗАЦИИ
— Наличие какого-либо из признаков угрожающего состояния.
— Наличие какого-либо признака, характерного для тяжелого обострения астмы, после начала лечения, особенно значение ПЭП менее 33%.
СНИЗИТЬ СТРОГОСТЬ КРИТЕРИЕВ ДЛЯ ГОСПИТАЛИЗАЦИИ
Приступы в дневное или вечернее время, недавно возникавшие ночные симптомы, недавние госпитализации, данные о предыдущих тяжелых приступах, неспособность пациента к адекватной оценке собственного состояния, социальные условия.
Тяжелое обострение астмы
ОЦЕНКА
— Пациент не способен произнести предложение на одном выдохе.
— Пульс более 110 в 1 мин.
— Частота дыхания более 25 в 1 мин.
— ПЭП до 50% от должного или лучшего значения.
ВЕДЕНИЕ
Серьезные показания к госпитализации при наличии одного из вышеперечисленных показателей
ЛЕЧЕНИЕ
— Кислород 40 — 60%, если доступно.
— Сальбутамол 5 мг или тербуталин 10 мг через небулайзер.
— Преднизолон 30 — 60 мг или гидрокортизон внутривенно 200 мг.
МОНИТОРИРОВАНИЕ ОТВЕТА ЧЕРЕЗ 15 — 30 МИН ПОСЛЕ НЕБУЛИЗАЦИИ
При наличии одного из признаков обстрения тяжелой астмы:
— принять меры к госпитализации;
— повторное введение b 2-агонистов плюс иптратропиум 0,5 мг с помощью небулайзера; или
-подкожная инъекция тербуталина или внутривенное (медленное) введение аминофиллина в ожидании неотложной помощи.
При хорошем ответе на первое проведение ингаляционной терапии с помощью небулайзера (улучшение симптомов, замедление пульса и снижение частоты дыхания, увеличение ПЭП до уровня более 50%):
— повысить ступень обычной терапии и продолжать лечение преднизолоном.
НАБЛЮДЕНИЕ
— Мониторирование симптомов и ПЭП.
— План самоконтроля.
— Посещение специалиста не позднее чем через 24 ч.
При посещении — коррекция терапии в соответствии с рекомендациями по ведению тяжелой персистирующей астмы
Жизнеугрожающие состояния при астме
ОЦЕНКА
— «Немое легкое».
— Цианоз.
— Брадикардия или усталость.
— ПЭП менее 33% от должного или лучшего значения.
ВЕДЕНИЕ
Принять меры к немедленной госпитализации.
ЛЕЧЕНИЕ
— Преднизолон 30 — 60 мг или гидрокортизон внутривенно 200 мг немедленно.
— Небулайзер с потоком кислорода в машине неотложной помощи.
— b 2 -агонист через небулайзер и ипратропиум или подкожная инъекция тербуталина, или внутривенная инъекция аминофиллина (250 мг медленно).
Оставаться с пациентом до прибытия неотложной помощи.
При отсутствии небулайзера провести два впрыскивания b 2 -агониста через спейсер большого объема и повторять 10 — 20 раз.
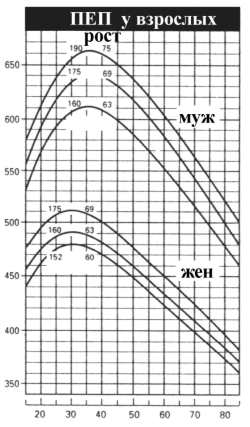
Нормальные показатели ПЭП у взрослых
По оси ординат — ПЭП, л/мин;
По оси ординат — возраст, годы.
источник
Терапия бронхиальной астмы немыслима без применения лекарственных препаратов. С их помощью удается добиться контроля над болезнью, но излечить ее полностью невозможно. Ингаляторы при бронхиальной астме являются лучшим способом введения лекарства в организм.
Все лекарства от астмы делятся на препараты базисной терапии и средства неотложной помощи. При полном контроле над болезнью используется базисная терапия бронхиальной астмы, потребность в препаратах скорой помощи минимальная.
Средства базисной терапии направлены на подавление хронического воспалительного процесса в бронхах. К ним относятся:
- глюкокортикоиды;
- стабилизаторы тучных клеток (кромоны);
- ингибиторы лейкотриенов;
- комбинированные средства.
Рассмотрим эти группы лекарств и самые популярные препараты.
иГКС показаны всем больным с астмой персистирующего течения, поскольку при любой тяжести болезни в слизистой оболочке бронхов присутствует хроническое воспаление. Эти препараты не имеют выраженных побочных эффектов, связанных с системным действием гормонов. Они могут подавлять активность надпочечников лишь при использовании в высоких дозах (более 1000 мкг в сутки).
Фармакологические эффекты иГКС:
- торможение синтеза медиаторов воспаления;
- подавление гиперреактивности бронхов, то есть снижение их чувствительности к аллергену;
- восстановление чувствительности β2-адренорецепторов к β2-агонистам (бронхолитикам);
- уменьшение отека и выработки слизи бронхиальными железами.
Чем выше доза препарата, тем выраженнее его противовоспалительное действие. Поэтому лечение начинают со средних и высоких доз. После улучшения состояния больного и положительных изменений функции внешнего дыхания доза иГКС может быть уменьшена, но полностью эти препараты не отменяют.
Такие побочные эффекты иГКС, как кандидозный стоматит, кашель, изменение голоса, неопасны, но неприятны для пациента. Избежать их можно, применяя для ингаляции спейсер и прополаскивая рот после каждого введения препарата чистой водой или слабым раствором пищевой соды.
Беклометазон входит в состав следующих препаратов, большинство из которых представляют собой аэрозольные ингаляторы:
- Беклазон Эко;
- Беклазон Эко легкое дыхание;
- Беклометазон;
- Беклометазон ДС;
- Беклометазон Аэронатив;
- Беклоспир;
- Кленил;
- Кленил УДВ – суспензия для ингаляций в ампулах.
Нежелательные явления – хрипота, оральный кандидоз, першение в горле, очень редко –спазм бронхов. Отмечаются и аллергические реакции (сыпь, зуд, отек лица). Крайне редко, при использовании в больших дозах, возникают системные эффекты: подавление активности надпочечников, повышение хрупкости костей, у детей – задержка роста.
Беклометазон противопоказан в следующих ситуациях:
- тяжелый приступ астмы, требующий лечения в отделении реанимации;
- туберкулез;
- 1 триместр беременности и лактация.
Единственная форма, предназначенная для ингаляций через компрессорный небулайзер – Кленил УДВ.
Флутиказона пропионат – действующее вещество препарата Фликсотид. Препарат показан для базисной терапии начиная с возраста больных 1 год. Таким маленьким детям лекарство вводится с помощью спейсера с лицевой маской (например, «Бэбихалер»).
Препарат противопоказан при остром приступе астмы, непереносимости, детям до 1 года. Исследования, доказавшие безопасность использования его при беременности и лактации, отсутствуют.
Всемирная организация здравоохранения рекомендовала писать название этого вещества через букву «з» – будезонид. Оно входит в состав препарата для базисной терапии астмы Будесонид Изихейлер. Особенностью этого средства является порошкообразная форма. Считается, что его можно использовать у детей и беременных женщин, если риск осложнений меньше пользы препарата. Противопоказаниями служат лишь повышенная чувствительность к будесониду и лактация.
Дозировку определяет врач в зависимости от возраста пациента и тяжести заболевания.
Преимущества порошкового ингалятора перед аэрозолем заключаются в отсутствии в его составе газов, а также более легком применении и, следовательно, лучшей доставке лекарства в дыхательные пути. После автоматического отмеривания необходимого количества порошка пациенту нужно только поместить мундштук ингалятора в рот и глубоко вдохнуть. При этом даже при нарушении функции дыхания вещество достигнет бронхов.
Флунизолид – действующее вещество препарата Ингакорт. Побочные эффекты, противопоказания те же, что и у других иГКС.
Эти препараты укрепляют (стабилизируют) мембрану тучных клеток – источников медиаторов воспаления. Тучные клетки выбрасывают эти вещества в окружающие ткани при контакте с аллергенами. Выделенные медиаторы воспаления увеличивают проницаемость сосудистых стенок, вызывают миграцию в очаг воспаления других клеток, повреждают окружающие клетки.
Если кромоны назначены до контакта с аллергеном, они препятствуют выбросу медиаторов воспаления и угнетают аллергическую реакцию. Однако их противовоспалительный эффект значительно ниже, чем у иГКС. С другой стороны, и нежелательных явлений у них практически нет. Поэтому они используются в лечении бронхиальной астмы у детей и подростков. У взрослых кромоны иногда хорошо помогают контролировать легкую атопическую астму. Для достижения эффекта их нужно принимать не менее 3 месяцев.
Из этой группы самым распространенным средством является Тайлед Минт, содержащий недокромил натрия. Это дозированный аэрозоль для ингаляций. Он подавляет воспаление и аллергические реакции в бронхах, уменьшает выраженность ночных симптомов и потребность в препаратах «неотложной помощи».
Можно дополнительно принять лекарство перед контактом с аллергеном, физической нагрузкой или выходом на холод. Добавление Тайледа к терапии иГКС во многих случаях помогает снизить дозировку последних.
Неудобство при использовании Тайледа – необходимость регулярного ухода и очищения мундштука, мытья и просушивания его.
Побочные эффекты возникают редко:
- раздражение зева и полости рта;
- сухость во рту;
- охриплость голоса;
- кашель и насморк;
- парадоксальный бронхоспазм;
- головная боль и головокружение;
- тошнота, рвота, боль в животе.
Противопоказания – возраст младше 2 лет, 1 триместр беременности, лактация.
Препарат следует принимать регулярно, каждый день, даже при отсутствии симптомов болезни. Отмену осуществляют постепенно, в течение недели. Если средство вызывает кашель, перед ингаляцией можно воспользоваться бронхолитиками, а после нее выпить воды.
Это довольно новая группа средств, применяемых для лечения астмы. Они блокируют действие лейкотриенов – веществ, образующихся при распаде арахидоновой кислоты в ходе воспалительной реакции. Тем самым они ослабляют воспаление, подавляют гиперреактивность бронхов, улучшают показатели внешнего дыхания.
Эти препараты находят свою нишу в терапии астмы, поскольку они особенно эффективны в следующих ситуациях:
- астма у детей;
- аспириновая астма;
- астма физического усилия;
- преобладание ночных приступов;
- отказ пациента от лечения иГКС;
- недостаточный контроль болезни с помощью иГКС (дополнительно к ним);
- трудности при использовании ингаляторов;
- сочетание астмы и аллергического ринита.
Преимуществом антагонистов лейкотриеновых рецепторов является их форма в виде таблеток. Часто используется зафирлукаст (Аколат).
- тошнота, рвота, боль в животе;
- поражение печени (редко);
- боль в мышцах и суставах (редко);
- аллергические реакции (редко);
- бессонница и головная боль;
- нарушение свертывания крови (редко);
- слабость.
Самые частые побочные эффекты – головная боль и тошнота – выражены слабо и не требуют отмены препарата.
Противопоказания:
- возраст до 7 лет;
- болезни печени;
- лактация.
Безопасность применения Аколата во время беременности не доказана.
Еще одно действующее вещество из класса антагонистов лейкотриеновых рецепторов – монтелукаст, входит в состав как оригинального препарата, так и дженериков: монакс, монкаста, монлер, монтелар, монтеласт, симплаер, синглон, сингулекс, сингуляр, экталуст. Эти лекарства принимают 1 раз в сутки вечером. Их можно использовать с 6 лет. Существуют не только обычные, но и жевательные таблетки.
Противопоказания: возраст до 6 лет, фенилкетонурия, индивидуальная непереносимость.
Новый шаг в базисной терапии бронхиальной астмы – создание и применение комбинаций, обладающих противовоспалительным и длительным брохнодилатирующим эффектами, а именно, сочетаний иГКС и длительно действующих β2-агонистов.
В этих лекарствах каждый из компонентов усиливает действие другого, в результате противовоспалительный эффект иГКС становится более выраженным, чем при монотерапии гормоном в той же дозе. Поэтому применение комбинированных средств – альтернатива увеличению дозы иГКС при их недостаточной эффективности. Оно облегчает течение астмы, снижает потребность в препаратах «неотложной помощи», эффективнее предупреждает обострения заболевания по сравнению с монотерапией иГКС. Эти средства не предназначены для купирования приступа, их необходимо принимать ежедневно вне зависимости от наличия симптомов астмы. Отменять их можно только постепенно.
Применяются два препарата: серетид и симбикорт.
Серетид выпускается в виде дозированного аэрозоля для ингаляций и порошкового ингалятора (Серетид Мультидиск). Он содержит флутиказон и салметерол.
Показания к применению:
- стартовая терапия бронхиальной астмы при наличии показаний к назначению иГКС;
- астма, хорошо контролируемая с помощью иГКС и β2-агонистов длительного действия, вводимых отдельно друг от друга;
- астма, недостаточно хорошо контролируемая с помощью только иГКС.
Побочные эффекты, встречающиеся чаще, чем у одного пациента из 1000:
- кандидоз слизистой оболочки полости рта;
- кожные аллергические проявления;
- катаракта;
- повышение уровня сахара в крови;
- нарушение сна, головная боль, мышечная дрожь;
- учащенное сердцебиение;
- охриплость голоса, кашель, раздражение глотки;
- появление кровоподтеков на коже;
- боль в мышцах и суставах.
Серетид противопоказан детям младше 4 лет и людям, не переносящим компоненты лекарства. Четких данных о безопасности применения препарата при беременности и лактации нет.
Серетид мультидиск удобнее в использовании, чем обычный карманный ингалятор при астме.
Симбикорт Турбухалер – дозированный порошок для ингаляций, содержащий будесонид и формотерол. В отличие от Серетида, препарат не используется в качестве стартовой терапии, зато его можно применять для купирования приступов. Преимущество этого препарата – большие возможности в подборе оптимальной дозировки, обеспечивающей контроль астмы.
Взрослым назначают от 1 до 8 ингаляций в день, подбирая наименьшую эффективную дозу, вплоть до однократного приема в сутки. Детям Симбикорт Турбухалер можно использовать с 6 лет. Побочные эффекты и противопоказания те же, что и у Серетида.
Применение комбинированных препаратов оправдано во всех случаях астмы, требующих назначения иГКС. Удобство использования, быстрый и выраженный эффект улучшают приверженность пациентов лечению, обеспечивают лучший контроль над симптомами заболевания, дают больным уверенность в возможности хорошего качества жизни при бронхиальной астме.
Посмотрите видео о том, как пользоваться спейсером для ингаляций:
источник