Бронхиальная астма (БА) – распространенная патология дыхательных путей. Она встречается у детей и взрослых. Какие признаки и особенности этого заболевания?
БА – это болезнь, которая характеризуется длительным течением. В основе ее лежит гиперреактивность бронхов и хронический воспалительный процесс в дыхательных путях. Воспаление при бронхиальной астме в большинстве случаев персистирующее, то есть постоянное. Без лечения болезнь прогрессирует, состояние больного постепенно ухудшается.
Основные симптомы патологии:
- Приступы удушья (именно они позволяют заподозрить бронхиальную астму).
- Свистящие хрипы в легких, которые ощущаются самим больным и нередко слышны на расстоянии.
- Затрудненный выдох.
- Сухой, малопродуктивный кашель.
При аускультации (прослушивании) легких определяются сухие хрипы во всех или в некоторых отделах, дыхание пациента свистящее. Выдох становится длиннее вдоха, что типично для бронхоспазма – сужения бронхов, из-за которого воздуху сложно проходить по дыхательным путям.
Также выделяют особую, атипичную форму БА. Ее основная характеристика – навязчивый сухой кашель, который чаще отмечается по ночам.
Такой вариант называется кашлевым, и нередко пациенту устанавливают диагноз хронического бронхита или аллергии. Стандартное лечение при этом не приносит улучшения, болезнь прогрессирует. Приступы удушья при кашлевой бронхиальной астме встречаются редко.
Воспаление при астме обусловлено рядом иммунохимических и патофизиологических процессов. Когда в организм пациента поступает аллерген, он взаимодействует с защитными антителами, расположенными на поверхности определенных клеток. В результате реакции высвобождается большое количество гистамина и медиаторов воспаления. Эти вещества провоцируют спазм бронхов, обильное выделение секрета, отек стенок дыхательных путей. Все это проявления воспалительного процесса.
Выделяют следующие формы бронхиальной астмы:
- Интермиттирующую (когда приступы возникают редко).
- Персистирующую – при хроническом воспалении в бронхах. Различают три степени болезни – легкую, среднюю и тяжелую.
При интермиттирующей форме обычно пользуются симптоматическими средствами – ингаляторами, содержащими бронхорасширяющее вещество. Лекарство позволяет быстро купировать бронхоспазм, улучшить состояние пациента, приостановить воспалительный процесс. Более тяжелые формы астмы требуют назначения постоянной противовоспалительной терапии. Это следующие группы препаратов:
Мембраностабилизирующие препараты при БА применяются в качестве противовоспалительных средств. Они не расширяют бронхи и не устраняют бронхоспазм, но благодаря способности предотвращать воспаление используются как профилактическая терапия.
Мембраностабилизирующие препараты наиболее часто назначают при инфекционно-аллергической БА и астме физического усилия у молодых пациентов. Пик их действия разворачивается через 10–14 дней после начала применения. Терапия длительная – не менее четырех месяцев.
К таким лекарствам относят:
- Кромогликат натрия (Интал, Кромолин).
- Недокромил натрия.
- Кетотифен.
- Антагонисты кальция.
Препараты эффективно купируют аллергическое воспаление, при профилактическом приеме предупреждают обострение астмы.
Кортикостероиды используют при персистирующей форме бронхиальной астмы различной степени тяжести. Постоянный прием предупреждает приступы удушья и кашель.
Лечение при этом заболевание ступенчатое. Вначале с противовоспалительной целью назначают ингаляционные препараты:
При прогрессировании болезни или недостаточном контроле симптомов БА пульмонологи рекомендуют пероральный прием глюкокортикоидов. Обычно это препараты на основе преднизолона. У таких лекарств высокий риск побочных эффектов, чаще всего встречаются следующие:
- Набор веса.
- Развитие стероидного диабета.
- Остеопороз.
- Язвенная болезнь.
- Угнетение иммунитета, низкая сопротивляемость инфекциям.
После нормализации состояния пациента системные глюкокортикоиды отменяют, оставляя их только в ингаляционной форме.
Воспаление при бронхиальной астме носит длительный, хронический характер. Для него типичны периодические обострения патологического процесса. Ежедневное применение противовоспалительных средств позволяет избежать приступов удушья и прогрессирования патологии.
источник
Что такое бронхиальная астма? Причины возникновения, диагностику и методы лечения разберем в статье доктора Сергеева А. Л., аллерголога со стажем в 10 лет.
Бронхиальная астма (БА) — заболевание, характерным проявлением которого является хроническое воспаление дыхательных путей, респираторные симптомы (свистящие хрипы, одышка, заложенность в груди и кашель), которые варьируют по времени и интенсивности и проявляются вместе с вариабельной обструкцией дыхательных путей. [1]
БА занимает лидирующую позицию по распространенности среди населения. Если верить статистике, за 15 лет зафиксировано удвоение количества заболевших этой патологией.
По оценкам ВОЗ, сегодня БА болеет примерно 235 млн человек, а к 2025 году прогнозируется увеличение до 400 млн человек в мире. [1] Так, в исследованиях 3 фазы (ISSAC) также выявлен рост мировой заболеваемости БА у детей в возрасте 6-7 лет (11,1-11,6%), среди подростков 13-14 лет (13,2-13,7%). [2] [3]
На появление и развитие БА влияет ряд причин.
Внутренние причины:
1. пол (в раннем детстве преимущественно болеют мальчики, после 12 лет девочки);
2. наследственная склонность к атопии;
3. наследственная склонность к гиперреактивности бронхов;
Внешние условия:
1. аллергены:
- неинфекционные аллергены: бытовые, пыльцевые, эпидермальные; грибковые аллергены;
- инфекционные аллергены (вирусные, бактериальные);
2. инфекции дыхательных путей. [4]
Характерные симптомы БА, на которые жалуются большинство больных, включают:
- кашель и тяжесть в груди;
- экспираторная одышка;
- свистящее дыхание.
Проявления БА изменчивы по своей тяжести, частоте появления и зависят от контакта с различными аллергенами и другими триггерными факторами. Зависят они и от подобранного противоастматического лечения, количества и тяжести сопутствующих заболеваний. Чаще всего симптомы БА беспокоят в ночное время или в ранние утренние часы, а также после физических усилий, что приводит к снижению физической активности больных. Воспалительные изменения в бронхиальном дереве и гиперреактивность дыхательных путей выступают основными патофизиологическими признаками БА. [5]
Механизмы, вызывающие основные симптомы БА [5]
| Симптом | Механизм |
|---|---|
| Кашель | Раздражение рецепторов бронхов, сокращение гладкой мускулатуры бронхов |
| Свистящее дыхание | Бронхообструкция |
| Заложенность в груди | Констрикция мелких дыхательных путей, воздушные ловушки |
| Одышка | Стимулированная работа дыхания |
| Ночные симптомы | Воспалительный процесс, гиперреактивность бронхов |
Патогенез бронхиальной астмы можно наглядно представить в виде схемы:
Сегодня есть огромное количество классификаций БА. Ниже представлены основные, они помогают в понимании причин и необходимы для статистики. Кроме того, приведен современный подход в рассмотрении проблемы астмы, как выделение фенотипов астмы. [1] [6]
В России используется следующая классификация БА:
Классификация БА (МКБ-10)
| J45, J45.0 Астма с преобладанием аллергического компонента |
| аллергическая экзогенная |
| атопическая |
| Бронхит аллергический без доп. уточнений |
| Ринит аллергический с астмой |
| Сенная лихорадка с астмой |
| J45.1 Астма неаллергическая |
| идиосинкратическая |
| эндогенная неаллергическая |
| J45.8 Астма сочетанная |
| ассоциация с состояниями, упомянутыми в J45.0, J45.1 |
| J45.9 Астма без уточнения |
| астма поздно начавшаяся |
| астматический бронхит без доп. уточнений |
| J46 Астматический статус |
| астма тяжелая острая |
Приоритетное внимание сейчас уделяется персонализированной медицине, которая на данный момент не имеет возможности создания индивидуального лекарственного препарата и способов обследования или предупреждения развития заболевания для конкретного больного, но предложено выделять отдельные категории. Эти подгруппы больных называют фенотипами БА, характеризующимися особенностями в причинах, развитии, методах обследования и терапии. [1] [8]
На данный момент существуют следующие фенотипические формы БА:
- Аллергическая БА. Этот тип не представляет сложности в диагностике — дебют заболевания выпадает на детский возраст, связан с отягощенным аллергологическим анамнезом. Как правило, у родственников также имеются респираторные или кожные проявления аллергии. У людей с этой разновидностью БА зафиксировано иммунное воспаление в бронхиальном дереве. Эффективно лечение больных этим типом БА местными кортикостероидами ( ГКС).
- Неаллергическая БА. Этим типом БА болеют преимущественно взрослые, в анамнезе нет аллергопатологии, наследственность по аллергии не отягощена. Характер воспалительных изменений в бронхах этой категории бывает нейтрофильно-эозинофильным, малогранулоцитарным или сочетать эти формы. ИГКС плохо работают в лечении этого типа БА.
- Астма с постоянной констрикцией дыхательных путей. Есть такая группа пациентов, у которых начинаются необратимые изменения в бронхах, как правило, это люди с неконтролируемыми симтомами БА. Изменения в бронхиальном дереве характеризуются перестройкой стенки бронхов. Терапия данных пациентов сложна и требует пристального внимания.
- Астма с запоздалым началом. Большинство больных, в основном женского пола, заболевают астмой в солидных годах. Эти категории больных требуют назначения повышенных концентраций ИГКС или становятся почти резистентными к базовой терапии.
- Астма в сочетании с лишним весом. Этот тип учитывает, что категория людей с превышением веса и БА страдают более тяжелыми приступами удушья и кашлем, постоянно бывает одышка, а изменения в бронхах характеризуются умеренным аллергическим воспалением. Лечение данных пациентов начинается с коррекции эндокринологических отклонений и диетотерапии.
Если вовремя не поставить диагноз бронхиальной астмы и не подобрать терапию, которая позволит контролировать течение болезни, могут развиться осложнения:
- легочное сердце, вплоть до острой сердечной недостаточности;
- эмфизема и пневмосклероз легких, дыхательная недостаточность;
- ателектаз легких;
- интерстициальная, подкожная эмфизема;
- спонтанный пневмоторакс;
- эндокринные расстройства;
- неврологические расстройства.
Бронхиальная астма представляет собой клинический диагноз, который устанавливает врач, учитывая жалобы, анамнестические особенности пациента, функциональные методы диагностики с учетом степени обратимости обструкции бронхов, специального обследования на наличие аллергопатологии и дифференциальной диагностики с прочими болезнями со схожими жалобами. Дебют развития заболевания чаще всего происходит в возрасте от 6 лет, реже после 12 лет. Но появление возможно и в более позднем возрасте. [9] Пациенты жалуются на эпизоды затрудненного дыхания ночью, в предутренние часы или связывают жалобы с эмоциональной, а иногда и физической перегрузкой. Эти симптомы сочетаются с затруднением дыхания, с нарушениями выдоха, «свистами» в груди, рецидивирующим кашлем с небольшим количеством мокроты. Эти симптомы могут купироваться самостоятельно или с использованием лекарственных бронхорасширяющих препаратов. Необходимо связать появления признаков БА после взаимодействия с аллергенными веществами, сезонность появления симптомов, связь с клиническими признаками насморка, присутствие в анамнезе атопических заболеваний или астматических проблем.
При подозрении на диагноз БА следует задать вопросы:
- Беспокоят ли вас приступы похрипывания в легких?
- Бывает ли покашливание в ночное время?
- Как вы переносите физическую нагрузку?
- Беспокоят ли вас тяжесть за грудиной, покашливание после пребывания в запыленных помещениях, контакта с шерстью животных, в весенне-летний период?
- Заметили ли вы, что чаще болеете дольше двух недель, и заболевание часто сопровождается кашлем и одышкой?
Специфические методы постановки диагноза
1. Оценка функции работы легких и степени возвратимости бронхиальной констрикции
- Спирометрия — это основной и простой метод исследования тяжести и возвратимости обструкции бронхов, применяемый также для последующей оценки течения БА. При проведении ФВД можно выявить тип изменений бронхиального дыхания (обструктивный, рестриктивный, смешанный), оценить тяжесть состояния. Для точной диагностики возвратимости бронхиальной констрикции можно применить пробу с бронхорасширяющими препаратами. Общепринятым положительным тестом считается прирост ОФВ1≥12%. Применяют следующие виды бронходилататоров: β2-агонисты быстрого эффекта (сальбутамол, фенотерол, тербуталин) с контролем ответа в течение 14 минут. Положительный тест свидетельствует об обратимости значений нарушений при БА. [9]
- Пикфлоуметрия. Часто применяется измерение пиковой скорости выдоха с помощью специального простого аппарата — пикфлоуметра. Необходимо объяснить больным, как измерять ПСВ в утренние часы (до пользования лекарственными препаратами); в этом случае измеряем самое минимальное значение ПСВ. Измерение ПСВ необходимо сделать и поздним вечером, это будет самый высокий уровень ПСВ. Изменчивость в течение суток ПСВ называют амплитудой ПСВ. Фиксирование ПСВ следует проводить около 2-3 недель. Данное исследование оценивает ПСВ в домашних и рабочих условиях, что позволяет определить, как влияют факторы внешней обстановки на самочувствие пациента (аллергены, профессиональные факторы, физическая нагрузка, стрессы и другие триггеры). [10]
- Определение гиперреактивности бронхов. Присутствие гиперреактивности бронхиального дерева считается важным критерием для постановки диагноза БА. Самым используемым методом исследования гипервосприимчивости бронхов на данный момент является бронхоконстрикторный тест с биологически активными веществами (метахолином, гистамином), а также физической нагрузкой. Оценка показателей исследования оценивается по изменениям ОФВ1. При уменьшении показателей ОВФ1 более чем на 20% (от первоначальных цифр) тест можно считать положительным. [8]
2. Аллергообследование. Подразумевает проведение аллергопроб на коже, тестов-провокаторов с некоторыми видами аллергенов, лабораторного исследования для выявления специфических IgE-антител. Наиболее распространенными являются кожные пробы, так как это простые методы по технике выполнения, достоверно точные и безопасные для пациентов.
2.1. Существуют следующие виды кожных аллергопроб по технике выполнения:
- скарификационные аллергопробы;
- пробы уколом (prick-test);
- внутрикожные пробы;
- аппликационные пробы
Чтобы проводить кожные пробы, необходимы данные из истории болезни пациента, свидетельствующие за однозначную связь жалоб и контакта с тем аллергеном или их группой в патогенезе болезни, IgE-зависимый тип аллергической реакции.
Кожное тестирование не проводится в случаях:
- обострения аллергического заболевания;
- острых вирусных или бактериальных заболеваний (ОРВИ, назофарингиты, бронхиты и др.);
- тяжелой формы астмы, ее неконтролируемого течения (ОФВ1 [10]
2.2. Провокационный ингаляционный тест. Эксперты Респираторного Общества из Европы рекомендуют проводить данное исследование. Перед исследованием проводят спирометрию, и если уровень ОФВ1 не снижается ниже отметки 70% от нормы, пациент допускается до провокации. Используют небулайзер, с помощью которого можно струей выдавать определенные дозы аллергена, и пациент делает несколько ингаляций с определенными разведениями аллергенов под постоянным контролем врача-аллерголога. После каждой ингаляции оцениваются результаты через 10 мин трижды. Тест расценивается как положительный при уменьшении ОФВ1 на 20% и больше от начальных показателей.
2.3. Методы лабораторной диагностики. Диагностика в лаборатории выступает неосновным методом. Проводится, если необходимо еще одно исследование для подтверждения диагноза. Основными показаниями для назначения лабораторной диагностики являются:
- возраст до 3-х лет;
- в анамнезе тяжелые аллергические реакции на кожное обследование;
- основное заболевание протекает тяжело, практически без периодов ремиссии;
- дифференциальная диагностика между IgE-опосредованными и не-IgE-опосредованными типами аллергических реакций;
- обострение кожных заболеваний или особенности строения кожи;
- требуется постоянный прием антигистаминных препаратов и глюкокортикостероидов;
- поливалентная аллергия;
- при проведении кожного тестирования получают ложные результаты;
- отказ больного от кожных проб;
- результаты кожных проб не совпадают с клиническими данными.
В лабораториях применяют следующие методы определения общего и специфического IgE — радиоизотопный, хемилюминисцентный и иммуноферментный анализы.
Самый новый подход к диагностике аллергических заболеваний на данный момент — это молекулярное аллергообследование. Оно помогает более точно поставить диагноз, рассчитать прогноз течения болезни. Для диагностики важно учитывать следующие нюансы:
- отличие истинной сенсибилизации и перекрестных реакций у больных с полиаллергией (когда имеется широкий спектр сенсибилизации);
- снижение риска тяжелых системных реакций при проведении аллергообследования, что улучшает приверженность пациентов;
- точное определение подтипов аллергенов для проведения аллерген-специфической иммунотерапии (АСИТ);
- наиболее распространена технология чипов Immuna Solid phase Allergen Chip (ISAC). Это самая полноценная платформа, которая включает в себя более 100 аллергенных молекул в одном исследовании.
Сегодня, к сожалению, современная медицина не может вылечить больного от бронхиальной астмы, однако все усилия сводятся к созданию терапии с сохранением качества жизни пациента. В идеале при контролируемой БА должны отсутствовать симптомы заболевания, сохраняться нормальными показатели спирометрии, отсутствовать признаки патологических изменений в нижних отделах легких. [1]
Европейскими рекомендациями предложен ступенчатый подход к лечению:
Фармакотерапию БА можно разделить на 2 группы:
- Препараты ситуационного использования
- Препараты постоянного использования
Препараты для купирования приступов следующие:
- коротко-действующие β-адреномиметики;
- антихолинергические препараты;
- комбинированные препараты;
- теофиллин.
К препаратам для поддерживающей терапии относят:
- ингаляционные и системные глюкокортикостероиды;
- комбинации длительно действующих β2-агонистов и ГКС;
- теофиллины с длительным действием;
- антилейкотриеновые препараты;
- антитела к имммуноглобулину Е.
Для терапии БА важны как лекарственные препараты, так и способы введения данных веществ в организм и дыхательные пути. Препараты могут назначаться внутрь per os, парентерально, ингаляционно.
Выделяют следующие группы доставки лекарственных препаратов через дыхательные пути:
- аэрозольные ингаляторы;
- порошковые ингаляторы;
- небулайзеры.
Самым современным и исследованным методом лечения аллергической БА с подтвержденной эффективностью является АСИТ (аллерген-специфическая иммунотерапия). АСИТ на данный момент является единственным способом терапии, который меняет развитие болезни, действуя на механизмы патогенеза астмы. Если вовремя провести АСИТ, данное лечение способно приостановить переход аллергического ринита в астму, а также пресечь переход легкой формы в более тяжелую. А также преимущества АСИТ — это возможность не дать появиться новым сенсибилизациям.
АСИТ при БА проводится пациентам с:
- легкой или средней тяжести формой заболевания (цифры ОФВ1 должны быть не менее 70% от нормы);
- если симптомы астмы не полностью контролируются гипоаллергенным бытом и лекарственной терапией;
- если у пациента имеются риноконъюнктивальные симптомы;
- если пациент отказывается от постоянной формакотерапии;
- если при проведении фармакотерапии возникают нежелательные эффекты, которые мешают пациенту.
Сегодня мы можем предложить пациентам следующие виды АСИТ:
- инъекционное введение аллергенов
- сублингвальное введение аллергенов
В современных условиях нет доказательств, что экологические, климатические факторы, нарушения питания могут ухудшать течение БА, и устранение этих триггеров поможет снизить тяжесть заболевания и уменьшить объем фармакотерапии. Требуется проведение дальнейших клинических наблюдений в этом ключе. [7]
Выделяют первичную профилактику. Она включает:
- элиминацию аллергенов во время беременности и в первые годы жизни ребенка (гипоаллергенный быт и гипоаллергенная диета);
- кормление грудью;
- молочные смеси;
- пищевые добавки во время беременности (существует несколько гипотез протективного эффекта рыбьего жира, селена, витамина Е);
- отказ от курения во время беременности.
Вторичная профилактика включает:
- избегать поллютантов (повышение концентраций озона, окислов озона, взвесей частиц, аэрозолей кислот);
- борьба с клещами домашней пыли;
- не заводить домашних животных;
- отказ от курения в семье.
источник
Бронхиальная астма – это хроническое неинфекционное заболевание дыхательных путей воспалительного характера. Приступ бронхиальной астмы часто развивается после предвестников и характеризуется коротким резким вдохом и шумным длительным выдохом. Обычно он сопровождается кашлем с вязкой мокротой и громкими свистящими хрипами. Методы диагностики включают оценку данных спирометрии, пикфлоуметрии, аллергопроб, клинических и иммунологических анализов крови. В лечении используются аэрозольные бета-адреномиметики, м-холинолитики, АСИТ, при тяжелых формах заболевания применяются глюкокортикостероиды.
За последние два десятка лет заболеваемость бронхиальной астмой (БА) выросла, и на сегодняшний день в мире около 300 миллионов астматиков. Это одно из самых распространенных хронических заболеваний, которому подверженные все люди, вне зависимости от пола и возраста. Смертность среди больных бронхиальной астмой достаточно высока. Тот факт, что в последние двадцать лет заболеваемость бронхиальной астмой у детей постоянно растет, делает бронхиальную астму не просто болезнью, а социальной проблемой, на борьбу с которой направляется максимум сил. Несмотря на сложность, бронхиальная астма хорошо поддается лечению, благодаря которому можно добиться стойкой и длительной ремиссии. Постоянный контроль над своим состоянием позволяет пациентам полностью предотвратить наступление приступов удушья, снизить или исключить прием препаратов для купирования приступов, а так же вести активный образ жизни. Это помогает поддержать функции легких и полностью исключить риск осложнений.
Наиболее опасными провоцирующими факторами для развития бронхиальной астмы являются экзогенные аллергены, лабораторные тесты на которые подтверждают высокий уровень чувствительности у больных БА и у лиц, которые входят в группу риска. Самыми распространенными аллергенами являются бытовые аллергены – это домашняя и книжная пыль, корм для аквариумных рыбок и перхоть животных, аллергены растительного происхождения и пищевые аллергены, которые еще называют нутритивными. У 20-40% больных бронхиальной астмой выявляется сходная реакция на лекарственные препараты, а у 2% болезнь получена вследствие работы на вредном производстве или же, например, в парфюмерных магазинах.
Инфекционные факторы тоже являются важным звеном в этиопатогенезе бронхиальной астмы, так как микроорганизмы, продукты их жизнедеятельности могут выступать в качестве аллергенов, вызывая сенсибилизацию организма. Кроме того, постоянный контакт с инфекцией поддерживает воспалительный процесс бронхиального дерева в активной фазе, что повышает чувствительность организма к экзогенным аллергенам. Так называемые гаптенные аллергены, то есть аллергены небелковой структуры, попадая в организм человека и связываясь его белками так же провоцируют аллергические приступы и увеличивают вероятность возникновения БА. Такие факторы, как переохлаждение, отягощенная наследственность и стрессовые состояния тоже занимают одно из важных мест в этиологии бронхиальной астмы.
Хронические воспалительные процессы в органах дыхания ведут к их гиперактивности, в результате которой при контакте с аллергенами или раздражителями, мгновенно развивается обструкция бронхов, что ограничивает скорость потока воздуха и вызывает удушье. Приступы удушья наблюдаются с разной периодичностью, но даже в стадии ремиссии воспалительный процесс в дыхательных путях сохраняется. В основе нарушения проходимости потока воздуха, при бронхиальной астме лежат следующие компоненты: обструкция дыхательных путей из-за спазмов гладкой мускулатуры бронхов или вследствие отека их слизистой оболочки; закупорка бронхов секретом подслизистых желез дыхательных путей из-за их гиперфункции; замещение мышечной ткани бронхов на соединительную при длительном течении заболевания, из-за чего возникают склеротические изменения в стенке бронхов.
В основе изменений бронхов лежит сенсибилизация организма, когда при аллергических реакциях немедленного типа, протекающих в виде анафилаксий, вырабатываются антитела, а при повторной встрече с аллергеном происходит мгновенное высвобождение гистамина, что и приводит к отеку слизистой бронхов и к гиперсекреции желез. Иммунокомплексные аллергические реакции и реакции замедленной чувствительности протекают аналогично, но с менее выраженными симптомами. Повышенное количество ионов кальция в крови человека в последнее время тоже рассматривается как предрасполагающий фактор, так как избыток кальция может провоцировать спазмы, в том числе и спазмы мускулатуры бронхов.
При патологоанатомическом исследовании умерших во время приступа удушья отмечается полная или частичная закупорка бронхов вязкой густой слизью и эмфизематозное расширение легких из-за затрудненного выдоха. Микроскопия тканей чаще всего имеет сходную картину – это утолщенный мышечный слой, гипертрофированные бронхиальные железы, инфильтративные стенки бронхов с десквамацией эпителия.
БА подразделяется по этиологии, тяжести течения, уровню контроля и другим параметрам. По происхождению выделяют аллергическую (в т. ч. профессиональную БА), неаллергическую (в т. ч. аспириновую БА), неуточненную, смешанную бронхиальную астму. По степени тяжести различают следующие формы БА:
- Интермиттирующая (эпизодическая). Симптомы возникают реже одного раза в неделю, обострения редкие и короткие.
- Персистирующая (постоянного течения). Делится на 3 степени:
- легкая — симптомы возникают от 1 раза в неделю до 1 раза в месяц
- средняя — частота приступов ежедневная
- тяжелая — симптомы сохраняются практически постоянно.
В течении астмы выделяют обострения и ремиссию (нестабильную или стабильную). По возможности контроля над пристпуами БА может быть контролируемой, частично контролируемой и неконтролируемой. Полный диагноз пациента с бронхиальной астмой включает в себя все вышеперечисленные характеристики. Например, «Бронхиальная астма неаллергического происхождения, интермиттирующая, контролируемая, в стадии стабильной ремиссии».
Приступ удушья при бронхиальной астме делится на три периода: период предвестников, период разгара и период обратного развития. Период предвестников наиболее выражен у пациентов с инфекционно-аллергической природой БА, он проявляется вазомоторными реакциями со стороны органов носоглотки (обильные водянистые выделения, непрекращающееся чихание). Второй период (он может начаться внезапно) характеризуется ощущением стесненности в грудной клетке, которое не позволяет дышать свободно. Вдох становится резким и коротким, а выдох наоборот продолжительным и шумным. Дыхание сопровождается громкими свистящими хрипами, появляется кашель с вязкой, трудно отхаркиваемой мокротой, что делает дыхание аритмичным.
Во время приступа положение пациента вынужденное, обычно он старается принять сидячее положение с наклоненным вперед корпусом, и найти точку опоры или опирается локтями в колени. Лицо становится одутловатым, а во время выдоха шейные вены набухают. В зависимости от тяжести приступа можно наблюдать участие мышц, которые помогают преодолеть сопротивление на выдохе. В периоде обратного развития начинается постепенное отхождение мокроты, количество хрипов уменьшается, и приступ удушья постепенно угасает.
Проявления, при которых можно заподозрить наличие бронхиальной астмы.
- высокотональные свистящие хрипы при выдохе, особенно у детей.
- повторяющиеся эпизоды свистящих хрипов, затрудненного дыхания, чувства стеснения в грудной клетке и кашель, усиливающийся в ночной время.
- сезонность ухудшений самочувствия со стороны органов дыхания
- наличие экземы, аллергических заболеваний в анамнезе.
- ухудшение или возникновение симптоматики при контакте с аллергенами, приеме препаратов, при контакте с дымом, при резких изменениях температуры окружающей среды, ОРЗ, физических нагрузках и эмоциональных напряжениях.
- частые простудные заболевания «спускающиеся» в нижние отделы дыхательных путей.
- улучшение состояние после приема антигистаминных и противоастматических препаратов.
В зависимости от тяжести и интенсивности приступов удушья бронхиальная астма может осложняться эмфиземой легких и последующим присоединением вторичной сердечно-легочной недостаточности. Передозировка бета-адреностимуляторов или быстрое снижение дозировки глюкокортикостероидов, а так же контакт с массивной дозой аллергена могут привести к возникновению астматического статуса, когда приступы удушья идут один за другим и их практически невозможно купировать. Астматический статус может закончиться летальным исходом.
Диагноз обычно ставится клиницистом-пульмонологом на основании жалоб и наличия характерной симптоматики. Все остальные методы исследования направлены на установление степени тяжести и этиологии заболевания. При перкуссии звук ясный коробочный из-за гипервоздушности легких, подвижность легких резко ограничена, а их границы смещены вниз. При аускультации над легкими прослушивается везикулярное дыхание, ослабленное с удлиненным выдохом и с большим количеством сухих свистящих хрипов. Из-за увеличения легких в объеме, точка абсолютной тупости сердца уменьшается, тоны сердца приглушенные с акцентом второго тона над легочной артерией. Из инструментальных исследований проводится:
- Спирометрия. Спирография помогает оценить степень обструкции бронхов, выяснить вариабельность и обратимость обструкции, а так же подтвердить диагноз. При БА форсированный выдох после ингаляции бронхолитиком за 1 секунду увеличивается на 12% (200мл) и более. Но для получения более точной информации спирометрию следует проводить несколько раз.
- Пикфлоуметрия. Измерение пиковой активности выдоха (ПСВ) позволяет проводить мониторинг состояния пациента, сравнивая показатели с полученными ранее. Увеличение ПСВ после ингаляции бронхолитика на 20% и более от ПСВ до ингаляции четко свидетельствует о наличии бронхиальной астмы.
Дополнительная диагностика включает в себя проведение тестов с аллергенами, ЭКГ, бронхоскопию и рентгенографию легких. Лабораторные исследования крови имеют большое значение в подтверждении аллергической природы бронхиальной астмы, а так же для мониторинга эффективности лечения.
- Анализа крови. Изменения в ОАК — эозинофилия и незначительное повышение СОЭ — определяются только в период обострения. Оценка газового состава крови необходима во время приступа для оценки тяжести ДН. Биохимический анализ крови не является основным методом диагностики, так как изменения носят общий характер и подобные исследования назначаются для мониторинга состояния пациента в период обострения.
- Общий анализ мокроты. При микроскопии в мокроте можно обнаружить большое количество эозинофилов, кристаллы Шарко-Лейдена (блестящие прозрачные кристаллы, образующиеся после разрушения эозинофилов и имеющие форму ромбов или октаэдров), спирали Куршмана (образуются из-за мелких спастических сокращений бронхов и выглядят как слепки прозрачной слизи в форме спиралей). Нейтральные лейкоциты можно обнаружить у пациентов с инфекционно-зависимой бронхиальной астмой в стадии активного воспалительного процесса. Так же отмечено выделение телец Креола во время приступа – это округлые образования, состоящие из эпителиальных клеток.
- Исследование иммунного статуса. При бронхиальной астме количество и активность Т-супрессоров резко снижается, а количество иммуноглобулинов в крови увеличивается. Использование тестов для определения количества иммуноглобулинов Е важно в том случае, если нет возможности провести аллергологические тесты.
Поскольку бронхиальная астма является хроническим заболеванием вне зависимости от частоты приступов, то основополагающим моментом в терапии является исключение контакта с возможными аллергенами, соблюдение элиминационных диет и рациональное трудоустройство. Если же удается выявить аллерген, то специфическая гипосенсибилизирующая терапия помогает снизить реакцию организма на него.
Для купирования приступов удушья применяют бета-адреномиметики в форме аэрозоля, для того чтобы быстро увеличить просвет бронхов и улучшить отток мокроты. Это фенотерола гидробромид, сальбутамол, орципреналин. Доза в каждом случае подбирается индивидуально. Так же хорошо купируют приступы препараты группы м-холинолитиков – аэрозоли ипратропия бромида и его комбинации с фенотеролом.
Ксантиновые производные пользуются среди больных бронхиальной астмой большой популярностью. Они назначаются для предотвращения приступов удушья в виде таблетированных форм пролонгированного действия. В последние несколько лет препараты, которые препятствуют дегрануляции тучных клеток, дают положительный эффект при лечении бронхиальной астмы. Это кетотифен, кромогликат натрия и антагонисты ионов кальция.
При лечении тяжелых форм БА подключают гормональную терапию, в глюкокортикостероидах нуждается почти четверть пациентов, 15-20 мг Преднизолона принимают в утренние часы вместе с антацидными препаратами, которые защищают слизистую желудка. В условиях стационара гормональные препараты могут быть назначены в виде инъекций. Особенность лечения бронхиальной астмы в том, что нужно использовать лекарственные препараты в минимальной эффективной дозе и добиваться еще большего снижения дозировок. Для лучшего отхождения мокроты показаны отхаркивающие и муколитические препараты.
Течение бронхиальной астмы состоит из череды обострений и ремиссий, при своевременном выявлении можно добиться устойчивой и длительной ремиссии, прогноз же зависит в большей степени от того, насколько внимательно пациент относится к своему здоровью и соблюдает предписания врача. Большое значение имеет профилактика бронхиальной астмы, которая заключается в санации очагов хронической инфекции, борьбе с курением, а так же в минимизации контактов с аллергенами. Это особенно важно для людей, которые входят в группу риска или имеют отягощенную наследственность.
источник
активация происходит под влиянием аллергенов, физических, химических, осмотических стимулов.
Находящиеся в гранулах: гистамин, хемотаксические факторы, гепарин, протеазы, супероксиддисмутаза.
Образующиеся в ходе активации: продукты метаболизма арахидоновой кислоты (ПГ D2, цистеиниловые лейкотриены (LT С4,Д4, Е4, тромбоксан А2), ФАТ и др.
Бронхоспазм, стимуляция воспаления, ГРБ.
Эозинофилы: повышение количества и медиаторов в респираторном тракте
гистаминаза, фосфолипаза Д, простагландины, ФАТ, ЛТС4, коллагеназа
Провоспалительное действие: деструкция и десквамация эпителия бронхов, высвобождение факторов роста, цитотокстическое действие на тучные клетки, нервные клетки, бактерии, вирусы, паразиты, грибы; повышение сосудистой проницаемости, повышение ГРБ, участие в ремоделировании дыхательных путей.
Противовоспалительное действие: инактивация медиаторов аллергических реакций: гистамина, лейкотриенов, гепарина, подавление дегрануляции тучных клеток.
Т-имфоциты:увеличение количества; повышение активности Th-2
Цитокины:IL-4, 5, 9, 13; TNF-альфа, GM-CSF
Регулирование процесса эозинофильного воспаления, выработки IgE В-лифоцитами.
Дендритные клетки: активация
Захватывают аллергены с поверхности слизистой бронхов и мигрируют в региональные лимфоузлы; стимулируют превращение недифференцированных Т-лимфоцитов в Th-клетки в лимфоузлах.
Макрофаги: увеличено количество;активируются под действием аллергенов
Медиаторы воспаления и цитокины
Усиление воспалительной реакции
Нейтрофилы:количество повышено в дыхательных путях у больных тяжелой БА и курильщиков
-Участие структурных клеток дыхательных путей в патогенезе БА.
Клетки бронхиального эпителия взаимодействуют с вирусами и поллютантами, продуцируют оксид азота (NO), цитокины, хемокины, вызывая стимуляцию воспаления, вазодилатацию. Гладкомышечные клетки бронхов экспрессируют воспалительные белки. Клетки эндотелия участвуют в миграции клеток воспаления из кровеносного русла в дыхательные пути. Фибробласты и миофибробласты при активации вырабатывают компоненты соединительной ткани — коллагены и протеингликаны, что приводит к ремоделированию дыхательных путей.
-Нервная система дыхательных путей.
Изменение функции нервной системы дыхательных путей характеризуется активацией холинэргических нервов под действием триггеров, высвобождением воспалительных нейропептидов, что приводит к бронхоспазму, гиперсекреции слизи.
Иммунологические механизмы патогенеза БА.
У значительной части больных БА патологические реакции иммунной системы на поступающие из внешней среды аллергены являются одним из основных звеньев патогенеза. Наличие у больного БА I типа аллергических реакций связано с повышением в сыворотке IgE , уровень которого у больных атопической астмой в 8 раз выше, чем у здоровых лиц. В ряде случаев атопическая БА сопровождается повышение IgG 4- антител. Сенсибилизация к аллергенам может произойти в раннем детстве. Антигенпрезентирующие клетки в слизистой бронхов захватывают попавший с вдыхаемым воздухом аллерген и представляют его CD4+ Т-лимфоцитам, которые затем превращаются в клетки фенотипа Th2. Эти клетки секретируют интерлейкины (ИЛ-4, 5, 9, 10, 13), которые, воздействуя на В-лимфоциты, переключают их на выработку специфических антител класса IgE. При атопической БА возможно появление IgE в бронхиальном секрете. Циркулирующие молекулы IgE, связываясь с рецепторами, фиксируются на поверхности клеток – мишеней первого порядка, главными из которых являются тучные клетки соединительной ткани и слизистых и базофилы крови (фаза сенсибилизации аллергической реакции).
При повторном попадании в организм аллергена и взаимодействии его с молекулами IgE, связанными с поверхностью клеток, эти клети – мишени первого порядка активируются с высвобождением БАВ: гистамина, протеаз, лейкотриенов, простагландинов, хемокинов и протеолитических ферментов типа металлопротеиназ (фаза активации аллергической реакции), что стимулирует активацию клеток – мишеней второго порядка, прежде всего эозинофилов и базофилов и приводит к вовлечению их в аллергическую реакцию (эффекторная фаза аллергической реакции). Возникающая бронхообструкция характеризуется бронхоспазмом, отеком стенки бронхов и гиперсекрецией слизи и осуществляется в 2 этапа. Первый — «ранний ответ» протекает с участием предшествующих медиаторов, высвобождающихся при дегрануляции тучных клеток: гистамина, гепарина, интерлейкинов IL- 4, IL- 5,IL-8, IL-9, TNF-альфа и других цитокинов. и характеризуется снижением легочной функции за первые 10-20 минут, восстановление происходит на протяжении нескольких часов.
Характерными признаками атопического механизма БА являются: развитие симптомов БА непосредственно после контакта с аллергеном, немедленная реакция при постановке кожных проб, наличие в сыворотке специфичесикх антител IgE к данному аллергену, эффективность лечения антигистаминными препаратами и инталом, эффект элиминации. Поздний ответ или реакция поздней фазы возникает в течение 48 часов и может продолжаться несколько дней. Она обеспечивается медиаторами тучных клеток, которые синтезируются de novo (медиаторы второй категории), и клетками, привлекаемыми к месту воспаления, прежде всего эозинофилами, а также базофилами, нейтрофилами, лимфоцитами, макрофагами. К числу вновь синтезированных медиаторов тучных клеток относятся медиаторы из клеточных мембран. В результате липооксигеназного пути метаболизма арахидоновой кислоты образуются цистеинил-лейкотриены (LTС4, LT D4, LT Е4), которые устойчивы к действию антигистаминных средств, вызывают длительный бронхоспазм и индуцируют выделение протеаз. Триптаза отщепляет С3а и брадикинин из белков – предшественников, что приводит к сокращению мышц бронхов, повышению сосудистой проницаемости и отеку. Химаза способствует гиперпродукции слизи бокаловидными клетками и слизистыми железами. В результате циклооксигеназного пути метаболизма арахидоновой кислоты образуются простагландины и тромбоксаны, многие из которых также обладают бронхоконстрикторным, вазоконстрикторным действием и усиливают хемотаксис нейтрофилов, эозинофилов, базофилов, моноцитов. Фактор активации тромбоцитов (ФАТ), активирует последние, что сопровождается усилением высвобождения метаболитов арахидоновой кислоты, серотонина, гистамина, вызывает сужение бронхов и вазодилатацию.
Эозинофилы могут связывать IgE. Активация эозинофилов сопровождается высвобождением ФАТ, главного основного белка, катионного белка, которые вызывают повреждение тканей. Активированные нейтрофилы продуцируют БАВ провоспалительного действия: лизосомальные ферменты, лейкотриены, ФАТ. Бронхоспазм в сочетании с отеком слизистой и гиперсекрецией слизи приводит к появлению респираторных симптомов астмы: кашля, одышки, свистящего дыхания. В период поздней фазы формируется кардинальный признак БА –гиперреактивность бронхов.
Аллергические реакции III типа (иммунокомплексные) формируются циркулирующими антителами, в основном IgG, и антигенами (при избытке растворимого антигена). Образующиеся иммунные комплексы (ЦИК) активируют систему комплемента. При связывании ЦИК с Fc-рецепторами тучных клеток, эозинофилов и макрофагов происходит выделение медиаторов воспаления, вызывающих обструкцию бронхов. Характерен «поздний ответ», который развивается через 4-6 часов после контакта с аллергеном, контролируется LTВ4 и ФАТ, сопровождается хемотаксисом эозинофилов. Эозинофилы выделяют основные белки: (МВР-maior basic protein) и эозинофильный катионный протеин (ЭКП), которые оказывают токсическое действие на эпителиальные клетки дыхательных путей. Увеличение числа бокаловидных клеток, гипертрофия слизистых желез, при одновременной гибели реснитчатого эпителия бронхов, приводит к стазу слизи и способствует закупорке бронхов вязким секретом. Вязкая слизь нарушает дренажную функцию бронхов, нарушает мукоцилиарный барьер, снижает местные иммунологические процессы, в частности содержание секреторного IgA, создавая предпосылки к инфекции дыхательных путей. Может наблюдаться пролиферация мышечных клеток и их миграция в подслизистый слой. Характерными для данного механизма патогенеза БА являются следующие признаки: «поздние» кожные реакции с аллергеном, антитела IgG, «позднее» развитие симптомов БА, лечебный эффект глюкокортикостероидов, отсутствие эффекта от интала.
Участие IV типа аллергических реакций (замедленная гиперчувствительность), обусловленой сенсибилизированными лимфоцитами, чаще связывают с аллергизирующим влиянием инфекционных агентов.
У больных БА выявлены функциональные нарушения Т- и В- лимфоцитов. Имеются нарушения дифференцировки и созревания Т-лимфоцитов. С недостаточностью супрессорного действия связано чрезмерное накопление специфических IgE-антител. Имеет место снижение антителобразующей функции В-лимфоцитов на поверхности эпителиальных клеток, сопровождающееся снижением синтеза IgA, обладающего защитными свойствами, предотвращающего адгезию бактериальных клеток , Уувеличивается популяция лимфоцитов, устойчивых к действию кортизола.
Ключевую роль в ранних стадиях воспаления играют молекулы адгезии. Цитокины. высвобождаемые Тh2л, тучными клетками (ИЛ13, ТНФ-а) усиливают экспрессию молекул адгезии на лейкоцитах и эндотелии, включая межклеточную молекулу адгезии –ICAM-1, селектин, молекулу адгезии сосудистой клетки- VCAM-1 и антиген лейкоцитов LEA-1.Все это приводит к усилению адгезии эозинофилов к эндотелию, миграции их через эндотелий и длительному нахождению в тканях легких.В качестве возможного способа лечения БА исследовали в эксперименте на животных применение антагонистов молекул адгезии, например моноклональных антител к ICAM-1,
Неиммунологические механизмы патогенеза БА
Стимуляция первичных эффекторных клеток – тучных и базофилов, может осуществляться неиммунными механизмами. Активация тучных клеток характеризуется изменением пространственной конфигурации рецепторов мембраны и активацией мембранных энзимов. При этом контакт клетки с аллергеном не обязателен. Дегрануляцию может вызвать нарушение адренергических механизмов со снижение цАМФ или повышением цГМФ. Изменение уровня циклических нуклеотидов, в свою очередь связано с уровнем внутриклеточного кальция. На секреторную активность тучных клеток влияет рН околоклеточной среды, воздействие различных метаболитов, кислородных радикалов. Гиперосмолярность стимулирует секрецию БАВ при астме физического усилия.
Стимуляция выделения медиаторов тучных леток может происходить при воздействии компонентов системы комплемента С3а и С5а на соответствующие рецепторы при активации системы комплемента по альтернативному пути. В качестве активаторов могут служить полисахариды бактерий, антигены грибов (плесневых, аспергилл) и компоненты аллергенов домашней пыли. Активация системы комплемента является причиной псевдоаллергических реакций при БА, вызывает независимую от IgE дегрануляцию тучных и других эффекторных клеток, которые секретируют медиаторы воспаления.
В формировании бронхообструктивного синдрома при БА имеет значение нарушение баланса нервных и гуморальных механизмов, участвующих в регуляции тонуса гладкой мускулатуры бронхов, продукции слизи бронхиальными железами, кровотока в сосудах малого круга кровообращения, активности клеточных элементов, расположенных в тканях дыхательных путей и легких.
Гормональные механизмы патогенеза БА
Эндокринные железы участвуют в регуляции бронхомоторного тонуса, действуя на бронхи непосредственно или опосредовано через влияние на иммунную и нервную систему. У некоторых больных дефекты эндокринной системы могут играть ведущую роль в патогенезе, формируя дисгормональный вариант БА.
Кортикостероиды. Физиологические эффекты глюкокортикоидных гормонов обладают протективным действием в отношении БА. Они ослабляют действие бронхоконстрикторных веществ, тормозят синтез антител, нарушая кооперацию Т- и В-лимфоцитов, тормозят высвобождение гистамина, лизосомальных ферментов из нейтрофилов, уменьшая иммунное повреждение, тормозят активность фосфолипазы-2, ограничивая синтез лейкотриенов и ПГF 2 альфа, повышают чувствительность бета-адренергических рецепторов к адреналину, стимулируют синтез сурфактанта. У больных БА глюкокортикоидная недостаточность может иметь надпочечниковое и вненадпочечниковое происхождение. Снижение функции надпочечников может быть связано с аллергическим повреждением, лечением глюкокортикоидными гормонами, гипоксией. Вненадпочечниковая недостаточность может обсловливаться кортизолрезистентностью тканей в связи с уменьшением числа рецепторов к кортизолу, повышенной потребностью в глюкокортикоидах у больных БА и другими причинами. Глюкокортикоидная недостаточность может быть одной из причин развития или обострения БА, при котором основными механизмами обструкции являются отек слизистой оболочки, инфильтрация стенок бронхов эозинофилами, утолщение базальной мембраны, накопление патологического экссудата в просвете бронхов и бронхоспазм.
Нарушение баланса половых гормонов.
Различные изменения гормонального фона у женщин могут влиять на состояние проходимости бронхов. В исследованиях, проведенных в клинике Г.Б. Федосеева (1985) показано, что у 76%женщин, больных БА выявлены дизовариальные расстройства со снижением уровня прогестерона и преобладанием эстрогенов и отмечена связь между выраженностью бронхиальной обструкции и уменьшением содержания прогестерона. Высказывается мнение об ингибирующей роли эстрогенов на активность холинэстеразы, что приводит к накоплению ацетилхолина и повышении вагусных влияний. Одним из предрасполагающих факторов, участвующих в возникновении БА у лиц пожилого возраста, может быть снижение андрогенной и эстрогенной функции половых желез. Отмечено, что может иметься сенсибилизация половыми гормонами, которая подтверждается положительными кожными пробами и повышением титров антител против гормонов
Известно, что тиреотоксикоз способствует развитию и прогрессированию БА. При гипертиреозе нарушается метаболизм кортикостероидов, простагландинов и гистамина, снижена чувствительность бронхов к адреностимуляторам, что в совокупности способствует развитию бронхоспастических реакций.
Нарушение гомеостаза кальция, повышение внутриклеточной концентрации кальция может оказывать влияние на различные механизмы патогенеза БА, прежде всего на формирование ГРБ. Гормонами, регулирующими обмен кальция являются кальцитонин, паратгормон и витамин Д. Для патогенеза БА важно не только антирезорбтивное действие кальциотонина на костную ткань, но и положительные эффекты на воспаление. Он оказывает противовоспалительное, противоотечное, антистрессовое действие, а также стимулирующее влияние на функцию надпочечников с увеличением выработка кортизола, увеличение АКТГ. У больных БА выявлено снижение концентрации кальцитонина, наиболее выраженные у пациентов, длительно принимающих ГКС.
Изменения вегетативной нервной системы при БА.
В регуляции бронхомоторного тонуса участвует симпатическая, парасимпатическая нервная система и нехолин-неадренергическая иннервация. Эффекторные клетки бронхов и легких воспринимают воздействие стимуляторов – адреналина и ацетилхолина соответствующими типами рецепторов. Тучные и другие клетки, продуцирующие БАВ, снабжены рецепторами к адреналину и ацетилхолину, реагируя на раздражение освобождением БАВ. Гладкие мышцы бронхов чувствительны ко многим БАВ – гистамину, серотонину, брадикинину, простагландинам, лейкотриенам (медленно реагирующая субстанция анафилаксии), которые могут оказывать действие как прямое, так и через сенсорные рецепторы раздражения, что сопровождается бронхоконстрикцией. Спазм крупных бронхов стимулируется главным образом рефлекторным механизмом, а спазм периферических отделов бронхиального дерева вызывается непосредственным действием биологически активных веществ на гладкую мускулатуру бронхов.
Адренергические механизмы. В регуляции бронхомоторного тонуса ведущая роль принадлежит бета2-адренергическим рецепторам (Б2-АР). Б2-АР расположены в клетках эпителия, эндотелия, стенках альвеол, гладкой мускулатуре дыхательных путей и в подслизистых железах. Физиологические эффекты Б2- АР заключаются в расслаблении гладких мышц бронхов, увеличении мукоцилиарного клиренса, расширении периферических кровеносных сосудов, снижении освобождения эндогенных спазмогенов (через бета-рецепторы на тучных и других эффекторных клетках), снижении клеточной проницаемости и экссудации плазмы в слизистую дыхательных путей (через Б2-АР эндотелия), торможении пролиферации гладкомышечных клеток дыхательных путей. Противоположным эффектом обладают альфа-адренорецепторы, стиуляция которых сопровождается сокращением гладких мышц бронхов, увеличением освобождения эндогенных спазмогенов, спазмом периферических сосудов. У больных БА выявляется нарушение функции и снижение количества бета-рецепторов. Недостаточность бета-рецепторов может развиться вследствие аллергического воспаления (алергениндуцированная десенситизация), активации фосфолипаз (действие метаболитов арахидоновой кислоты), применения бета 2-агонистов. Недостаточность Б2-АР у больных БА вызывает бронхоспазм, нарушение мукоцилиарного транспорта и развитие дискринии, отек и экссудацию слизистых дыхательных путей, гиперплазию гладкой мускулатуры бронхов и ремоделирование дыхательных путей. При БА отмечается увеличение концентрации адреналина и норадреналина, но одновременно с этим, по мере нарастания тяжести заболевания, снижается чувствительность бронхов к адреналину, формируется адренергический дисбаланс.
Холинергические механизмы. Блуждающий нерв иннервирует бронхиальную мускулатуру, а также сосуды и клетки слизистой оболочки на всем протяжении бронхиального дерева от трахеи до бронхиол диаметром 0,5 мм. Стимуляция блуждающего нерва сопровождается выделением ацетилхолина в окончаниях постганглионарных нервов и ведет к бронхоконстрикции, гиперсекреции бронхиальной слизи. В трахеобронхиальном дереве имеются три типа холинорецепторов: рецепторы растяжения — механорецепторы, физиологический эффект возбуждения выражается в ингибировании вдоха и расслаблении дыхательной мускулатуры, рефлекс развивается только при полном расширении легких и отсутствует при нормальном дыхании; рецепторы раздражения — ирритантные (бронхоадаптирующиеся, рецепторы выдоха), которые стимулируются большим числом эндогенных и экзогенных факторов, раздражение сопровождается бронхоконстрикцией; J-рецепторы – юкстакапиллярные , расположены в интерстиции легких, раздражителем является повышение давления в малом круге кровообращения, рефлекторно происходит констрикция бронхов. Холинорецепторы делятся на мускариновые и никотиновые. Известно пять типов мускариновых рецепторов, различающихся по фармакологической активности. М-рецепторы располагаются на плазматической мембране клеток и передают внутриклеточный сигнал посредством взаимодействия с G-протеином. Считается, что М1-холинорецепторы, расположенные в ганглиях, участвуют в усилении ганглионарной передачи и усиливают холинергический ответ, М2-холинорецепторы, расположенные в окончаниях холинергических нервов ингибируют выброс ацетихолина, М3-холинорецепторы локализуются на эффекторных клетках (гладкомышечных, железистых, эндотелиальных) и вызывают активацию этих клеток.
Баланс между сокращением и расслаблением гладкой мускулатуры зависит от преобладания симпатических или парасимпатических влияний. При БА установлено выраженное преобладание тонуса тонуса парасимпатической нервной системы, выявляются изменения в ирритантных рецепторах, постганглионарных волокнах , угнетается активность холинэстеразы под действием аллергического процесса, что сопровождается накоплением ацетилхолина. Бронхоспастические реакции холинергического типа могут возникать при активации холинергических нервов, расположенных в мышцах неба, гортани, слизистой носа и носовых мышцах. У больных БА существует назобронхиальный рефлекс, который вызывает усиление бронхоспазма при раздражении слизистой носа. Активация холинергических механизмов сопровождается расширением сосудов слизистой оболочки, затруднением носового дыхания. Включение дыхания через рот приводит к раздражению дыхательных путей холодным воздухом, пылью, химическими веществами.
Нехолинергическая неадренергическая система.Наряду с холинергической и адренергической регуляцией, на функцию бронхолегочного аппарата оказывает влияние нехолинергическая неадренергическая система Медиаторами являются нейрогуморальные факторы – пептиды (вазоинтестинальный пептид, вещество Р, кинины и др., продукты метаболизма арахидоновой кислоты, биогенные амины), образующиеся в эндотелии легочных сосудов и эпителии слизистой бронхов. Пептиды неадренергической системы действуют как антагонисты парасимпатической иннервации.
Нервно-психические механизмы патогенеза БА
Для больных БА характерен комплекс психосоматических взаимоотношений астмы и эмоций, который определяется термином «астматический дистресс». Проявления астматического дистресса разнообразны. Это негативные эмоции, связанные с самим заболеванием, с отрицательной реакцией центральной нервной системы на патологические процессы в органах дыхания, с влиянием медикаментозной терапии и различных жизненных ситуаций на течение заболевания. Нервно-психические изменения у больных БА позволили выделить четыре варианта: истероподобный, неврастеноподобный, психастеноподобный, шунтовой.
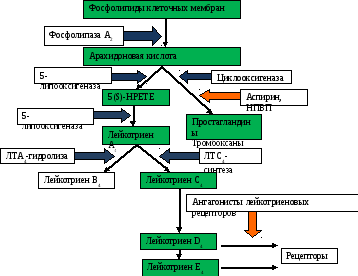
Нарушение метаболизма арахидоновой кислоты
Нарушению метаболизма арахидоновой кислоты отводится основная роль при «аспириновой астме», когда основным причинным фактором являются нестероидные противовоспалительные препараты, в том числе и ацетилсалициловая кислота. Арахидоновая кислота высвобождается из мембран клеток воспаления при их активации. Метаболизм арахидоновой кислоты представляет собой каскад ферментативных реакций. Под действием циклоокигеназы (ЦО) образуются простагландины (ПГ G2. ПГ Н2, ПГ F2-альфа, ПГ Е2, ПГ I2) и тромбоксаны, из которых бронхорасширяющим действием обладают ПГ Е2 и ПГ I2. С помощью системы ферментов 5-липооксигеназы образуются лейкотриены. Первым продуктом липоксигеназного окисления является ЛТА4, который под действием фермента ЛТА4-гидралазы превращается в ЛТ В4, а при помощи фермента ЛТА4-синтазы соединяется с глутатионом с образованием цистеинилового лейкотриена ЛТС4; последний с помощью лямбда-глютамилтрансферазы превращается в ЛТД4, который под действием дипептидаз переходит в ЛТЕ4. Эозинофилы, тучные клетки и альвеолярные макрофаги синтезируют преимущественно ЛТ С4, а нейтрофилы — ЛТ В4. ЛТ С4, Д4, Е4 являются мощными бронхоконстрикторами, превосходят в 100-1000 раз эффект гистамина ( в совокупности они составляют медленнореагирующую субстанцию анафилаксии), увеличивают сосудистую проницаемость, усиливая отек слизистой, вызывают повышенную секрецию слизи бронхиальными железами, привлекают эозинофилы в зону воспаления. ЛТ В4 вызывает хемотаксис лейкоцитов, агрегацию и адгезию их к эндотелию, высвобождение лизосомальных ферментов и супероксидного аниона из нейтрофилов. При применении НПВС, являющихся ингибиторами ЦО, происходит переключением метаболизма арахидоноваой кислоты преимущественно на липоксигеназный путь. При «аспириновой БА» имеется нарушение метаболизма арахидоновой кислоты, который осуществляется преимущественно по липоксигеназному пути, с образованием избытка медиаторов. Не исключается, что повышенная чувствительность ЦО к инактивации является наследственно обусловленной.
Гипререактивность дыхательных путей (ГРБ) и бронхиальная обструкция являются основными синдромами нарушения респираторной функции при БА.
Гиперреактивность дыхательных путей при БА
Гиперреактивность бронхов (ГРБ) — повышение бронхоконстрикторного ответа на широкий спектр экзогенных и эндогенных стимулов, приводящее к вариабельной бронхиальной обструкции и эпизодическому появлению симптомов. Различные стимулы могут вызывать бронхоконстрикцию непосредственно воздействуя на гладкую мускулатуру (метахолин, гистамин), путем высвобождения медиаторов из секретирующих клеток (тучных, эозинофилов, Т-лимфоцитов и пр.) и сенсорных нейронов (брадикинин). Клиническими проявлениями ГРБ являются симптомы бронхоспазма (свистящие хрипы, кашель) при действии различных раздражителей (холод, вдыхание дыма, курение, раздражение при кашле, смехе и эмоциональном возбуждении, охлаждении, физической нагрузке), фармакологических воздействиях (гистамин, метахолин, аденозин, местные анестетики и пр.). Первичная ГРБ обусловлена генетическими особенностями, вторичная — формируется в ходе заболевания.
Механизмы развития ГРБ при БА:
чрезмерное сокращение гладких мышц дыхательных путей за счет увеличения объема и сократимости гладкомышечных клеток;
десинхронизация сокращения гладкой мускулатуры дыхательных путей вследствие воспалительных изменений;
увеличение степени сужения дыхательных путей при спазме гладких мышц бронхов за счет утолщения стенки и измененной геометрии бронхов (отек, структурные изменения);
избыточная бронхоконстрикция в ответ на стимуляцию за счет сенсибилизации чувствительных нервов при воспалении.
Для выявления бронхиальной обструкции определяется ОФВ1 методом спирометрии, ПСВ методом пифлоуметрии, отношение ОФВ1/ФЖЕЛ, в норме составляющее >0,70-0,80. Обострения БА характеризуются активацией воспаления в дыхательных путях, что сопровождается увеличением ГРБ, нарастанием бронхиальной обструкции и симптомов астмы и снижением показателей. Определяющее значение для диагностики и оценки течения БА имеет выявление вариабельности и обратимости бронхиальной обструкции. Вариабельность обструкции — изменение бронхиальной проходимости в течение определенного времени (1 суток, нескольких дней, сезонная), которая проявляется колебаниями ПСВ или ОФВ1 в исследуемый период. Обратимость обструкции – быстрое увеличение ОФВ1 или ПСВ более 15% или на 200 и более мл. от исходного значения через 10-20 минут после ингаляции бронхолитика быстрого действия (В2-агониста или антихолинергического препарата). Положительный тест с бронхолитиками выявляет повышенный базальный тонус гладкой мускулатуры бронхов, как следствием ГРБ при БА . Бронходилатационный тест имеет диагностическое значение только при исходно сниженном ОФВ1 менее или равном 80% от должной или лучшей для пациента величины. Провокация бронхоконстрикторного ответа может быть вызвана физической нагрузкой, медикаментами (гистамин, метахолин), аллергенами и пр. Положительным ответом считается снижении ОФВ1 на 20 и более % от исходного уровня.
Способы расчета бронходилатационного ответа
1 .Измерение обратимости бронхиальной обструкции в бронходилатационном тесте по абсолютному приросту ОФВ1в мл:
ОФВ1 абс. (мл) = ОФВ1дилат. (мл) — ОФВ1исх. (мл)
2. Измерение обратимости бронхиальной обструкции по выраженному в процентах отношению абсолютного прироста показателя ОФВ1 к исходному ОФВ1: прирост ОФВ1 исх. (%).= ОФВ1дил.(мл)-ОФВ1исх.(мл.) х100% /ОФВ1исх. (мл) .
3. Измерение вариабельности бронхиальной обструкции методом пикфлоуметрии:
Ограничение скорости воздушного потока.
В основе ограничения воздушного потока лежат четыре основных механизма, являющихся отражением воспалительного ответа дыхательных путей.
Механизмы обструкции бронхов при БА
Острый спазм гладкой мускулатуры бронхов, практически полностью обратим под влиянием бронхолитиков
Бронхоконстрикция может реализоваться по аллергическому и неаллергическим механизмам. Аллергениндуцированная — JgE специфическая острая бронхоконстрикция осуществляется при участии медиаторов, выделяемых тучными клетками в ходе аллергической реакции. Клинически это проявляется ранней астматической реакцией при контакте с аэроаллергеном (атопическая БА). Неаллергические механизмы острой бронхоконстрикции могут реализоваться при участии лейкотриенов при аспириновой БА, провоцироваться действием физических факторов (физическая нагрузка, изменение осмолярности бронхиальной слизи, холодный воздух, сильные эмоции, пары и химикаты). При астме физического усилия (АФУ). Возможна прямая стимуляция тучных клеток с высвобождением медиаторов, изменение физических свойств бронхиальной слизи с повышением осмолярности , возбуждение локальных и центральных рефлекторных механизмов.
Отек бронхиальной стенки приводит к ее утолщению и ограничению воздушного потока. Развивается в течение 6 -24 часов после действия аллергена (поздняя аллергическая реакция), характеризуется увеличением микрососудистой проницаемости и пропотеванием жидкости, что приводит к утолщению слизистой и отеку бронхов вне гладкой мускулатуры с утратой эластической тяги бронхов. Данный компонент бронхиальной обструкции контролируется противовоспалительными препаратами и, в некоторой степени, бронхолитиками.
Хроническая обструкция вязким секретом (гиперсекреция слизи).
Воспалительный процесс в стенке бронхов сопровождается повышенной секрецией слизи, экссудацией белков сыворотки, слущиванием эпителия образованием клеточного детрита. Формируют плотные пробки, которые обтурируют периферические дыхательные пути. Для разрешения этого механизма требуется длительное время, обычно 6 и более недель лечения кортикостероидами.
Ремоделирование стенки бронхов.
Перестройка бронхиальной стенки, формирующаяся вследствие выраженного и длительно текущего воспаления, является необратимым компонентом ограничения воздушного потока при БА и может быть одной из причин «стероидной резистентности». Структурные изменения матрикса бронхов характеризуются отложением коллагена и протеингликанов под базальной мембраной (субэпителиальный фиброз), гипертрофией и гиперплазией гладкой мускулатуры бронхов и пролиферацией сосудов бронхиальной стенки (утолщение стенки бронха), увеличением числа бокаловидных клеток и гипертрофией подслизистых желез (гиперпродукция слизи.)
Гипревоздушность легких при БА
При остром приступе БА вследствие обструкции бронхов наблюдается появление обширных полей резкого эмфизематозного вздутия, характеризующееся расширением или увеличением ацинусов без разрушения альвеолярных перегородок. Отсутствие деструкции межальвеолярных перегородок объясняют тем, что при БА воспалительный процесс не опускается ниже респираторных бронхиол (в отличии от ХОБЛ). Однако, при присоединении инфекции возможен переход воспаления на легочную ткань и формирование деструктивной эмфиземы. Гиперинфляция — приспособительный механизм, увеличение объема легких сопровождается расширением просвета бронхов. У пациентов БА возникает желание сделать глубокий вдох (рефлекс осуществляется через центростремительные нервы) — это адаптивная реакция, уменьшающая обструкцию за счет растяжения внутрилегочных дыхательных путей. Но при этом возникают неблагоприятные для вентиляции изменения: увеличивается функциональная остаточная емкость легких, диафрагма и межреберные мышцы перемещаются в невыгодное положение для совершения механической работы. Дыхательные мышцы испытывают повышенную нагрузку, преодолевая возросшее эластическое сопротивление легких, грудной клетки и сопротивление суженных дыхательных путей. Резервные способности дыхательных мышц ограничены, в результате наступает их утомление. Больной переходит на частое и поверхностное дыхание. Сочетание повышенного дыхательного рефлекса и усиления сопротивления дыханию сопровождается чувством острой нехватки воздуха при тяжелом приступе БА.
Дыхательная недостаточность при БА
Изменение газов крови наблюдается при тяжелой БА. Первоначально гипервентиляция приводит к развитию гипокапнии. При истощении и неэффективности вентиляции развивается гиперкапния. Клинически заметной ДН становится при снижении ОФВ1 менее 70 % от нормы. Гипоксемия развивается вследствие вентиляционно-перфузионных несоответствий.
Циркуляторные эффекты при тяжелой БА
Тяжелая бронхиальная обструкция сопровождается развитием синусовой тахикардии. Из-за перепадов внутригрудного давления возможно появление парадоксального пульса с колебаниями АД на 15-20 мм (АД увеличивается на выдохе и уменьшается при вдохе).
Таким образом, развитие БА осуществляется при наличии предрасположенности к заболеванию. Воспаление дыхательных путей, возникающее при воздействии индукторов и триггеров приводит к ГРБ, которая сопровождается развитием бронхиальной обструкции и появлению респираторных симптомов БА.
Мокрота у больных аллергической БА содержит конгломераты дегенерированных клеточных элементов и эозинофильный детрит. Типичными элементами мокроты при бронхиальной астме являются спирали Куршмана и кристаллы Шарко-Лейдена. Спирали Куршмана могут иметь форму слепка бронхов, имеют в основном мукозный состав, повышенную вязкость и стекловидную консистенцию. Вязкость возрастает при пропотевании из легочных сосудов альбумина, обладающего склеивающими свойствами. Кристаллы Шарко-Лейдена являются дериватами эозинофилов. При присоединении инфекции мокрота приобретает гнойный характер.
Структурные изменения в дыхательных путях при БА
БА является воспалительным заболеванием, воспаление развивается в средних, крупных и в мелких дыхательных путях (МДП), к которым относятся бронхи с внутренним диаметром менее 2 мм (терминальные и респираторные бронхиолы 8-24 порядка). При трансбронхиальной биопсии в бронхах обнаруживается инфильтрация тучными клетками и эозинофилами, повышено содержание IgE. У больных тяжелой БА плотность воспалительных клеток (Тh , тучных, эозинофилов) больше в стенках периферических дыхательных путей по сравнению с бронхами крупного и среднего калибра. Косвенными маркерами воспаления МДП являются повышение уровня эозинофилов и эозинофильного анионного протеина или нейтрофилов и нейтрофильной эластазы в поздней порции индуцированной мокроты у больных БА, а также альвеолярной фракции оксида азота. Экспериментальные исследования выявили более высокую гипререактивность мелких дыхательных путей по сравнению с крупными бронхами в ответ на ацетилхолин и аллергены. Персистирующее воспаление МДП обусловливает такие функциональные нарушения, как раннее закрытие мелких дыхательных путей с формированием воздушных «ловушек», снижение эластической отдачи и гиперифляцию легких. Косвенным показателем воздушных «ловушек» является увеличение ООЛ, величина которого коррегирует с периферическим сопротивлением дыхательных путей. Уменьшение ФЖЕЛ обратно пропорционально увеличению ООЛ/ОЕЛ и отражает гиперинфляцию легких. Воздушные ловушки определяются с помощью компьютерной томографии высокого разрешения (КТВР).
Структурные изменения матрикса бронхов характеризуются гипертрофией и гиперплазией гладкой мускулатуры бронхов и пролиферацией сосудов бронхиальной стенки (утолщение стенки бронха), увеличением числа бокаловидных клеток и гипертрофией и дегенерацией подслизистых желез, (гиперпродукция слизи). Наиболее типичны для БА изменения базальной мембраны бронхов, она утолщается до 10-30 мкм (при норме 7 мкм), гиалинизируется, в ней откладываются IgM и С3 компонент комплемента. В результате отложения коллагена и протеингликанов под базальной мембраной и в других слоях стенки бронха развивается субэпителиальный фиброз, который отмечается у всех больных БА, даже до начала клинических проявлений. Под действием лечения выраженность его может уменьшаться. У больных БА, умерших от других причин, выявляются изменения в легочной паренхиме, бронхах и сосудах. Легкие перерастянуты, могут занимать всю грудную полость, прикрывая переднюю часть перикарда, но без деструкции межальвеолярных перегородок и нарушения архитектоники. В просвете бронхов определяются слизистые пробки, слизистая оболочка бронхов отечна, имеются дегенеративные изменения мерцательного эпителия, метаплазия и гибель клеток с обнажением базальной мембраны. Повышено количество бокаловидных клеток.
Таким образом, развитие БА осуществляется при наличии предрасположенности к заболеванию. Воспаление дыхательных путей, возникающее при воздействии индукторов и триггеров приводит к ГРБ, которая сопровождается развитием бронхиальной обструкции и появлению респираторных симптомов БА.
Вернемся к истории болезни пациентки А.
В пользу предполагаемого диагноза БА у пациентки свидетельствуют данные анамнеза, указывающие на наличие наследственной предрасположенность к БА (бабушка больна БА) и атопии ( у матери атопический анамнез), проявления гиперчувствительности к пыльце и домашней пыли на протяжении жизни. Повторные эпизоды респираторных инфекций, вероятно, выполняют роль триггеров, стимулируя аллергическое воспаление. Под влиянием инфекции дыхательных путей происходит повреждение эпителия, усиление высвобождения медиаторов и стимуляция позднего астматического ответа на имеющиеся ингалируемые аллергены (аллергены пыльцы, домашней пыли у данной пациентки).У нашей больной
утяжеление заболевания совпадает с периодом менопаузы, что не исключает роль гормонального дисбаланса в патогенезе заболевания.
БА отличается разнообразием клинической картины. Симптомы и течение болезни могут различаться у пациентов разного возраста, изменяться под действием факторов внешней среды, психоэмоционального состояния, социальных условий. Для диагностики БА важен анализ жалоб и сбор анамнеза, на основании которых в большинстве случаев диагноз может быть установлен. Вместе с тем, картина болезни может иметь стертый характер, нередко симптомы кашля и одышки расцениваются как обострения хронического бронхита. Поэтому важное значение имеет раскрытие причин появления респираторных симптомов. Для оптимизации метода опроса больного разработаны стандартизированные вопросы, которые помогают больному изложить жалобы, а врачу осуществлять диагностический процесс. Российским респираторным обществом рекомендован к использованию Тест по контролю над астмой (АСQ), который позволяет оценить степень контроля над заболеванием. Тест включает 5 вопросов, ответы на которые больной оценивает в баллах и по суммарному результату оценивает степень контроля над заболеванием.
БА является заболеванием, при котором правильно построенная беседа с больным позволяет получить достаточно информации для диагностики БА, о причинах ее возникновения, предрасполагающих, провоцирующих факторах, о роли наследственности и пр.
Анализ жалоб. Наиболее характерным для неконтролируемой БА является симптомокомплекс удушья, протекающего по типу экспираторного диспноэ. Начало приступа БА обычно сопровождается кашлем, который предшествует развитию удушья, носит изнуряющий, непродуктивный характер (начальный кашель). Большое значение в картине удушья придается силе кашлевого рефлекса: с ослаблением мышечной силы снижается эффективность кашля и развивается картина тяжелого удушья, на высоте приступа кашель обычно отсутствует. При завершении приступа кашель вновь усиливается с отхождением вязкой мокроты (кашель завершающего периода). В ряде случаев в клинической картине кашель является доминирующим симптомом, в этих случаях выделяют кашлевой вариант БА, который рассматривается как легкая степень заболевания.
Сбор анамнеза. Сбор анамнеза играет решающую роль в диагностике БА. При первой встрече с больным сложно получить исчерпывающую информацию, поэтому необходимо повторно обращаться к сбору анамнеза, по мере получения новых объективных диагностических данных. В процессе сбора анамнеза у больного БА необходимо выяснить наличие наследственной предрасположенности к аллергическим реакциям.
Наследственная предрасположенность. Выясняется наличие аллергических заболеваний (астма, вазомоторной ринит, крапивница, вазомоторный отек Квинке, экзема) у кровных родственников.
Аллергологический анамнез Для больных БА характерно наличие легочных и внелегочных проявлений атопии. Признаками поллиноза являются сезонный характер обострений, привязанный к пыльцевому календарю в данной географической зоне, сопутствующие симптомы ринита, конъюнктивита. Внелегочные проявления аллергии проявляются атопическим дерматитом, экземой, крапивницей, ангионевротическим отеком, которые провоцируется приемом определенных пищевых продуктов с выраженными аллергенными свойствами (клубника, шоколад, цитрусовые и пр.). Провоцирующими факторами в возникновении кожных проявлений аллергии могут быть стрессы различной природы, холод, лекарственные препараты (антибиотики, витамины, салицилаты, сыворотки и вакцины). Появление респираторных симптомов при проведении уборки квартиры, просмотре старых книг, газет, контакте с домашними животными, ночное преимущество симптомов, наличие эффекта элиминации характерно для сенсибилизации бытовыми аллергенами. При длительности БА до года у 50% пациентов выявляется атопическая природа заболевания и почти в половине случаев в стадии моноаллергии. В этой стадии можно ожидать эффекта от специфической иммунотерапии. При длительности заболевания свыше трех лет атопия выявлялась в 19% случаев, причем поливалентная сенсибилизация -до 90%.. что сопровождается утяжелением течения БА .
Лекарственный анамнез. Важное значение имеет указание больного на то, что те или иные лекарственные препараты могут приводить к появлению или утяжелению симптомов БА. Наиболее аллергизирующими свойствами обладают антибиотики, сульфаниламидные препараты (перекрестная гиперчувствительность к новокаину). Следует выяснить переносимость больным препаратов ацетилсалициловой кислоты и других НПВП. Среди пациентов с непереносимостью аспирина смертность достигает 10%, анафилактически — подобные реакции развиваются после приема аспирина и пищевых продуктов, содержащих салицилаты в повышенных концентрациях. У данных больных следует обратить внимание на состояние слизистой носа, характерным является наличие полипозных разрастаний, причем ухудшение течение астмы отмечается после полипэктомии. Следует выяснить, какие лекарственные средства и с какой эффективностью принимает больной для купирования симптомов БА, потребность в бронхолитических препаратах, приеме глюкокортикостероидов. Эти сведения позволяют установить степень контроля над БА, конролиролвать возможные побочные реакции на медикаменты.
Инфекции дыхательных путей. Больные БА отличаются особой восприимчивостью к вирусным инфекционным заболеваниям, обычно сопровождающимися обострениями БА. В анамнезе больных БА необходимо выяснить сведения о перенесенных пневмониях, бронхитах, частых ОРВИ, особое внимание придается локализованной инфекции в придаточных пазухах носа, хроническому тонзиллиту, отиту, состоянию полости рта. При прогрессировании БА часто присоединяется инфекционный процесс в бронхах и легких. Частое и длительное нарушение бронхиальной проходимости приводит к повреждению мукоцилиарного барьера, развитию ателектазов, нарушению аэрации с развитием очагов инфекции, бактериальной сенсибилизации и присоединению инфекционно-аллергического компонента.
Переносимость физической нагрузки. У ряда больных БА удушье может провоцироваться физическими усилиями: быстрой ходьбой, бегом. Если симптомы астмы появляются после прекращения физического усилия в ближайшие 10 минут или через несколько часов после нагрузки, можно предполагать особый вариант БА -астму физического усилия.
Пищевой анамнез. Приступы удушья у ряда больных возникают при употреблении того или иного пищевого продукта. По механизмам патогенеза пищевая астма относится к аллергическим реакциям замедленного типа, поэтому симптомы БА возникают через 8-12 часов после приема пищевого продукта. Диагностическое значение имеет сочетание респираторных симптомов с другими аллергическими проявлениями, таких, как атопический дерматит, крапивница, отек Квинке. При пищевой аллергии отсутствует сезонность, характерна роль наследственного фактора (в семьях прослеживается непереносимость одних и тех же пищевых продуктов), присутствует эффект элиминации (голодание приводит к прекращению симптомов). В клинической картине пищевой астмы выражен экссудативный компонент, образуется большое количество бронхиальной слизи.
Роль экологических и метеорологических факторов. При расспросе больного необходимо выяснять влияние на пациента погодных факторов, так как известно, что быстрая смена погоды, холодный и влажный воздух, экологически неблагоприятные воздействия могут провоцировать симптомы астмы.
Профессиональный анамнез. Выяснение профессионального маршрута имеет важное значение, так как известен ряд профессий, связанных с действием аллергизирующих факторов (химическая, текстильная, пищевая, сельскохозяйственная, меховая промышленность).
Нервно – психические и стрессовые воздействия. При оценке нервно-психического статуса учитываются особенности характера больного (мнительность, боязливость, склонность к ипохондрии), наличие у больного функционального расстройства нервной системы.
Дизгормональные расстройства. Патология эндокринной системы оказывает негативной влияние на течение БА. У женщин может выявляться связь дизовариальных расстройств с проявлениями заболевания: усиление симптомов в предменструальный период, во время беременности. Для климактерического периода характерно утяжеление симптомов БА, высокая эозинофилия, быстрое развитие побочных реакций на прием кортикостероидов и симпатомиметиков. при наступлении климакса. Заболевания щитовидной железы (гипертиреоз), сахарный диабет способствуют развитию ятрогенных реакций на прием противоастматических средств.
Сопутствующие заболевания. У пожилых людей БА часто сочетается с ИБС и гипертонической болезнью. Для данных больных особенно важно при назначении медикаментозной терапии учитывать кардиотоксические эффекты симпатомиметиков и теофиллинов, которые могут проявляться сердечными аритмиями, острой ишемией миокарда, повышением АД. У этих больных необходимо дифференцировать одышку, обусловленную БА, от проявлений сердечной недостаточности, приступы БА — от приступов сердечной астмы. Симптомы со стороны желудочно-кишечного тракта нередко встречаются у больных БА. Полагают, что кишечник и желудок могут выступать как орган-мишень при аллергических реакциях. Одним из клинических признаков при пищевой сенсибилизации является метеоризм. В кале таких больных могут присутствовать эозинофилы и кристаллы Шарко-Лейдена, что дало основание использовать термин «кишечная астма». При наличии рефлюкс-эзофагита возможна аспирация желудочного содержимого в дыхательные пути, что может приводить к ночным эпизодам удушья. Патология эндокринной системы оказывает негативной влияние на течение БА. Заболевания щитовидной железы (гипертиреоз), сахарный диабет способствуют развитию ятрогенных реакций на прием противоастматических средств. Для климактерического периода характерно утяжеление симптомов БА, высокая эозинофилия, быстрое развитие побочных реакций на прием кортикостероидов и симпатомиметиков.
Объективное обследование больного БА.
Осмотр больного. Вне приступа БА изменений внешнего вида больного нет, либо они могут быть обусловлены сопутствующими заболеваниями. При развитии приступа БА кожные покровы могут приобретать бледно-сероватую окраску, при астматическом состоянии появляется диффузный теплый цианоз, выраженность которого соответствует тяжести вентиляционных нарушений. В период приступа возможно обильное потоотделение. На кожных покровах могут иметься признаки атопического дерматита с характерной локализацией в области носогубного треугольника. глазниц, сгибательных поверхностей конечностей. Если больной длительно принимает глюкокортикоиды, кожа истончается, особенно на предплечьях, приобретая вид папиросной бумаги, легко травмируется с отслаиванием эпидермиса и образованием кровоподтеков. На поверхности кожи имеются синячки и точечные кровоизлияния вследствие стероидной ангиопатии. При стероидозависимой БА часто развивается грибковое поражение ногтей, кожных покровов и слизистых оболочек, что всегда характеризует тяжелую астму и ухудшает прогноз. У больных стероидозависимой астмой отмечаются изменения костно — мышечного аппарата: развиваетяся атрофия мышц, остепороз с возможными нетравматическими переломами, асептический некроз головки бедренной кости. При начале заболевания в раннем детстве и тяжелом течении возможно формирование деформаций скелета в виде кифосколиоза, бочкообразной грудной клетки, развивается грудь «сапожника». На фоне гормональной терапии развивается синдром Иценко-Кушинга с нарушениями жирового и углеводного обмена , артериальной гипертензией. Со стороны верхних дыхательных путей возможны проявления ринита в виде заложенности носа, обильной ринорреи, чихания, которые являются симптомами аллергического или вазомоторного ринита.
Система дыхания. Развернутый приступ БА характеризуется дистанционными сухими хрипами, брадипноэ или, реже, тахипноэ до 20-24 в минуту, коротким вдохом и продолжительным шумным выдохом и отсутствием апноэ. При тяжелом приступе больной разговаривает отрывистами фразами или отдельными словами. Положение вынужденное — сидя или стоя, руками больной фиксирует плечевой пояс, что облегчает работу дыхательных мышц по преодолению возросшей обструкции дыхательных путей. Наибольшая нагрузка приходится на mm trapezius, levator scapule, rhomboideus, sternocleidomastoideus. Они приподнимают плечевой пояс так, что создается впечатление короткой и втянутой шеи; грудная клетка приобретает цилиндрическую форму, не опадает вместе с выдохом; надключичные ямки выполнены выбухающей апикальной частью легких, возникшей из-за остро развившейся гиперинфляции во время приступа, подключичные ямки втягиваются при вдохе. В дыхании активно участвуют наружные и внутренние межреберные мышцы, мышцы брюшного пресса и диафрагмы. Признаком утомления дыхательных мышц является развитие парадоксального дыхания — на вдохе видно втяжение межреберных и брюшных мышц, возможно появление болей по линии прикрепления диафрагмы. Тягостное ощущение удушья формируется вследствие появления сигнала сенсорного восприятия утомления респираторных мышц, происходящего из веретенообразных волокон, соединяющих внутренние и наружные межреберные мышцы. При развернутой картине удушья экскурсии легких сокращены, при перкуссии легочный звук с коробочным оттенком, нижние границы легких опущены в среднем на одно ребро, При аускультации определяется «пестрая» картина: чередование участков ослабленного дыхания в зонах максимальной обструкции с участками жесткого дыхания. Над всей поверхностью легких слышны сухие жужжащие и свистящие хрипы, с преобладанием последних, в большем количестве определяющиеся в нижнебазальных отделах легких, более интенсивные в фазу выдоха. Неблагоприятным прогностическим признаком является уменьшение или исчезновение хрипов в нижних отделах — появление зон «немого легкого», и преимущественная локализация хрипов в верхних отделах легких, что свидетельствует об обтурации бронхов вязкой слизью и чаще соответствует астматическому статусу. Разрешение приступа характеризуется усилением или возобновлением кашля, увеличением количества сухих хрипов и отхождением мокроты слизистого стекловидного характера в виде слепков мелких бронхов. Количество мокроты никогда не бывает обильным, но возрастает при присоединении инфекционного процесса. Характерной особенностью приступа БА, имеющей важное диагностическое и прогностическое значение, имеет реакция больного на прием бонходилататоров, симпатомиметики и теофиллиновые препараты купируют приступ БА, отсутствие или ослабление эффекта свидетельствуют о тяжелой астме.
Сердечно-сосудистая систем. При обследовании сердца на высоте приступа БА определяется приглушенность сердечных тонов из-за сопутствующей эмфиземы легких, тахикардия, иногда акцент 2 тона над легочной артерией. При развитии астматического состояния возможно появление парадоксального пульса, сердечных аритмий, возможна внезапная остановка сердца. В возникновении кардиальных симптомов придается значение аритмогенному действию симпатомиметиков и теофиллина. У ряда больных в период приступа повышается системное артериальное давление, как проявление симптоматической пульмоногенной АГ. Тяжелое течение БА может сопровождаться развитием осложнений — легочной гипертензии и легочного сердца, возникновение которого связывают с развитием склеротических изменений в сосудах малого круга кровообращения. При прогрессировании хронического легочного сердца появляются признаки сердечной недостаточности.
В межприступный период у больных могут отсутствовать изменения физикальной картины, однако, при персистирующем течении БА сохраняются сухие хрипы, особенно в горизонтальном положении, которые сам больной слышит на расстоянии, сохраняется кашель и отхождение мокроты, определяются признаки викарной эмфиземы легких.
Система пищеварении. При осмотре ротовой полости возможны поражения слизистой в виде стоматита, глоссита, кандидоза. Поражения развиваются вследствие действия ряда причин: аллергической реакции, побочных эффектов ингаляционных стероидов, дисбактериоза. При наличии язвенного поражения желудка необходимо исключать ятрогенную природу как следствие приема глюкокортикостероидов. Особенностью стероидных язв является бессимптомное течение и склонность к кровотечениям. Рефлюкс-эзофагит может быть причиной ночных приступов БА из-за аспирации желудочного содержимого. Нарушения функции поджелудочной железы, печени, желчевыводящих путей, кишечника возможны вследствие аллергических и побочных реакций на лекарственные препараты, ферментопатий. В литературе описаны случаи стероидного панкреатита.
Мочевыводящая система. Поражение почек не свойственно БА. В случае сочетании симптомов БА и нефрита необходимо исключать системные иммунопатологические заболевания (узелковый полиартериит, и др). Наличие сопутствующей патологии, особенно пиелонефрита и мочекаменной болезни, могут отягощать течение БА.
Эндокринная система. Большое значение в генезе БА имеют дисгормональные нарушения. При приеме стероидов возможны внешние проявления, связанные с гиперкортицизмом и осложнениями гормональной терапии: одутловатое лицо, багровые стрии, акне, диспластиченский тип ожирения, синяки и легкая ранимость кожных покровов как следствие стероидной вазопатии.
данные объективного обследования характерны для клинической картины приступа бронхиальной астмы: бледный цианоз, одышка экспираторного характера, шумное дыхание с дистанционными свистящими хрипами, признаки гиперинфляции легких (коробочный перкуторный звук, раздутые верхушки легких, выполняющие надключичтные ямки), обилие свистящих хрипов и удлинение выдоха при аускультации. Таким образом, предварительный диагноз БА является вполне вероятным. Для подтверждения нозологического диагноза необходимо проанализировать данные инструментального и лабораторного обследование больного .
Методы обследования при БА.
Лабораторные исследования помогают подтвердить предполагаемый диагноз, оценить эволюцию заболевания и эффективность проводимого лечения. При исследовании периферической крови возможна эозинофилия (норма от1до 4% всех лейкоцитов), но повышение эозинофилов у больных БА варьирует, имеется суточный ритм, который контролируется гидрокортизоном с максимумом в ночные и минимумом – в утренние часы. Циркуляция эозинофилов в крови составляет несколько часов, затем они выходят в ткани, где остаются несколько дней. У больных с острой тяжелой астмой возможна эозинопения вследствие миграции клеток в респираторный тракт. Количество эозинофилов выше у больных с атопической БА, а более высокий уровень — при аспириновой БА. На количество эозинофилов влияют лекарственные препараты: ГКС тормозят высвобождение эозинофилов из костного мозга и хемотаксис в ткани. Эозинопению и торможение активности эозинофилов могут вызывают бета-2 агонисты, теофиллин, кромогликат натрия. Биохимическое исследование крови (белок и его фракции, острофазовые реакции) показаны для подтверждения инфекционного характера обострения БА. Для диагностики дисгормонального фона по показаниям проводится исследование гормонов коры надпочечников ( 11-ОКС), прогестерона, эстрогенов.
Неинвазивное определение маркеров воспаления дыхательных путей. Для оценки активности воспалительного процесса можно использовать спонтанно продуцируемую или индуцированную ингаляцией гипертонического раствора мокроту и бронхоальвеолярный смыв на наличие клеток воспаления: эозинофилов, базофилов, нейтрофилов. Отмечают как количественные, так и морфологические и функциональные изменения клеток. Могут присутствовать кристаллы Шарко-Лейдена, представляющие собой структуру, состоящую из белка — эозинофильной лизофосфолипазы и фрагментов мембран эозинофилов. При инфекционной этиологии обострения БА возможно преобладание в мокроте и бронхиальных смывах нейтрофильных лейкоцитов. Маркером воспаления является повышенный уровень окиси азота и окиси углерода в выдыхаемом воздухе. В случаях, когда обострение БА связано с острой или обострением хронической инфекции дыхательных путей показано микробиологическое исследование мокроты (высев патогенной бактериальной флоры, грибов в диагностических титрах), вирусологическое исследование (выявление вирусных антигенов в эпителии слизистой оболочки носа, серодиагностика) .
Оценка аллергологического статуса. Наличие аллергических заболеваний и наследственной предрасположенности увеличивают вероятность БА. Гиперчувствительность к определенным аллергенам устанавливается с учетом данных анамнеза и методом кожных тестов с использованием набора предполагаемых аллергенов вне обострения заболевания. Наиболее достоверной является специфическая диагностика БА — выявление специфической гиперреактивности бронхов с помощью ингаляционных провокационных тестов, однако такой путь введения может спровоцировать тяжелый приступ БА или развитие астматического статуса. При диагностики пищевой аллергии проводятся элиминационные диеты с ведением пищевого дневника . Для специфической диагностики БА, например, при невозможности проведения аллергологического тестирования, применяют также радиоаллергосорбентный тест и ферментный иммуносорбентный анализ позволяющий количественно оценить аллергенспецифические IgE-антитела.
Спирометрия. Оценка функции легких позволяет определить тяжесть бронхиальной обструкции, ее обратимость, вариабельность и подтвердить диагноз БА. Спирометрии выявляет характерные признаки нарушения бронхиальной проходимости по обструктивному типу: снижение объема форсированного выдоха за первую секунду (ОФВ1), уменьшение соотношения ОФВ1 /ФЖЕЛ в процентах. Показатели спирометрии показательны при обструкции, связанной с патологией крупных и мелких бронхов. Термин «обратимость» бронхиальной обструкции означает быстрое увеличение ОФВ1 через несколько минут после ингаляции бронхолитика быстрого действия (200-400 мкг сальбутамола), или медленное улучшение функции легких в процессе лечения. Критерием диагностики БА является прирост ОФВ1 > 12% или > 200 мл по сравнению с исходным показателем. Для стойкой бронхиальной обструкции при преимущественном поражении МДП характерно уменьгение форсированной жизненной емкости легких (ФЖЕЛ). При анализе спирограммы могут обнаруживаться признаки трахеобронхиальной дискинезии, способствующей нарушению бронхиальной проходимости, по наличию зазубрины в верхней части нисходящего колена спирограммы (симптом Колбета—Висса). Появление повышенного бронхиального сопротивления в ответ на физическую нагрузку, вдыхание холодного воздуха, раздражающих газов, свидетельствует об измененной реактивности бронхов. Пикфлоуметрия позволяет контролировать бронхиальную проходимость по пиковой скорости выдоха (ПСВ) в л/мин. Термин «вариабельность» обозначает колебание выраженности симптомов и показателей функции легких в течение определенного времени — одних суток, нескольких дней, месяцев или носить сезонный характер. Определение вариабельности является важным диагностическим критерием БА и критерием для оценки контроля над заболеванием. Суточная пикфлоуметрия позволяет оценить степень вариабильности бронхиальной обструкции, нарастание разницы между утренними и вечерними показателями может являться первым признаком обострения БА. Прирост ПСВ после ингаляции бронхолитика на 60 л/мин или на величину > 20% ПСВ означает обратимость обструкции, а изменения ПСВ в течение суток более чем на 20%, или разница при измерении утренних и вечерних показателей более чем на 10% является признаком, характерным для БА. Преимуществом метода является возможность самоконтроля больного и своевременная диагностика нарастания бронхиальной обструкции
Бодиплетизмография . При тяжелой БА преобладающее значение в формировании бронхиальной обструкции имеет воспаление и обструкция МДП, которое приводит к преждевременному закрытию их при выдохе и формированию воздушной «ловушки». При этом возрастает остаточный объем легких (ООЛ), общая емкость легких (ОЕЛ) и изменяется отношение ООЛ/ОЕЛ. Эти параметры можно определить методом бодиплетизмографии. снижение ФЖЕЛ.
Оценка бронхиальной реактивности. У пациентов в клиническими симптомами БА и при неизмененной функции легких в постановке диагноза могут помочь провакационные пробы, либо прямые с ингаляцией метахолина или гистамина, либо непрямые провоцирующие воздействия, такие как физическая нагрузка. Оценка пробы производится по величине снижения показателя ОФВ1 как правило на 20%. Положительный результат не всегда может указывать на наличие БА, бронхиальная гиперреактивность может иметься у пациентов с аллергическим ринитом, ХОБЛ и другими заболеваниями респираторного
Рентгенологическое исследование. Рентгенография органов грудной полости позволяет установить повышение воздушности легких, выявить сопутствующую патологию. При компьютерной томографии высокого разрешения (КТВР) можно выявить перибронхиальные утолщения стенок средних, крупных и мелких бронхов, определить наличие и тип эмфиземы легких. На КТ, выполненных в фазу вдоха, выявляется мозаичная картина плотности легочной ткани. На экспираторных КТ выявляется воздушная «ловушка»: в зоне обструкции, вследствие неполной эвакуации воздуха, отмечается повышенная воздухонаполненность легких по сравнению с участками неизмененных бронхиол, где плотность легочной ткани больше. Эти КТ- признаки являются более чувствительными по сравнению со спирометрическими показателями для выявления ранних стадий поражения МДП. По показаниям пациентам проводится исследование придаточных пазух носа.
ЭхоКГ и ЭКГ могут выявить признаки легочного сердца (легочную гипертензию, нарушения кардиогемодинамики и гипертрофию правых отделов сердца), определить сопутствующую патологию сердца.
Исследование газового состава крови и кислотно-основного состояния.Показанием для проведения газового анализа крови является затянувшийся приступ БА. Общедоступным скрининговым методом является метод пульсоксиметрии, выявляющий насыщение кислородом капиллярной крови. Снижение показателя Sa02 до 90% и ниже соответствует уровню парциального давления кислорода Pa02 менее 60 мм рт.ст., что сопровождается изменением кислотно-щелочного состояния крови и является показанием для проведения расширенного исследования.
Тест вымывания азота при одиночном вдохе. Увеличение содержания NO в выдыхаемом воздухе отражает воспалительный процесс в респираторном тракте при многих бронхолегочных заболеваниях. В настоящее время установлено, что NO является маркером атопического воспаления при БА. Тест имеет значение для выявления обструкции на уровне МДП. Для БА с поражение МДП характерно повышение содержание оксида азота в выдыхаемом воздухе вследствие увеличения высвобождения NO из альвеолоцитов II типа и эпителия дистальных бронхов.
Трансбронхиальная биопсия. Метод морфологичесого исследования биоптатов из стенки бронхов позволяет оценить выраженность и распространенность воспаления бронхов при БА, решать вопросы прогноза и дифференциального диагноза, но ввиду сложности не относится к рутинным методам обследования.
Консультации специалистов. Больным БА показаны консультации консультации аллерголога, отоларинголога, психотерапевта, по показаниям – эндокринолога и других специалистов.
для верификации предварительного диагноза БА больной проведена пикфлоуметрия до и после введения бронхолитика. Выявлено значительное снижение ПСВ:- 160 л/мин.- 47% от должной величины. Прирост показателя после ингаляции сальбутамола на 100л/мин подтвердил наличие бронхоспазма и обратимость обструкции, что характерно для БА. Кратковременный бронходилатационный эффект, который продолжался около 40 минут с последующим падением ПСВ до исходного значения, указывал на наличие и других механизмов обструкции на фоне тяжелого обострения заболевания. У больной на протяжении суток проводилось мониторирование ПСВ, при этом выявлена значительная вариабельность показателя, что также характерно для неконтролируемой БА в период обострения: суточный разброс= [:1/2]х100%=66%. Наличие дыхательной недостаточности подтверждалось снижением SaO2 до 92%. При рентгенографии выявлены признаки гиперинфляции легких, что характерно для обострения БА. Перегрузка правого желудочка сердца по данным ЭКГ может быть расценена как следствие легочной артериальной гипертензии, развившейся на фоне астматического состояния в ответ на альвеолярную гипоксию.
Диагностические критерии БА
Эпизоды одышки, кашля, свистящих хрипов, заложенности в грудной клетке, особенно ночью и в ранние утренние часы.
Появление симптомов после воздействия определенных факторов (аллергенов при атопической астме, физической нагрузки, НПВП, после ОРВИ и пр.)
Обратимость обструкции бронхов после ингаляции В2- агонистов быстрого действия (быстрое увеличение ОФВ1при спирографии на величину > 12% или 200 мл от исходного значения, при пикфлоуметрии на величину > 20% или на 60 л/мин).
Сезонная вариабельность симптомов, эффект элиминации при атпической БА.
Наследственная отягощенность по БА и атопии.
Внелегочные проявления атопии и аллергии.
Вариабельность обструкции бронхов при неконтролируемой БА: на наличие БА указывает изменение ПСВ в течение суток более чем на 20%
Наличие маркеров воспаления: эозинофилия мокроты или повышение содержания оксида азота и окиси углерода в выдыхаемом воздухе
Обоснование нозологического диагноза пациентки А.
Данные расспроса, объективного и инструментального обследования больной выявили диагностические критерии, подтверждающие диагноз БА:
— приступы удушья с наличием свистящих хрипов, непродуктивного кашля, связь респираторных симптомов с действием аэрополлютантов, аллергенов, инфекционных факторов и купировании их ингаляцией бронхолитика;
— факторы риска: внелегочные проявления аллергии, наследственная отягощенность по БА и атопии.;
-данные объективного осмотра и инструментальных исследований: наличие вариабельной бронхиальной обструкции, гиперифляция легких.
Дифференциальный диагноз БА.
Дифференциального диагноза БА проводится с заболеваниями, имеющими общий с БА синдром обструкции бронхов. Основным дифференциально-диагностического признаком, отличающим БА от других заболеваний с бронхообструктивным синдромом является типичный признак БА –приступ удушья. Диагноз может быть затруднительным при наличии у больного его эквивалентов — дыхательного дискомфорта, непродуктивного кашля, особенно в ночью и рани утром.
Дифференциальный диагноз БА с другими заболеваниями респираторного тракта.
Дифференциальный диагноз БА и хронической обструктивной болезни легких (ХОБЛ)
источник