*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Для цитирования. А.А. Зайцев. Бронхиальная астма у взрослых: ключевые вопросы диагностики и фармакотерапии // РМЖ. 2015. № 18. С. 1096–1100.
Бронхиальная астма (БА) относится к числу наиболее распространенных и социально значимых заболеваний человека. Так, среди взрослого населения европейских стран распространенность БА составляет 6–9%, в США – 11% [1–5]. Согласно официальной статистике, распространенность астмы в России составляет около 3%. В то же время результаты отдельных эпидемиологических исследований позволяют уточнить истинную распространенность БА в Москве – 6,4%, Екатеринбурге – 6,2%, Иркутске – 5,6%. Экспертами Российского респираторного общества признается, что распространенность БА среди детей составляет от 5,6 до 12,1%, а среди взрослых – 5,6–7,3%. В абсолютных цифрах можно предположить, что в России общее число больных БА составляет как минимум 7 млн человек [6, 7].
Проблема усугубляется тем, что больные БА нуждаются в продолжительной медицинской помощи, что требует больших экономических затрат. В развитых странах затраты на ведение пациентов с БА составляют 1–2% от бюджетных средств, выделяемых на здравоохранение. Экономическое бремя БА связано не только с высокими расходами на лечение, но и с затратами, связанными с потерей работоспособности и снижением качества жизни больных [1]. Согласно российским данным, общие расходы на ведение больных БА в 2007 г. составили более 11 млрд руб. [8]. Из них порядка 6 млрд руб. составляют расходы на оказание неотложной помощи и стационарное лечение пациентов в связи с обострением заболевания или ухудшением состояния из-за недостаточно эффективной терапии. Очевидный рост затрат вследствие неадекватной базисной терапии подтверждается целым рядом исследований [9–11]. Таким образом, рациональный выбор терапии для достижения и поддержания контроля над клиническими проявлениями БА является чрезвычайно важной задачей [12–14].
Типичные симптомы БА, отмечаемые большинством пациентов, включают: экспираторную одышку, свистящее дыхание, кашель и заложенность в груди [12]. Наиболее часто симптомы БА проявляются ночью или сразу после пробуждения, а также после физической нагрузки, что зачастую приводит к ограничению физической активности пациентов. Важным этапом клинической оценки БА является оценка внелегочных проявлений аллергии – прежде всего аллергического ринита, конъюнктивита, атопического дерматита. Диагноз БА устанавливается на основании жалоб и анамнестических данных пациента, клинико-функционального обследования с оценкой обратимости бронхиальной обструкции, специфического аллергологического обследования (кожные тесты с аллергенами и/или специфический иммуноглобулин класса Е (IgЕ) в сыворотке крови) и исключения других заболеваний. Важнейшим фактором диагностики является тщательный сбор анамнеза, который укажет на причины возникновения, продолжительность и разрешение симптомов, наличие аллергических реакций у пациента и его кровных родственников, причинно-следственные особенности возникновения признаков болезни и ее обострений.
Начало заболевания БА в большинстве случаев приходится на детский и юношеский возраст. Однако дебют болезни может быть в любом возрасте, и начало болезни у взрослых и даже пожилых пациентов не является редкостью. Вместе с тем бронхообструктивный синдром, впервые развившийся в пожилом возрасте, требует проведения дифференциальной диагностики с целым рядом сходных по клиническому течению заболеваний (хроническая обструктивная болезнь, тромбоэмболия легочной артерии, острая левожелудочковая недостаточность, опухолевый процесс в легких и др.). Важно установить связь появления симптомов БА после контакта с аллергеном, сезонную вариабельность симптомов, сочетание с ринитом, наличие в семейном анамнезе атопии или БА. Иногда встречается кашлевой вариант БА, когда единственным проявлением заболевания является кашель, беспокоящий преимущественно в ночные часы.
Клинические признаки, повышающие вероятность наличия БА [12]:
1) наличие более одного из следующих симптомов: хрипы, удушье, чувство заложенности в грудной клетке и кашель, особенно в случаях ухудшения симптомов ночью и рано утром; возникновение симптомов при физической нагрузке, воздействии аллергенов и холодного воздуха; возникновение симптомов после приема ацетилсалициловой кислоты или β-блокаторов;
2) наличие атопических заболеваний в анамнезе;
3) наличие астмы и/или атопических заболеваний у родственников;
4) распространенные сухие свистящие хрипы при аускультации;
5) низкие показатели пиковой скорости выдоха (ПСВ) или объема форсированного выдоха за 1 с (ОФВ1) (ретроспективно или в серии исследований), необъяснимые другими причинами;
6) эозинофилия периферической крови, необъяснимая другими причинами.
Специальные методы диагностики БА включают исследование вентиляционной функции легких с оценкой обратимости бронхиальной обструкции, выявление бронхиальной гиперреактивности, проведение специфического аллергологического обследования. При проведении спирометрии важным параметром является ОФВ1, указывающий на степень бронхиальной обструкции. Бронходилатационный тест считается положительным, если после ингаляции бронходилататора величина прироста ОФВ1 составляет ≥12% от должного или абсолютный прирост составляет 200 мл и более (для заключения о положительном тесте обязательно достижение обоих критериев). У пациентов с показателями спирометрии в пределах нормы следует провести дополнительное исследование для выявления бронхиальной гиперреактивности – ингаляционный тест с метахолином. Тест является высокочувствительным, поэтому положительный результат является подтверждением БА. Мониторирование ПСВ используется для выявления повышенной суточной вариабельности показателей, характерных именно для БА (вариабельность показателей ПСВ или >30% в течение 1 сут). Характерным признаком БА является эозинофилия периферической крови (более 0,4х109/л), в анализах мокроты обнаруживаются также эозинофилы, кристаллы Шарко – Лейдена, спирали Куршмана. Среди дополнительных тестов стоит упомянуть аллергологическое обследование, позволяющее выявить чувствительность к различным аллергенам, определение общего и специфических IgE. Проба с физической нагрузкой используется для подтверждения БА у детей и подростков. После 7-минутных упражнений более чем у 90% детей с БА наблюдается снижение ОФВ1.
В зависимости от факторов, провоцирующих обострение, выделяют различные клинические формы БА: аллергическая (атопическая), аспириновая, астма физического усилия и др. Аллергические механизмы имеют преобладающее значение (
80% случаев) в развитии детской астмы и обнаруживаются более чем в 50% случаев у взрослых. Такая астма нередко сочетается с аллергическим ринитом, конъюнктивитом и дерматитом. Отмечается гиперчувствительность к различным аллергенам. Для аспириновой астмы характерна триада симптомов: БА, полипозный риносинусит и непереносимость нестероидных противовоспалительных препаратов. Астма физического усилия характерна для молодого и детского возраста (приступ бронхоспазма провоцируется физической активностью – ходьбой, бегом и т. д., причем симптомы возникают не во время действия фактора, а через 5–30 мин после него. Нередко провоцирующим фактором обострения БА является вирусная инфекция, поэтому говорят об инфекционно-зависимой астме. В ряде случаев выделить какой-либо механизм не представляется возможным, поэтому в клинических диагнозах встречается термин «смешанная форма БА».
По степени тяжести БА делится на интермиттирующую и персистирующую (легкой, средней и тяжелой степени тяжести) (табл. 1).
В руководстве GINA (The Global Initiative for Asthma) в настоящее время рекомендована 3-уровневая классификация БА по уровню контроля клинических признаков и характеристике внешнего дыхания (контролируемая, частично контролируемая и неконтролируемая БА) (табл. 2). Такой подход лучше описывает состояние болезни на фоне проводимых лечебных мероприятий, отражает понимание того, что тяжесть БА зависит не только от выраженности симптомов заболевания, но и от ответа на терапию.
Целями фармакотерапии БА являются достижение и поддержание клинического контроля над заболеванием в течение длительного периода времени с учетом безопасности терапии, потенциальных нежелательных реакций и стоимости лечения [12, 14–15]. Увеличение потребности в препаратах неотложной помощи, особенно ежедневное их использование, указывает на утрату контроля над БА и необходимость пересмотра терапии. Если текущая терапия не обеспечивает контроля над БА, необходимо увеличивать объем терапии до достижения контроля. В случае достижения частичного контроля над БА следует рассмотреть возможность увеличения объема терапии с учетом наличия более эффективных подходов к лечению, их безопасности, стоимости и удовлетворенности пациента достигнутым уровнем контроля. При сохранении контроля над БА в течение 3 мес. и более возможно уменьшение объема поддерживающей терапии с целью установления минимального объема терапии и наименьших доз препаратов, достаточных для поддержания контроля.
Фармакотерапия БА включает в себя 2 вида препаратов: препараты неотложной помощи (купирование бронхоспазма) и препараты для базисной («поддерживающей») терапии. К первым относятся β2-агонисты короткого и длительного действия (сальбутамол, фенотерол, формотерол), ингаляционные антихолинергические препараты (ипратропия бромид, тиотропия бромид). Препараты базисной терапии: ингаляционные глюкокортикостероиды (ИГКС) и системные кортикостероиды, комбинированные препараты (пролонгированные β2-агонисты + ИГКС), пролонгированные теофиллины, антагонисты лейкотриеновых рецепторов и антитела к IgE.
ИГКС являются препаратами первой линии в терапии БА, они показаны для лечения персистирующей БА любой степени тяжести [12–14]. ИГКС, составляющие основу базисной противовоспалительной терапии БА, предотвращают развитие симптомов и обострений болезни, улучшают функциональные показатели легких. Раннее назначение ИГКС может улучшить контроль БА и нормализовать функцию легких, а также предотвратить развитие необратимого поражения дыхательных путей. В клинической практике применяются следующие ИГКС: беклометазона дипропионат (БДП), будесонид, флютиказона пропионат, мометазона фуроат и циклесонид.
Отдельной строкой необходимо выделить, что в лечении среднетяжелой и тяжелой БА наиболее эффективной и перспективной является комбинация ИГКС и длительно действующего β2-агониста (ДДБА) [12–14]. В настоящее время в клинической практике применяются следующие фиксированные комбинации ИГКС+ДДБА: салметерол+флутиказон, формотерол+будесонид, формотерол+беклометазон. По результатам ряда исследований показано, что комбинация ДДБА+ИГКС эффективнее увеличенных доз ИГКС, быстрее позволяет достигнуть контроля над симптомами БА, и при использовании комбинированного препарата отмечается снижение количества обострений. Так, исследование GOAL [16] продемонстрировало преимущества комбинированной терапии ИГКС+ДДБА в достижении контроля над симптомами заболевания при среднетяжелой и тяжелой БА по сравнению с монотерапией ИГКС. В авторитетном исследовании N. Barnes et al. было показано, что при персистирующей БА терапия с использованием комбинации флутиказон/салметерол оказалась более эффективной по сравнению с монотерапией флутиказоном [17]. В метаанализе, включившем более 20 тыс. пациентов с персистирующей БА, применение комбинированного препарата салметерол/флутиказон сопровождалось снижением риска обострений заболевания, риска госпитализаций по сравнению с монотерапией ИГКС [18].
Таким образом, в целом ряде клинических исследований было доказано, что добавление ДДБА к низким и средним дозам ИГКС обеспечивает лучший клинический эффект, чем увеличение дозы ИГКС, что в конечном итоге легло в основу современной стратегии ведения больных с БА [12–14].
Очевидно, что большим преимуществом фиксированных комбинаций является не только их высокая эффективность в достижении контроля над симптомами БА, но и хорошая комплаентность за счет соединения 2-х лекарственных средств в одном ингаляторе. Стоит отметить, что представленные на российском фармацевтическом рынке оригинальные комбинированные препараты обладают достаточно высокой стоимостью, но появление в настоящее время дженерических форм, безусловно, расширяет возможности их применения в реальной клинической практике.
Так, в начале 2015 г. в России зарегистрирован препарат Сальмекорт – фиксированная комбинация салметерол+флутиказон в форме дозированного аэрозольного ингалятора (ДАИ) в дозировках 25/50, 25/125 и 25/250 мкг. Клиническая эффективность и безопасность Сальмекорта в сравнении с оригинальным препаратом в форме аэрозоля для ДАИ изучались в рамках клинического исследования, включившего 107 больных с персистирующей БА и нуждающихся в комбинированной терапии высокими дозами ИГКС+ДДБА [19, 20]. Препараты применялись в дозе 25/250 мкг по 2 ингаляции 2 р./сут, продолжительность наблюдения за больными составила 12 нед. В группу больных, получавших Сальмекорт, вошли 56 пациентов, группу сравнения (оригинальный препарат) составил 51 больной с БА. В ходе исследования Сальмекорт продемонстрировал сравнимые с оригинальным препаратом эффективность и безопасность. Так, количество пациентов с положительным ответом на лечение по данным спирометрии составило 35 (64,81%) в группе Сальмекорта и 25 (49,02%) – в группе больных, получавших оригинальный препарат (табл. 3).
При анализе контроля над симптомами БА с использованием опросника АСТ – теста по контролю над астмой (Asthma Control Test) в обеих группах был отмечен значимый прирост показателей на фоне лечения, при этом количество пациентов с приростом оценки как минимум на 1 балл составило 45 в группе Сальмекорта и 40 – в группе сравнения (табл. 4).
В ходе исследования пациенты указывали на уменьшение общего количества приступов БА. При сравнительном анализе оказалось, что статистически значимое уменьшение общего количества приступов астмы наблюдалось в группе больных, получавших Сальмекорт. Анализ частоты развития нежелательных явлений не выявил статистически значимой разницы между группами. Нежелательные явления были зарегистрированы у 9 (16,1%) пациентов, получавших Сальмекорт, и у 3 больных (5,88%) в группе сравнения.
Таким образом, практические врачи располагает теперь более широкими возможностями для базисной терапии БА.
Возвращаясь к принципам терапии, необходимо отметить, что системные глюкокортикостероиды не рекомендуются для поддерживающей терапии БА из-за развития побочных эффектов. Эти препараты применяются для лечения тяжелых обострений БА. Теофиллины длительного действия могут быть использованы в качестве препаратов второй линии у пациентов с персистирующей БА. Анти-IgE-препараты – новый класс лекарственных средств, используемых в настоящее время для улучшения контроля над тяжелой персистирующей атопической БА. В числе наиболее изученных препаратов стоит упомянуть омализумаб. Его применение наиболее оправданно у больных с высоким сывороточным уровнем IgE, нуждающихся в повторных госпитализациях, экстренной медицинской помощи, применяющих высокие дозы ингаляционных и/или системных глюкокортикостероидов.
Для достижения контроля над симптомами БА рекомендован принцип ступенчатой терапии [12]. Каждая ступень включает варианты лечения, которые могут служить альтернативой при выборе поддерживающей терапии БА. У большинства больных с симптомами персистирующей БА, не получавших терапии, следует начинать лечение со ступени 2. Если симптомы БА при первичном осмотре указывают на отсутствие контроля (табл. 5), то лечение необходимо начинать со ступени 3. Если лечение неэффективно или ответ на него недостаточен, проверьте технику ингаляции, соблюдение назначений, уточните диагноз и оцените сопутствующие заболевания. При принятии решения, дозу какого препарата снижать первой и с какой скоростью, должны быть приняты во внимание тяжесть астмы, побочные эффекты лечения, продолжительность приема текущей дозы, достигнутый положительный эффект и предпочтения пациента. Снижение дозы ингаляционных стероидов должно быть медленным в связи с возможностью развития обострения. При достаточном контроле возможно снижение дозы каждые 3 мес., примерно от 25 до 50%.
источник
А.Н. Цой 1 , В.В. Архипов 1 , А.Г. Чучалин 2
1 — ММА им. И.М. Сеченова, г. Москва
2 — НИИ Пульмонологии МЗ РФ, г. Москва
Выбор источников достоверной информации имеет решающее значение для эффективной медицинской деятельности на всех ее уровнях. Качество имеющейся в распоряжении специалиста информации особенно важно при принятии решения относительно каждого конкретного клинического случая, при создании медицинских стандартов и формуляров, а также общем планировании деятельности здравоохранения [12]. Предложенная в начале 90-х гг. концепция доказательной медицины подразумевает добросовестное, точное и осмысленное использование лучших результатов клинических исследований для выбора лечения конкретного больного [2]. Подобный подход позволяет уменьшить уровень врачебных ошибок, облегчить процесс принятия решения для практических врачей, администрации лечебных учреждений и юристов, а также снизить расходы на здравоохранение и претворять в жизнь крупные социально-ориентированные медицинские проекты и инициативы [2].
Прошло почти 10 лет после появления первого международного руководства по диагностике и лечению бронхиальной астмы (БА) [I]. Российские врачи уже в 1996 г. имели возможность познакомиться с этим документом и применять его в своей практике. Имеется опыт создания аналогичных стандартов по лечению БА, ориентированных на отечественные условия и особенности системы здравоохранения в нашей стране [4]. Можно констатировать, что работа с подобными руководствами заставляет нас во многом пересмотреть вопросы обучения и самообразования практических специалистов, стимулирует отказ от рутинных и недостаточно эффективных методов диагностики и лечения и, в конечном счете, повышает уровень медицинской помощи больным БА.
Стандарты и протоколы по клинической практике предназначены, главным образом, для врачей широкого профиля (терапевты поликлиник и стационаров, врачи скорой помощи) и посвящены наиболее общим вопросам диагностики и лечения. Поэтому для этих руководств характерны строго ограниченный объем теоретических сведений и отсутствие описаний редких форм заболевания и новых экспериментальных методов лечения. Но благодаря этому они выполняют свою основную функцию — предоставляют врачам необходимую и точную информацию, позволяют оптимизировать лечебный процесс и обеспечить одинаково высокое качество медицинской помощи в любом из лечебных учреждений.
Первые руководства по клинической практике [1,3] строились по принципу консенсуса группы специалистов, однако в наши дни этого подхода явно недостаточно. Современный врач нуждается в строго взвешенных рекомендациях, основанных на данных наиболее качественно выполненных клинических исследований. Поэтому применение методов доказательной медицины, и в частности рейтинговой системы рекомендаций, на наш взгляд, более перспективно при подготовке будущих руководств по клинической практике и в дальнейшем обещает стать стандартом при подготовке подобных документов.
Цель настоящего обзора — ознакомить практических врачей с результатами использования концепции доказательной медицины на примере рекомендаций по лечению больных БА. При этом обоснование каждой из рекомендаций проводится с учетом уровня доказательности в соответствии с системой, принятой в доказательной медицине.
Уровень доказательности. Удобным механизмом, который позволяет каждому специалисту легко оценить качество каждого клинического исследования и достоверность полученных данных, является предложенная в начале 90-х гг. рейтинговая система оценки клинических исследований. Для непосредственной оценки исследования используются понятия — уровень доказательности. Обычно выделяют от 3 до 7 уровней доказательности [19], при этом с возрастанием порядкового номера уровня (обозначается латинскими числами) качество клинического исследования снижается, а результаты представляются менее достоверными или имеют только ориентировочное значение [II].
К I уровню в доказательной медицине принято относить хорошо разработанные, крупные, рандомизированные, двойные слепые, плацебоконтролируемые исследования. К этому же уровню доказательности принято относить данные, полученные в ходе мета-анализа нескольких рандомизированных, контролируемых исследований [2].
Небольшие рандомизированные и контролируемые исследования (в том случае, когда получить статистически корректные результаты, не удалось из-за малого числа больных, включенных в исследование) относят ко II уровню доказательности, а исследования «случай-контроль» или когортные исследования — к II или III уровню. Наконец, данные, содержащиеся в отчетах экспертных групп или консенсусах специалистов, принято относить к III или IV уровню [2].
В зависимости от мнения составителей (национальные общества доказательной медицины, общества специалистов) одно и то же исследование в различных рейтингах может относиться к разным уровням, однако общий порядок распределения исследований — практически везде одинаков. Так, в каждом из этих рейтингов первое место принадлежит крупным, рандомизированным, двойным слепым, плацебоконтролируемым исследованиям (как наиболее достоверным источникам информации), а завершается каждый рейтинг мнениями отдельных специалистов и данными крупных руководств по клинической практике.
В системе доказательной медицины отдельные практические рекомендации по диагностике и лечению различных заболеваний также имеют свой рейтинг — степень убедительности рекомендаций (обозначаются латинскими буквами). Система рейтинга рекомендаций в англоязычной литературе обозначается как сила рекомендаций (Strength of recommendation). При этом рекомендации, вытекающие из исследований I уровня, обозначаются как А, II уровня — В и т.д. Кроме того, к рекомендациям В относятся экстраполяции из исследований I категории доказательности, а рекомендации С строятся как на основании исследований III уровня доказательности, так и на экстраполяции данных исследований I и II уровня. Таким образом, рекомендации уровня А представляются вполне убедительными, так как опираются на веские доказательства, у рекомендаций уровня В — убедительность относительная, а для рекомендаций уровня С имеющихся доказательств недостаточно, но и эти рекомендации могут использоваться с учетом определенных обстоятельств. Положения, относимые к уровню D и Е, представляются доказанными недостаточно [2, II].
В настоящем обзоре была принята система оценки клинических исследований Canadian asthma consensus report (1999) [8]. При присвоении отдельным рекомендациям того или иного рейтингового уровня авторы опирались на мнение экспертов Великобритании и Канады [7, 18, 25].
Рекомендации по диагностике, оценке состояния больных и лечению бронхиальной астмы
Общие принципы лечения бронхиальной астмы в амбулаторных условиях
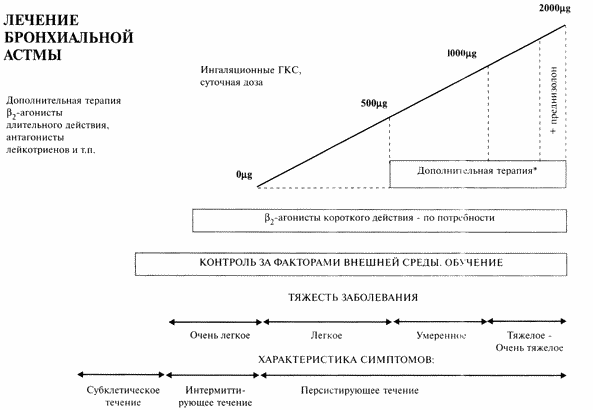
Бронхиальная астма характеризуется значительной вариабельностью тяжести течения. Поэтому для терапии бронхиальной астмы в конце 80-х гг. был предложен ступенчатый терапевтический подход, согласно которому каждой степени тяжести течения заболевания соответствует определенная схема лечения (рис. 1) [I].
Ступенчатый подход к лечению бронхиальной астмы
Первоначально было принято выделять четыре степени тяжести бронхиальной астмы (рис. 2) [ 1, 3]. Впоследствии показалось рациональным выделить группу больных с «очень тяжелым течением БА», т.е. тех, у кого адекватный контроль достигается только при применении пероральных глюкокортикостероидов (ГКС) [8]. К этой категории относят также пациентов с так называемой «трудной /тяжелой/ астмой» (аспириновый вариант астмы, ГКС-зависимая и ГКС-резистентная астма, лабильная астма) [10].
Общий алгоритм лечебного подхода к бронхиальной астме приведен на рис. 2. Он включает диагностический этап, выбор схемы первоначального лечения, подбор долговременной терапии заболевания и последующее наблюдение за больным. Так как бронхиальная астма является хроническим воспалительным заболеванием дыхательных путей [I], эффективность терапии оценивается не как полное излечение, а как адекватный контроль за течением заболевания, предотвращающий обострения ( табл. 1) [8]. Рис. 2
Алгоритм лечения бронхиальной астмы
Диагностика и клиническая оценка бронхиальной астмы
Для подтверждения диагноза бронхиальной астмы и оценки тяжести состояния у всех больных с явлениями бронхообструктивного синдрома следует проводить исследование функции внешнего дыхания (С) [25]. К диагностическим критериям, специфичным для бронхиальной астмы, относятся (D) [1, 3]:
- — увеличение ОФВ1, >12% (предпочтительнее >15%, -т.е. примерно 180 мл) через 15 мин после ингаляции бета2-агониста;
- — увеличение ОФВ1 >20% (около 250 мл) после 10-14 дней лечения преднизолоном;
- — значимая спонтанная вариабельность ОФВ1.
При оценке ОФВ1, и ПСВ следует ориентироваться на среднестатистические нормы для данной популяции, а в идеале — на индивидуальный лучший показатель данного больного, измеренный в период стабильного состояния (С) [З].
Когда проведение спирометрии или бронхопрово-кационного теста недоступны, можно оценить вариа-бельный характер бронхообструкции (> 20%) при многодневном измерении ПСВ в домашних условиях, что также может указывать на наличие бронхиальной астмы (В) [8].
Для установления диагноза бронхиальной астмы используют бронхопровокационный тест с метахолином (С) [8].
Бронхиальная астма и факторы внешней среды
В целом, тяжесть симптомов астмы коррелирует со степенью чувствительности больного к аллергенам [I], хотя у целого ряда пациентов аллергия не играет ведущей роли в течении заболевания. Следует помнить, что увеличение объема медикаментозной терапии не должно заменять предотвращение контактна больного с аллергенами и ирритантами (С) [I].
Больным астмой также следует избегать контакта с табачным дымом (С) [1] и строго воздерживаться от курения (В) [25].
Больным с астмой следует избегать высокой концентрации ирритантов во вдыхаемом воздухе (С) [8], но до сих пор не имеется достаточных данных об эффективности применения для этих целей увлажнителей и других средств очистки воздуха (С) [8].
Все взрослые больные с первично возникшей астмой должны проходить обследования для исключения профессионального характера заболевания (В) [5, 8].
Мониторинг и обучение больных бронхиальной астмой.
Обучение пациентов является обязательным компонентом лечения астмы (А) [З]. Целью обучения является контроль за течением заболевания и выбор правильного поведения больного в различных ситуациях, связанных с заболеванием. Программа обучения не должна строиться только на ознакомлении больных с соответствующей литературой (А), а обучение больных необходимо проводить при каждом личном контакте медицинских работников с пациентами (В) [8], что требует хорошего контакта между медицинским работником и обучаемым (С) [З].
Признаки контроля за течением астмы [8]
| Параметры | Их частота или характеристика |
| Дневные симптомы | 85% от индивидуального лучшего показателя |
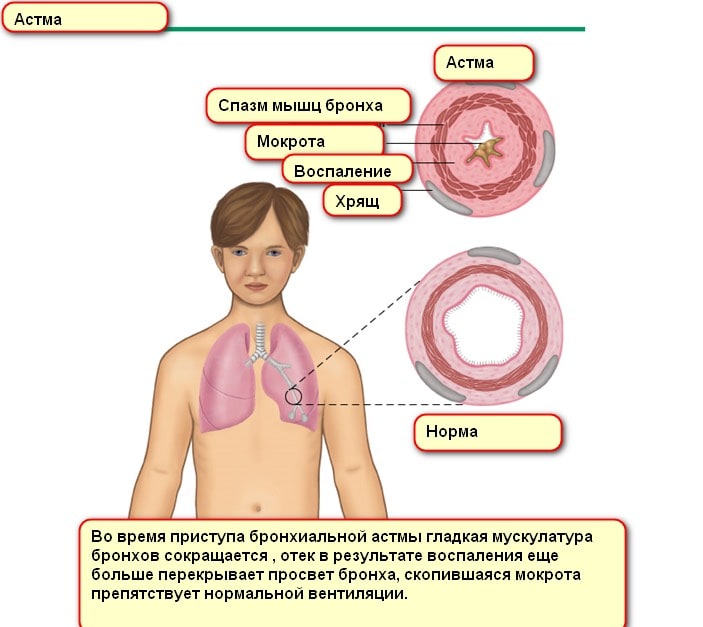
| Дневные вариации ПСВ* | 1000 мкг/сут в пересчете на беклометазон дипропионат, показано проведение денситометрии, в том случае если у них имеются факторы риска остеопороза (С) [8]. Больные, регулярно принимающие ингаляционные ГКС, должны после ингаляций полоскать полость рта водой для предотвращения системной адсорбции препарата (А) [З]. Применение спейсера также снижает риск нежелательного действия ингаляционных ГКС (D) [1, З]. Бета2-агонисты короткого действия Бета2-агонисты короткого действия являются наиболее эффективными бронхолитическими средствами для купирования симптомов бронхиальной астмы (А) и профилактики астмы физического усилия (А) [3, 22]. Хотя применение бета2-агонистов короткого действия приводит к эффективному увеличению величины ПСВ (А) [18], эти препараты не должны рекомендоваться для постоянного применения в качестве базисной терапии (А) [I]. Наличие у больного потребности в ежедневном приеме бета2-агонистов является показанием к назначению противовоспалительной терапии (А) [1, З]. Если у больного бронхоспазм провоцируется физической нагрузкой, то до выполнения физических упражнений рекомендуется применять бета2-агонисты короткого действия (А) [I]. Например, сальбутамол более эффективен для предотвращения бронхоспазма, вызванного физической нагрузкой, чем хромогликат натрия (А) [7]. Пероральные бронхолитики следует рассматривать как препараты второго ряда после ингаляционных бронхолитиков (С) [З]. Бета2-агонисты длительного действия Применение бета2-агонистов длительного действия является альтернативой увеличения доз ингаляционных ГКС при недостаточном контроле за течением астмы [13, 23]. Эти лекарственные средства могут применяться в качестве дополнительной терапии при умеренном и тяжелом течении астмы (А) [3, 8]. Не рекомендуется применять бета2-агонисты длительного действия для купирования острых приступов астмы (за исключением формотерола) и применять эти лекарственные средства при отсутствии противовоспалительной терапии (В). На фоне применения бета2-агонистов длительного действия должен быть продолжен прием препаратов с коротким действием для купирования симптомов (В) [З]. У большинства больных, получавших сальметерол, удается достигнуть удовлетворительного контроля за течением БА при назначении его по 50 мкг дважды в сутки (В) [13]. Сальметерол вызывает значимую бронходилатацию в течение 12 ч; при назначении препарата в суточной дозе 100 мкг побочные эффекты не существенны, но при увеличении дозы их риск увеличивается (В) [13]. Применение сальметерола 2 раза в день более эффективно, чем использование препаратов короткого действия 4 раза в течение дня (А) [7]. Назначение сальметерола у больных с недостаточным контролем за течением БА может быть столь же эффективно, как увеличение дозы ингаляционных ГКС в 2 раза [23]. Антагонисты лейкотриеновых рецепторов Антагонисты лейкотриеновых рецепторов (АЛТ) являются альтернативой увеличения доз ингаляционных ГКС при недостаточном контроле за течением астмы. Эти лекарственные средства могут применяться совместно со средними и высокими дозами ингаляционных ГКС (А) [З]. Недостаточно данных, которые позволили бы отнести АЛТ к числу противовоспалительных препаратов первого выбора у больных бронхиальной астмой, однако у пациентов, которые не могут принимать ГКС, АЛТ являются препаратами выбора (D) [8]. Другим показанием к назначению АЛТ является аспириновый вариант бронхиальной астмы (D) [8]. Препараты хрома. Кромогликат натрия и недокромил могут применяться как альтернатива бета2-агонистам для предотвращения астмы физического усилия (А) [З]. Не существует свидетельств, на основании которых можно предпочесть недокромил хромогликату натрия или наоборот (А) [I]. Хотя недокромил более эффективен, чем плацебо, однако степень его эффективности не позволяет рекомендовать препарат в качестве средства первого ряда лечения БА (А), тем не менее у детей младше 12 лет и взрослых с легким течением астмы он может являться альтернативой низким дозам ингаляционных ГКС, не обладая нежелательными эффектами ГКС (А). Теофиллин. Теофиллин не должен применяться при бронхиальной астме в качестве препарата первого ряда (А) [З]. У пациентов с течением астмы, при котором средние дозы ингаляционных ГКС неэффективны, добавление к теофиллина лечению ГКС может улучшить контроль за течением астмы и сократить потребность в ГКС (В) [I]. Дозу теофиллина следует увеличивать постепенно путем титрации (С) [I]. Антихолинэргические средства. Препараты этой группы не рекомендуются в качестве препаратов первого ряда для лечения бронхиальной астмы, за исключением случаев толерантности к действию бета2-агонистов (С) [8]. Кетотифен не рекомендуется для лечения бронхиальной астмы (В) [8]. При лечении бронхиальной астмы ингаляционный путь доставки бронхолитиков и противовоспалительных препаратов является более предпочтительным, чем назначение этих лекарственных средств перорально или парентерально (А) [З]. В последние годы существенно расширился арсенал средств доставки ингаляционных препаратов. Условно принято выделять аэрозольный дозированный ингалятор (применяются со спейсером или без него), порошковые ингаляторы (турбухайлер, дискхайлер, циклохайлер и т.д.) и небулайзер. Существует алгоритм подбора больному адекватного средства доставки (С) [8]. Согласно этому алгоритму, первоначально больным астмой следует назначать лекарственные препараты в виде дозированных аэрозольных ингаляторов. Если при употреблении дозированных ингаляторов у больного возникают трудности, следует дополнительно применять спейсер большого объема (объем > 0,75 л). Если же и при использовании дозированного ингалятора со спейсером больной не справляется с техникой ингаляций или не может применять их в течение всего дня, то ему показано назначение препарата в виде порошкового ингалятора наиболее дешевой модели или дозированного аэрозольного ингалятора «легкое дыхание». Аэрозольный ингалятор со спейсером показан для всех возрастных групп, у пожилых больных и детей можно применять аэрозольный ингалятор со спейсером, оснащенным лицевой маской (В). При использовании любой системы доставки ингаляционных препаратов необходимо периодически оценивать технику ингаляции и проводить обучение больных (А) [З]. Применение ингаляционных ГКС через спейсер позволяет уменьшить риск кандидоза полости рта (А) [б]. При обострении бронхиальной астмы использование спейсера большого объема является эффективной альтернативой применению небулайзера, при этом удается в несколько (до 7-14) раз уменьшить дозы бронхо-литических средств (А) [7]. Аэрозольные ингаляторы со спейсером большого объема (>0,75 л) можно рекомендовать и при тяжелых обострениях астмы (А) [7]. Дозированные аэрозольные ингаляторы столь же эффективны, как порошковые ингаляторы (А), в том числе аутохаллер (А) [3, 21]. Лечение бронхиальной астмы в условиях стационара Признаком нестабильного течения БА на всех ее стадиях является увеличение потребности в ингаляционных бета2-агонистах (С), более частое, чем обычно, появление симптомов бронхообструкции и уменьшение величины ПСВ (А) [2, 8]. Пациенты, у которых величины ОФВ1 и ПСВ, измеренные до начала лечения, меньше 40% от индивидуального лучшего показателя (ИЛП) или должных величин (ПСВ 70% от должного, имеющие доступ к необходимым медикаментам, обладающие адекватной техникой ингаляции и получившие индивидуальный лечебный план, могут быть выписаны из стационара (D) [8]. Asthma is an illness with many variations in cause and severity. Many treatment options are available to control and reverse asthma symptoms. What’s the best treatment? It is important to provide more effective care for asthma from the point of view of evidence-based medicine. While the situations and outcomes varied-to some degree, the morbidity and resource utilization attributable to asthma can be strikingly reduced if moderate and severe asthmatics receive expert care источник Бронхиальная астма – это хроническое неинфекционное заболевание дыхательных путей воспалительного характера. Приступ бронхиальной астмы часто развивается после предвестников и характеризуется коротким резким вдохом и шумным длительным выдохом. Обычно он сопровождается кашлем с вязкой мокротой и громкими свистящими хрипами. Методы диагностики включают оценку данных спирометрии, пикфлоуметрии, аллергопроб, клинических и иммунологических анализов крови. В лечении используются аэрозольные бета-адреномиметики, м-холинолитики, АСИТ, при тяжелых формах заболевания применяются глюкокортикостероиды. За последние два десятка лет заболеваемость бронхиальной астмой (БА) выросла, и на сегодняшний день в мире около 300 миллионов астматиков. Это одно из самых распространенных хронических заболеваний, которому подверженные все люди, вне зависимости от пола и возраста. Смертность среди больных бронхиальной астмой достаточно высока. Тот факт, что в последние двадцать лет заболеваемость бронхиальной астмой у детей постоянно растет, делает бронхиальную астму не просто болезнью, а социальной проблемой, на борьбу с которой направляется максимум сил. Несмотря на сложность, бронхиальная астма хорошо поддается лечению, благодаря которому можно добиться стойкой и длительной ремиссии. Постоянный контроль над своим состоянием позволяет пациентам полностью предотвратить наступление приступов удушья, снизить или исключить прием препаратов для купирования приступов, а так же вести активный образ жизни. Это помогает поддержать функции легких и полностью исключить риск осложнений. Наиболее опасными провоцирующими факторами для развития бронхиальной астмы являются экзогенные аллергены, лабораторные тесты на которые подтверждают высокий уровень чувствительности у больных БА и у лиц, которые входят в группу риска. Самыми распространенными аллергенами являются бытовые аллергены – это домашняя и книжная пыль, корм для аквариумных рыбок и перхоть животных, аллергены растительного происхождения и пищевые аллергены, которые еще называют нутритивными. У 20-40% больных бронхиальной астмой выявляется сходная реакция на лекарственные препараты, а у 2% болезнь получена вследствие работы на вредном производстве или же, например, в парфюмерных магазинах. Инфекционные факторы тоже являются важным звеном в этиопатогенезе бронхиальной астмы, так как микроорганизмы, продукты их жизнедеятельности могут выступать в качестве аллергенов, вызывая сенсибилизацию организма. Кроме того, постоянный контакт с инфекцией поддерживает воспалительный процесс бронхиального дерева в активной фазе, что повышает чувствительность организма к экзогенным аллергенам. Так называемые гаптенные аллергены, то есть аллергены небелковой структуры, попадая в организм человека и связываясь его белками так же провоцируют аллергические приступы и увеличивают вероятность возникновения БА. Такие факторы, как переохлаждение, отягощенная наследственность и стрессовые состояния тоже занимают одно из важных мест в этиологии бронхиальной астмы. Хронические воспалительные процессы в органах дыхания ведут к их гиперактивности, в результате которой при контакте с аллергенами или раздражителями, мгновенно развивается обструкция бронхов, что ограничивает скорость потока воздуха и вызывает удушье. Приступы удушья наблюдаются с разной периодичностью, но даже в стадии ремиссии воспалительный процесс в дыхательных путях сохраняется. В основе нарушения проходимости потока воздуха, при бронхиальной астме лежат следующие компоненты: обструкция дыхательных путей из-за спазмов гладкой мускулатуры бронхов или вследствие отека их слизистой оболочки; закупорка бронхов секретом подслизистых желез дыхательных путей из-за их гиперфункции; замещение мышечной ткани бронхов на соединительную при длительном течении заболевания, из-за чего возникают склеротические изменения в стенке бронхов. В основе изменений бронхов лежит сенсибилизация организма, когда при аллергических реакциях немедленного типа, протекающих в виде анафилаксий, вырабатываются антитела, а при повторной встрече с аллергеном происходит мгновенное высвобождение гистамина, что и приводит к отеку слизистой бронхов и к гиперсекреции желез. Иммунокомплексные аллергические реакции и реакции замедленной чувствительности протекают аналогично, но с менее выраженными симптомами. Повышенное количество ионов кальция в крови человека в последнее время тоже рассматривается как предрасполагающий фактор, так как избыток кальция может провоцировать спазмы, в том числе и спазмы мускулатуры бронхов. При патологоанатомическом исследовании умерших во время приступа удушья отмечается полная или частичная закупорка бронхов вязкой густой слизью и эмфизематозное расширение легких из-за затрудненного выдоха. Микроскопия тканей чаще всего имеет сходную картину – это утолщенный мышечный слой, гипертрофированные бронхиальные железы, инфильтративные стенки бронхов с десквамацией эпителия. БА подразделяется по этиологии, тяжести течения, уровню контроля и другим параметрам. По происхождению выделяют аллергическую (в т. ч. профессиональную БА), неаллергическую (в т. ч. аспириновую БА), неуточненную, смешанную бронхиальную астму. По степени тяжести различают следующие формы БА:
В течении астмы выделяют обострения и ремиссию (нестабильную или стабильную). По возможности контроля над пристпуами БА может быть контролируемой, частично контролируемой и неконтролируемой. Полный диагноз пациента с бронхиальной астмой включает в себя все вышеперечисленные характеристики. Например, «Бронхиальная астма неаллергического происхождения, интермиттирующая, контролируемая, в стадии стабильной ремиссии». Приступ удушья при бронхиальной астме делится на три периода: период предвестников, период разгара и период обратного развития. Период предвестников наиболее выражен у пациентов с инфекционно-аллергической природой БА, он проявляется вазомоторными реакциями со стороны органов носоглотки (обильные водянистые выделения, непрекращающееся чихание). Второй период (он может начаться внезапно) характеризуется ощущением стесненности в грудной клетке, которое не позволяет дышать свободно. Вдох становится резким и коротким, а выдох наоборот продолжительным и шумным. Дыхание сопровождается громкими свистящими хрипами, появляется кашель с вязкой, трудно отхаркиваемой мокротой, что делает дыхание аритмичным. Во время приступа положение пациента вынужденное, обычно он старается принять сидячее положение с наклоненным вперед корпусом, и найти точку опоры или опирается локтями в колени. Лицо становится одутловатым, а во время выдоха шейные вены набухают. В зависимости от тяжести приступа можно наблюдать участие мышц, которые помогают преодолеть сопротивление на выдохе. В периоде обратного развития начинается постепенное отхождение мокроты, количество хрипов уменьшается, и приступ удушья постепенно угасает. Проявления, при которых можно заподозрить наличие бронхиальной астмы.
В зависимости от тяжести и интенсивности приступов удушья бронхиальная астма может осложняться эмфиземой легких и последующим присоединением вторичной сердечно-легочной недостаточности. Передозировка бета-адреностимуляторов или быстрое снижение дозировки глюкокортикостероидов, а так же контакт с массивной дозой аллергена могут привести к возникновению астматического статуса, когда приступы удушья идут один за другим и их практически невозможно купировать. Астматический статус может закончиться летальным исходом. Диагноз обычно ставится клиницистом-пульмонологом на основании жалоб и наличия характерной симптоматики. Все остальные методы исследования направлены на установление степени тяжести и этиологии заболевания. При перкуссии звук ясный коробочный из-за гипервоздушности легких, подвижность легких резко ограничена, а их границы смещены вниз. При аускультации над легкими прослушивается везикулярное дыхание, ослабленное с удлиненным выдохом и с большим количеством сухих свистящих хрипов. Из-за увеличения легких в объеме, точка абсолютной тупости сердца уменьшается, тоны сердца приглушенные с акцентом второго тона над легочной артерией. Из инструментальных исследований проводится:
Дополнительная диагностика включает в себя проведение тестов с аллергенами, ЭКГ, бронхоскопию и рентгенографию легких. Лабораторные исследования крови имеют большое значение в подтверждении аллергической природы бронхиальной астмы, а так же для мониторинга эффективности лечения.
Поскольку бронхиальная астма является хроническим заболеванием вне зависимости от частоты приступов, то основополагающим моментом в терапии является исключение контакта с возможными аллергенами, соблюдение элиминационных диет и рациональное трудоустройство. Если же удается выявить аллерген, то специфическая гипосенсибилизирующая терапия помогает снизить реакцию организма на него. Для купирования приступов удушья применяют бета-адреномиметики в форме аэрозоля, для того чтобы быстро увеличить просвет бронхов и улучшить отток мокроты. Это фенотерола гидробромид, сальбутамол, орципреналин. Доза в каждом случае подбирается индивидуально. Так же хорошо купируют приступы препараты группы м-холинолитиков – аэрозоли ипратропия бромида и его комбинации с фенотеролом. Ксантиновые производные пользуются среди больных бронхиальной астмой большой популярностью. Они назначаются для предотвращения приступов удушья в виде таблетированных форм пролонгированного действия. В последние несколько лет препараты, которые препятствуют дегрануляции тучных клеток, дают положительный эффект при лечении бронхиальной астмы. Это кетотифен, кромогликат натрия и антагонисты ионов кальция. При лечении тяжелых форм БА подключают гормональную терапию, в глюкокортикостероидах нуждается почти четверть пациентов, 15-20 мг Преднизолона принимают в утренние часы вместе с антацидными препаратами, которые защищают слизистую желудка. В условиях стационара гормональные препараты могут быть назначены в виде инъекций. Особенность лечения бронхиальной астмы в том, что нужно использовать лекарственные препараты в минимальной эффективной дозе и добиваться еще большего снижения дозировок. Для лучшего отхождения мокроты показаны отхаркивающие и муколитические препараты. Течение бронхиальной астмы состоит из череды обострений и ремиссий, при своевременном выявлении можно добиться устойчивой и длительной ремиссии, прогноз же зависит в большей степени от того, насколько внимательно пациент относится к своему здоровью и соблюдает предписания врача. Большое значение имеет профилактика бронхиальной астмы, которая заключается в санации очагов хронической инфекции, борьбе с курением, а так же в минимизации контактов с аллергенами. Это особенно важно для людей, которые входят в группу риска или имеют отягощенную наследственность. источник До 30 сентября действует скидка 20% на курс лечения бронхиальной астмы Обострение астмы полностью «выбивает» человека из нормального ритма жизни. Постоянные ночные симптомы нехватки воздуха, удушливый кашель, плохой сон, невозможность работать и заниматься привычным делом. Для оказания быстрой и эффективной помощи мы применяем сочетанное, комплексное воздействие нескольких методик. В клинике применяется интенсивный курс лечения обострения бронхиальной астмы под контролем врачей пульмонологов с 20-летним опытом работы в НИИ пульмонологии. Программа подходит для взрослых и детей.
Весь комплекс терапии проходит под контролем врача. Поэтому в ходе сеансов можно сделать акценты на особенности заболевания и самочувствия, уменьшить или усилить нагрузку, поменять или добавить препараты для ингаляций. Длительность сеанса 45 минут. Курс лечения включает 5 сеансов. Стоимость 1 сеанса – 5000 руб.* * До 30 сентября действует скидка 20% при оплате всего курса.
Врач-пульмонолог, сомнолог, кандидат медицинских наук, Главный врач медицинского центра «ИнтеграМедсервис» Кандидат медицинских наук, врач-пульмонолог высшей категории, врач функциональной диагностики,заведующая отделением пульмонологии ИнтеграМедСервис, экс-сотрудник ФГУ НИИ пульмонологии ФМБА России. Бронхиальная астма противоречивое, неоднозначное и «капризное» хроническое заболевания легких. Эта болезнь рекордсмен по легендам, заблуждениям, мифам, альтернативным подходам к лечению и шарлатанству. В этой статье постараемся понятно рассказать об этом заболевании. Бронхиальная астма подробно описана и известна давно. Но, несмотря на это по сей день остается загадочным заболеванием. До конца не ясна природа этой болезни. Термин астма дословно означает удушье. Удушье считалось главным, обязательным признаком болезни. Лабораторным доказательством болезни считалась эозинофилия крови и мокроты и аллергия. Но с развитием молекулярной биологии и генетики стало очевидным, что это не так. Современное определение бронхиальной астмы — хроническое воспалительное заболевание нижних дыхательных путей, в развитии которого играют роль большое количество клеток и клеточных элементов. Принято считать, что это воспаление приводит к развитию гиперреактивности бронхов, а следствие этой гиперреактивности — удушье, кашель и одышка. Распространенность бронхиальной астмы увеличивается ежегодно. По информации ВОЗ астмой страдает около 300 млн. человек, затрагивая все возрастные и гендерные группы. За два последних десятилетия в мире произошло двух-кратное увеличение больных бронхиальной астмой. В России с 1998 по 2002 распространенность заболевания увеличилась на 28,2 %. Распространенность болезни в нашей стране составляет 6,9% среди взрослых и 10% среди детей. В РФ бронхиальной астмой болеет 7 миллионов человек. Заболел бронхиальной астмой- я скоро умру? Что касается смертности, то бронхиальная астма редко является причиной смерти. В Канаде, Австралия, некоторых Европейских странах отмечен рост смертности от астмы. А в Англии отмечено снижение этого показателя . Бронхиальная астма не прогрессирующая болезнь, в отличие от ХОБЛ. Болезнь ни во что не перерождается. «О самом главном». Бронхиальная астма: почему она обостряется весной? Послушать выступление Кулешова А.В. на радио Россия. Бронхиальная астма это мульти-факториальное заболевание. Установлено, что фактором развития болезни является семейный анамнез аллергии (атопии). Наличие аллергии в семье увеличивает в 5 раз риск развития аллергического ринита и бронхиальной астмы! Аллергены домашнего клеща, эпидермиса животных, пыльцы растений, таракана, грибов Alternaria считаются наиболее распространенными факторами риска.
Инфекция так же играет спорную роль в развитии болезни. Описаны случаи, указывающие на прямую связь между рецидивирующей в детстве респираторной инфекцией и снижением риска развития бронхиальной астмы. Но при этом известно, что вирусная инфекция часто провоцирует обострение БА. Вероятно, и те и другие наблюдения верны. Инфекция играет роль пускового агента, проявляется на разных этапах жизни человека и влияет на стадии заболевания. Ухудшающаяся экологическая обстановка – бронхиальная астма экологозавиимое заболевание. Уровень промышленного загрязнения и распространенность болезни тесно и напрямую взаимосвязаны. К примеру, распространенность БА среди городских жителей (дети, взрослые) в 1,6-1,8 раза выше, чем в сельской местности. Прочие факторы – это малый или избыточный вес при рождении, курение матери во время беременности, наличие животных в доме, ожирение, избыточное потребление соли.
Симптомы бронхиальной астмы различны и индивидуальны. Нет характерного симптома, который однозначно указывал на то, что человек болеет астмой. Для большинства людней заболевший астмой – задыхающийся человек, постоянно кашляющий и свистящий на все лады. Однако это не обязательно так. На приеме некоторые пациенты жалуются на затрудненный выдох, кто то на сложности с вдохом. Некоторые предъявляют жалобы на кашель ночью, утром, при физической нагрузке,а некоторых удушье не беспокоит. Такой диапазон степени выраженности жалоб и размытости симптомов, характерен для бронхиальной астмы. Астма в период между обострениями может никак себя не проявлять. В этот «спокойный» промежуток времени пациенты совершают ошибку — прекращают лечение. В результате у пациента случается обострение астмы. Для бронхиальной астмы не обязательны:
Я не задыхаюсь, а только кашляю. А доктор говорит, что у меня астма! Разве это возможно? При кашлевом варианте бронхиальной астмы (а встречается и такой) у пациента нет удушья. Мало того показатели ФВД фиксируют нормальные или слегка сниженные показатели вентиляции. Кашель у пациентов с кашлевым вариантом астмы беспокоит ночью и утром, возникает при быстрой ходьбе или при занятиях спортом. Такой вопрос часто звучит на приеме в клинике. Даже имея специальную подготовку в тонкостях диагностики бронхиальной астмы, врачи сталкиваются с диагностической дилеммой — астма или нет? При тщательном опросе пациента, анализа детства и родственных связей, характере жалоб диагноз астмы становиться вероятным. Но это не вся диагностика астмы! Главным функциональным тестом для диагностики бронхо — обструктивного синдрома принято считать спирометрию, или функцию внешнего дыхания, или ФВД. Спирометрия показывает, как функционируют легкие, сужены или нет дыхательные пути (бронхиальная обструкция), изменены ли дыхательные объемы. Тест безболезненный и бескровный. Проводиться в 2 этапа. На первом этапе из трех попыток дыхательного маневра (форсированного выдоха), выбирается больший показатель. Затем врач предлагает вдохнуть бронхо — расширяющий препарат (Сальбутамол) и через 15-20 минут, повторяется этап номер один. Продолжительность процедуры 20-25 мину. Полученный результат расшифровывает сам лечащий врач. Задача теста Несмотря на простоту теста, выполнение дыхательного маневра требует четкости. Как показывает опыт из 10 сделанных ФВД в других поликлиниках и медицинских центрах, только два будут соответствовать критериям качества. Чтобы избежать ошибок при диагностике астмы, в нашей в клинике лечения астмы и аллергии, врачи пульмонологи сами исполняют этот тест. Сложнее становится задача, если спирометрия нормальная, а положительной реакции на препарат нет. В этом случае рекомендуем провести бронхопровакационный тест. Это ФВД наоборот. Это экспертное исследование подтверждает или опровергает диагноз астмы. Бронхопровакационный тест незаменим при диагностике кашлевого варианта бронхиальной астмы и астмы физического усилия. Мы предлагаем прием врачей, специализирующихся на лечении астмы, экспертного уровня в Москве Если Вы подозреваете у себя или близких астму, запишитесь на прием: Тек же у Вас есть возможность обойтись без телефона и записаться онлайн через сайт. Позже, наш диспетчер свяжется с Вами для уточнения деталей приема. Учитывая вариабельность симптомов, функциональных показателей, разнообразие причин развития бронхиальной астмы для контроля требуется классификация. Классификация бронхиальная астма ( по рекомендациям GINA 2016) по степени тяжести: Ступень 1: Интермиттирующая бронхиальная астма
Ступень 2: Легкая персистирующая бронхиальная астма
Ступень 3: Бронхиальная астма средней тяжести, персистирующая. Удушье, кашель беспокоят ежедневно. Нарушен сон, обычная физическая активность дается с трудом.
Ступень 4: Тяжелая персистирующая бронхиальная астма. Тяжелое состояние — дыхательные нарушения и симптомы носят выраженный, ежедневный характер. Обострения сменяют друг друга. Ночные симптомы ежедневные. Значительное снижение физической активности ОФВ1 или ПСВ ≤ 60% от должного. Это опасное состояние. Требуются действия со стороны медицинского персонала, для купирования симптомов и принятия решения о госпитализации в стационар. По этой классификации степень тяжести избирается из самого тяжелого проявления симптома или показателя ФВД. Причем достаточно одного симптома или показателя. Но из-за переменчивости проявлений астмы степень тяжести так же становиться величиной непостоянной. Тяжесть БА – не статичная характеристика. Аллергическая БА: «классика» для нее характерно начало в раннем детстве, как правило, присутствует ряд аллергических сопутствующих заболеваний. Характерен наследственный фактор аллергии. В основе патогенеза лежит эозинофильное воспаление. Ответ на терапию ИГКС хороший. Неаллергическая БА: аллергия не причина развития этого варианта астмы. Воспаление реализуется за счет смешанного, нейтрофильного, эозинофильного звеньев. Ответ на терапию ИГКС иногда отсутствует либо неполный. БА с поздним дебютом: такой вариант чаще встречается у женщин, развивается во взрослом состоянии. При этом типе астмы — аллергия так же не характерна. ИГКС применяют в дозах более 1000 мкг . БА с фиксированной обструкцией дыхательных путей: пациенты, страдающие этим типом астмы, болеют астмой давно. И под воздействием длительного воспаления стенка бронхов видоизменяется на столько, что обструкция становиться постоянной.. БА у больных с ожирением: пациенты с ожирением и БА страдают от выраженных респираторных симптомов, не связанных с эозинофильным воспалением. Определение фенотипов болезни позволяет подойти к лечению персонифицировано и индивидуально. ГЭРБ индуцированная – гастроэзофагеальный рефлюкс актуальная проблема затяжного кашля у пациентов и ГЭРБ способен спровоцировать развитие бронхиальной астмы. Причиной тому вдыхание аэрозоля кислотного содержимого из пищевода. Аспирин зависимая астма — причиной воспаления в бронхах в этой ситуации является аспирин или иные НПВС. Обычно аспириновая форма характеризуется т.н. аспириновой триадой – астма, полипы полости носа и реакция на салицилаты. Кашлевой вариант бронхиальной астмы- с введением в диагностику бронхопровакационного теста стало возможным выявить этот тип болезни. Вместо приступов удушья присутствует спастический кашель с акцентом в ночные или утренние часы. Астма физического усилия – приступы затрудненного дыхания возникают исключительно при физических нагрузках. При ней же отмечается вариабельность показателей вентиляции. Иногда слышны свисты и хрипы. Профессиональная астма – исключительно факторы производственной среды провоцируют эту форму астмы. Иные факторы, вне рабочего места, недолжны при этой форме быть, причиной заболевания. Ночная астма – спорный вариант. Но описаны исключительно ночные приступы нехватки воздуха. Очень часто коррелирует с СОАС. Мульти факториальному заболеванию – многоуровневое лечение! Успешный контроль над бронхиальной астмой возможен в комплексе мероприятий:
Задачи терапии бронхиальной астмы:
Для решения задач применяется ступенчатая терапия. Главный принцип ступенчатой терапии – это увеличение объема терапии при отсутствии должного контроля над астмой (при ее обострении) и соответственное уменьшение этого объема при достижении стабилизации состояния, стихания симптомов болезни. Ступени содержат информацию о вариантах лечения, отличающихся по своей эффективности. Ступень и объем терапии выбираются лечащим врачом и зависят от степени выраженности симптомов астмы у пациента. Применение ступенчатой терапии позволяет, при ее правильном применении, оценить эффективность выбранной схемы лечения. Например, если не удается стабилизовать обострение астмы, необходимо проверить технику использования ингаляторов. Проверить выполняет ли пациент назначения и рекомендации. Возможно, внимания не было уделено сопутствующим болезням? И оценив эти факторы, принимается решение об изменении объема лечения. Снижение объема терапии, например кратности или дозировки ингаляторов, так же требует осторожности. Тяжесть заболевания обязательно учитывается при изменении терапии. Пациенты часто ошибаются отменяя прием препаратов на ранних этапах стабилизации астмы. Лекарства для лечения разделены на две группы: Симптоматические 2. Для базисной терапии астмы используют комбинации противовоспалительных лекарств — ИГКС ( ингаляционные глюкокортикостероиды – Будесонид, Мометазон, Беклазон ) и бронхорасширяющих средств длительного действия (Форадил, Формотерол, Сальметерол). Цель этой группы лекарств — предотвратить обострение симптомов астмы и контроль над заболеванием. Противовоспалительный эффект достигается действием кортикостероидных гормонов на медиаторы воспаления — эозинофилы, цитокины и прочие клетки воспаления. Карманные дозированные ингаляторы — средства доставки лекарственных средств в бронхи. Они специально разработаны для вдыхания лекарственного препарата в виде аэрозоля или пудры. Небулайзеры — это ингаляторы, но стационарные — они средство доставки препаратов в виде суспензий или растворов в бронхи. Применяется при обострении бронхиальной астмы, особенно тяжелом течение. Для успешного лечения важно, принимать все лекарства, которые доктор предписывает. Пациенты должны научиться правильному использованию ингаляторов. Вам, возможно, придется принимать лекарства несколько раз день и при этом отсутствие симптомов не повод самостоятельно вводить коррекции в схему терапии. Наши специалисты уделяют особое внимание правильности использования ингаляторов. Ведь модификаций препаратов для ингаляционной терапии очень много, а мы знаем особенности использования всех препаратов. Пациенту может показаться, что рекомендованный препарат не работает, но это не означает, что он не помогает. При возникновении таких сомнений обратитесь к пульмонологу. Важно знать, что неправильное лечение БА, приводит к изменениям в легких. Некорректный прием лекарств может привести Вас на больничную койку. (анти-лейкотриеновые средства- Монтелукаст и Зафирлукаст). Эти препараты менее эффективны, чем ИГКС, для контроля астмы. Препарат эффективен при атопической форме бронхиальной астмы, а так же пациентов с аспириновой формой астмы и астмой физического усилия. Эти препараты подавляют сужение бронхов в ответ на ингаляцию лейкотриенов, уменьшают астматическую реакцию на холод и физические усилия. Кромоны — кромогликат натрия («Интал») и недокромил («Тайлед»). Эффективность и безопасность современных ингаляционных стероидов, производство новых антилейкотриеновых препаратов привели к вытеснению кромогликата и недокромила из арсенала пульмонологов. Терапия гуманизированными антителами к IgE — Омализумаб. Это моноклональное антитело, которое может связать циркулирующий в крови пациента IgE, оказав выраженное опосредованное влияние на аллергены, снижая воспаление в бронхах. Этот препарат наиболее полезен при тяжелых формах астмы, с эозинофильным воспалением, с неэффективным ответом на терапию ИГКС. Эффективность применения около 30%. Метотрексат и препараты золота – оказывают кортикостероид щадящий эффект при лечении астмы. Однако применение ограничено побочными реакциями. Теофиллины – применяются с середины прошлого века для лечения астмы. Их большое преимущество – это их дешевизна. Поэтому препарат охотно применяется в странах с низким экономическим уровнем. Однако у теофиллина выявлены новые свойства, которые изучаются. И мы увидим возрождение этой группы лекарств. Специфическая иммунотерапия (СИТ или АСИТ). Применяется при доказанной связи между астмой и аллергеном (аллергенами). Одномоментно и опасный способ лечения астмы, но и единственный способ терапии астмы способный дать многолетнюю ремиссию в 70% случаев, при полном трехгодичном цикле лечения. Эффект достигается за счет снижение иммунного ответа на постепенно и периодически повышающиеся дозы вводимого аллергена в организм человека. Получается нечто похожее на прививку от аллергии. У метода много противопоказаний и ограничений. Реабилитация пациентов с бронхиальной астмой Складывается из чёткого соблюдения плана медикаментозного лечения пациентом, обучение контролю над своим состоянием, симптомами астмы. В разработанный индивидуальный план вписывается рекомендации по правильному поведению при обострении болезни. Физические упражнения и тренажеры помогаю сохранить дыхательную мускулатуру в тренированном состоянии, обеспечивая толерантность к физическим нагрузкам, улучшают сердечно-легочную функцию. Регулярные занятия физкультурой сократят тяжесть обострений. Профилактика пациентов с бронхиальной астмой У пациентов астматиков существует представление о том, что если избегать факторов провоцирующих приступы, то медикаментозное лечение не нужно или хотя бы сократить объем лекарственной поддержки. Доказательств на сей счет недостаточно. Но, тем не менее, можно с уверенностью предложить в качестве профилактических мер следующее:
Соляные пещеры или галотерапия безопасный метод профилактики заболеваний верхних и нижних дыхательных путей и психоэмоциональной разгрузки организма. Рассматривать эту методику как лечение астмы не стоит. При прохождении курортного лечения , соляные пещеры полезны. Пациент, болеющий астмой должен регулярно кушать! Нет рекомендаций, подтвержденных клиническими исследованиями о необходимости диеты. Международные исследования доказали, что инициировать астму может избыток потребления соли и фактором риска является ожирение. Если употреблять в пищу меньше соли и следить за калориями, проблем не возникнет. Диета при астме применяется при наличии аллергии на продукты питания. Тут рекомендация одна — исключите эти продукты из рациона и аллергической реакции на них не будет. Так же при наличии ГЭРБ и астмы необходимо соблюдать режим питания, прописанный врачом для профилактики ГЭРБ. Прогноз течения бронхиальной астмы благоприятный. По нашим наблюдениям 70% пациентов» боится «астму, но игнорирует обструктивный бронхит. И это заблуждение т.к. прогноз ХОБЛ трагичней и опасней. Если соблюдать рекомендации врачей астма не будет менять ваш привычный ритм жизни. Бронхиальная астма ожирения, бронхиальная астма с фиксированной нагрузкой, атопическая астма или астма курильщика трудные варианты для лечения. Назначенная терапия не приносит облегчения дыхания и самочувствия. В 10% случаев не обойтись без стационарное лечение , вплоть до отделения реанимации. В чем отличие отделения пульмонологии «ИтеграМедсервис» от других клиник и отделений в лечении бронхиальной астмы? Это мульти дисциплинарный подход к проблеме бронхиальной астмы у каждого конкретного пациента. Ведь астма мульти-факториальная болезнь. К болезни нельзя подходить, просто назначив аэрозольный ингалятор. Владеем всеми способами терапии бронхиальной астмы. Астма школа и реабилитация Н.Н Мещеряковой, популярна в Москве. При выборе схемы лечения врачи оценивают возможные нежелательные эффекты применяемых лекарств и честно обговаривают это с пациентами. Ежегодно обновляем информацию о новых препаратах на конгрессе по проблемам органов дыхания и на Европейском конгрессе по респираторным заболеваниям. Позвоните нам и запишитесь на прием: Тек же у Вас есть возможность обойтись без телефона и записаться онлайн через сайт. Позже, наш диспетчер свяжется с Вами для уточнения деталей приема. Нажимая на кнопку «ЗАПИСАТЬСЯ НА ПРИЕМ», Вы даете свое согласие на обработку ваших персональных данных! источник |
 Снижение концентрации домашнего клеща в доме снижает риск развития БА у ребенка до 8 лет. Но при этом контакт ребенка первого года жизни снижает реакцию на большинство аллергенов и развитие БА в будущем. По данным международных исследований, более десятка обстоятельств регулируют вероятность возникновения БА у детей и взрослых.
Снижение концентрации домашнего клеща в доме снижает риск развития БА у ребенка до 8 лет. Но при этом контакт ребенка первого года жизни снижает реакцию на большинство аллергенов и развитие БА в будущем. По данным международных исследований, более десятка обстоятельств регулируют вероятность возникновения БА у детей и взрослых.