Как контролировать бронхиальную астму?
Представить классификацию БА по уровню контроля, в соответствии с «Глобальной стратегией лечения и профилактики бронхиальной астмы» (GINА, пересмотр 2007 г.).
Контроль над бронхиальной астмой означает устранение проявлений заболевания.
Выделяют критерии контролируемой, частично контролируемой и неконтролируемой бронхиальной астмы.
Необходимо стремиться к тому, чтобы на фоне лечения был полный контроль над астмой, что соответствует критериям контролируемой астмы.
Контролируемая бронхиальная астма – это отсутствие каких-либо ограничений физической активности, ночных пробуждений и, в идеале, дневных симптомов астмы.
Не чаще чем два раза в неделю могут наблюдаться кратковременные эпизоды астмы днем, для купирования которых может требоваться применение ингаляторов, содержащих бронхорасширяющие вещества.
При наличии критериев контролируемой астмы проводимое лечение считается достаточным и его следует продолжить.
При частично контролируемой бронхиальной астме лечение недостаточно эффективно, так как наблюдаются отдельные симптомы астмы, либо ночные, либо дневные (более двух эпизодов в неделю), возможно, с ограничением повседневной активности, может быть снижена пиковая скорость выдоха.
В этой ситуации необходимо выяснить причины и длительность появления симптомов астмы и рассмотреть возможность увеличения объема терапии для достижения лучшего контроля.
При неконтролируемой бронхиальной астме симптомы (кашель, свистящие хрипы, одышка, приступы удушья) обычно наблюдаются у пациента и в дневные, и в ночные часы, зачастую ограничивают повседневную активность, требуют более частого использования ингаляторов, содержащих бронхорасширяющие средства, и сопровождаются снижением показателей пикфлоуметрии.
Если такое ухудшение сохраняется хотя бы неделю, то состояние пациента расценивают как обострение бронхиальной астмы.
Поэтому, при первом появлении признаков неконтролируемой астмы необходимо увеличить дозы, кратность применения и/или количество используемых препаратов, для того чтобы предупредить развитие обострения.
Для оценки контроля над клиническими проявлениями БА используется Тест по контролю над астмой, он подходит для использования взрослыми и детьми старше 12 лет с целью самооценки и может заполняться пациентами перед визитом к лечащему врачу или во время визита.
Этот простой вопросник позволяет улучшить оценку контроля над заболеванием, так как его результаты представляют собой объективные показатели (баллы) и обеспечивает улучшение взаимопонимания между пациентом и врачом.
План самоведения при бронхиальной астме.
Необходимо обучить слушателей принципам составления плана самоведения на основании значений пиковой скорости выдоха и клинических проявлений БА.
План самоведения больных бронхиальной астмой даёт возможность пациенту самостоятельно изменять лечение, в заранее определенных пределах, в зависимости от самочувствия и данных пикфлоуметрии.
Необходимо объяснить пациенту, что четкое соблюдение рекомендаций, обозначенных в плане, может предотвратить обострение заболевания.
Дневник самоконтроля должен содержать следующую информацию:
– перечисление индивидуальных факторов риска обострения астмы, которых больному необходимо избегать;
– индивидуальную ежедневную дозу профилактических препаратов длительного действия;
– инструкцию, как распознать признаки ухудшения состояния, включая симптомы и, если возможно, пиковую скорость выдоха;
– инструкцию, как лечить обострение астмы самостоятельно и когда вызывать скорую медицинскую помощь.
Уровни контроля над астмой
Контролируемая бронхиальная астма (все нижеперечисленное)
Частично контролируемая бронхиальная астма (любое проявление в течение недели)
Неконтролируемая бронхиальная астма
пробуждения
Характеристика Контролируемая Частично Неконтролируемая
Дневные симптомы Нет (дважды контролируемая Более чем дважды в
или менее в неделю неделю
Ночные симптомы Нет Любые
Необходимость в Нет(дважды Более чем Наличие трех или
препарате, снимаю- или менее дважды более признаков
щем симптомы неделю неделю ЧКА в какую-либо
Ограничение Нет(дважды Любые неделю
Функция легких Нормальная ПОСМОТРЕТЬ ЕЩЕ:
Вопрос 1. Как часто на протяжнии последних 4-х недель не позволяла Вам выполнять обычный объем работы в учебном заведении, на работе или дома?
Вопрос 2. Как часто на протяжении последних 4-х недель Вы замечали у себя затруднительное дыхание?
1) чаще, чем 1 раз на день (1 балл);
3) от 3 до 6 раз в неделю (3 балла);
4) 1 или 2 раза в неделю (4 балла);
Как часто на протяжении последних 4 -х недель Вы просыпались ночью или раньше, чем всегда.
Попричине симптомов астмы (свистящее дыхание, затрудненное дыхание, ощющение боли или стиснения в груди)?
1) 4 ночи в неделю и чаще (1 балл);
2) 3-4 ночи в неделю (2 балла);
Как часто на протяжении последних 4-х недель Вы пользовались быстродействующим ингалятором (например, Вентолин, Беротек, Беродуал, Атровент, Сальбутамол, Саламол, Астмопент) или небулайзером (аэрозольным аппаратом) с лекарствами (например, Беротек, Беродуал, Вентолин Небулы)?
1) 3 раза на день и чаще (1 балл);
2) 1 или 2 раза на день (2 балла);
3) 2 или 3 раза в неделю (3 балла);
4) 1 1 раз в неделю или меньше (4 балла);
5) ни одного раза (5 баллов).
Какую оценку Вы бы дали состоянию контроля астмы на протяжении последних 4-х недель?
1) совсем не удавалось контролировать (1 балл);
2) плохо удавалось контролировать (2 балла);
3) в некоторой степени удавалось контролировать (3 балла);
4) хорошо удавалось контролировать (4 балла);
5) полностью удавалось контролировать (5 баллов).
Результатом теста является сумма в баллах, она же используется для формулировки рекомендаций:
— 25 баллов – полный контроль;
— 20-24 балла — астма контролируется хорошо, но не полностью.
Врач может помочь больному добиться полного контроля;
— 19 баллов и меньше – неконтролируемая астма. Возможно, следует изменить терапию для достижения оптимального контроля;
— 14 баллов и меньше – астма у пациента серьезно вышла из-под контроля.
В этом случае пациента следует направить к специалисту.
Date: 2015-11-14; view: 34; Нарушение авторских прав
источник
Неконтролируемая бронхиальная астма, которая характеризуется возникновением приступов удушья, свистящим кашлем и сильной одышкой, как правило, сопровождается ограничением повседневной активности пациента и требует обязательного лечения.
В том случае, когда это состояние остается без изменений даже на фоне проводимого лечения, его классифицируют, как обострение бронхиальной астмы. В соответствии с этим диагнозом при первых проявлениях неконтролируемого заболевания необходимо увеличение дозировки лекарственных препаратов для предупреждения астматического приступа.
Бронхиальная астма характеризуется хроническим течением, что требует обязательного контроля развития симптоматики, которая зависит от индивидуальных особенностей организма и тяжести заболевания.
Астма неконтролируемой, средней и тяжелой степени оценивается по выраженности симптоматики в ночное и дневное время. Кроме того, учитывается потребность в бронхолитиках для лечения острого приступа и возможности заболевания повлиять на активность пациента.
В классификации астмы по уровню контроля можно выделить следующие формы:
К определению уровня контроля необходимо отнестись со всей ответственностью, так как многие астматики не в состоянии самостоятельно оценить степень тяжести заболевания, в результате чего переоценивают возможные результаты лечения.
Кроме того, недостаточно контролируемая форма заболевания способна резко изменить уровень жизни, оказывая воздействие на социальный и психологический статус пациента. Наиболее распространенной формой бронхиальной астмы является персистирующая. При неконтролируемом заболевании возможно внезапное появление астматического приступа, увеличивающего риски развития патологических изменений в организме больного.
Клиническое течение любой формы заболевания зависит от количества дневных и ночных приступов, возникающих в течение недели. На основании этого выбирается интенсивность воздействия β2 -адреномиметиков короткого действия.
- К первой ступени относится астма легкой интермиттирующей степени, проявляющаяся одышкой и нечастым спастическим кашлем. Симптомы интермиттирующей астмы могут отмечаться 1 раз в течение 7 дней, а в ночное время не чаще 1 раза в месяц. Симптомы средней степени в промежутках между приступами практически не наблюдаются.
- Ко второй ступени относится персистирующая легкая астма. Симптомы заболевания возникают не чаще 2 раз в месяц. В ночное время приступы появляются очень редко. В период обострений пациент чувствует дискомфорт, связанный с нарушением привычной деятельности. Постепенно отмечается рост реактивности легочной системы.
- К третьей ступени относится персистирующая форма заболевания средней тяжести. При этом наблюдаются практически ежедневные приступы, которые способствуют снижению качества жизни, нарушая сон и затягивая выздоровление. Эта стадия требует ежедневного приема бета-адреномиметиков короткого действия.
- Четвертое место принадлежит тяжелой, неконтролируемой, форме бронхиальной астмы, течение которой осложняется постоянными болями. При этой форме заболевания осложняется постоянными астматическими приступами, которые могут повторяться несколько раз за ночь и требуют дополнительного приема бронхолитиков.
Необходимо отметить, что степень развития тяжести заболевания, опираясь только на симптоматику, можно выяснить только до начала лечебных мероприятий. При получении надлежащей терапии рекомендуется учитывать степень ее интенсивности.
Неконтролируемое течение заболевания предусматривает выбор наиболее эффективных препаратов, к которым относятся и комбинированные средства, например ингаляционный препарат Беродуал. Входящие в его состав Фенотерол и Ипратропия бромид обладают способностью расслабления бронхиальной мускулатуры, обеспечив тем самым максимально быстрое и пролонгированное действие.
Нередко применяются синтезированные симпатомиметики, которые избирательно стимулируют β – адренорецепторы. К ним относятся Новодрин, Эуспиран, Изадрин, Астмопент и т.д. Избирательное свойство позволяет избежать побочных воздействий, которые отмечаются при использовании Адреналина. Эти препараты чаще всего применяются ингаляционно, что позволяет добиться быстрого купирования приступа. Однако при передозировке ингаляций (4-6 раз в течение суток) способен возникнуть воспалительный процесс дыхательных путей и бронхоспазмы.
Острая симптоматика может купироваться при помощи Эуфиллина в таблетированной форме или растворе для внутримышечного и внутривенного введения, в зависимости от состояния пациента. Пероральный прием Эуфиллина(0,15 г) можно совмещать с (0,025 г) Эфедрина гидрохлоридом. Кроме того, независимо от стадии заболевания, рекомендуется прием увлажненного кислорода.
При выборе лечебной тактики необходимо учитывать возможные осложнения. От этого зависит увеличение или снижение потребности в лекарственных препаратах для купирования острого приступа. Увеличение дозировки противоастматических препаратов (более 2 раз в течение 7 дней) указывает на потерю контроля над бронхиальной астмой, что требует пересмотра базисного лечения в дальнейшем.
Состояние пациента, в зависимости от степени тяжести симптоматики, необходимо проводить регулярно. Для контроля над тяжестью состояния следует оценить такие показатели, как показатели диагностических обследований и лабораторных анализов.
Важно проводить мониторинг состояния больного для того, чтобы оценить эффективность проводимого лечения. При необходимости проводится коррекция терапии, предполагающая « ступенчатую» систему назначений. При этом интенсивность медикаментозной терапии зависит от тяжести симптоматики.
Такая система наиболее оптимальна и позволяет достигнуть контроля над бронхиальной астмой при минимальном лекарственном воздействии и длительно его поддерживать. При этом необходимо учитывать индивидуальные особенности организма и тяжесть симптоматики.
Достижение полного контроля над бронхиальной астмой должно характеризоваться не только отсутствием симптомов заболевания и нормализацией легочной функции. В этом состоянии необходимо следить за тем, чтобы в нижних отделах дыхательных путей отсутствовали воспалительные процессы, так как они способны привести к бронхиальной гиперреактивности.
В том случае, когда астма находится под контролем, пациент может вести привычный образ жизни, занимаясь спортом, посещая учебные заведения и занимаясь профессиональной деятельностью. При этом нормализуется сон, и предупреждается развитие новых приступов и обострений.
Профилактические мероприятия по предупреждению развития острого приступа бронхиальной астмы заключается в соблюдении следующих условий:
- Важно избегать прямого контакта с аллергенами, так как наиболее часто заболевание связано с повышенной аллергической чувствительностью организма.
- Рекомендуется в холодное время года защищать дыхательные пути и дышать только через нос. Это позволит избежать переохлаждения и, как результата, воспалительных заболеваний дыхательных путей.
- Необходимо регулярно проводить мониторинг заболевания по степени тяжести. Если оно осложняется присоединением вторичных инфекций, необходимо обратиться к лечащему врачу для дальнейшего лечения.
- Рекомендуется соблюдать гипоаллергенную диету, особенно при наследственной предрасположенности к аллергическим проявлениям.
- Своевременного предупреждение астматического приступа можно добиться с помощью аэрозольного ингалятора, который необходимо всегда иметь с собой.
Важно помнить, что нельзя заниматься самолечением, так как иногда это может привести к тяжелым осложнениям, а в некоторых случаях и к летальному исходу. При первых признаках заболевания следует незамедлительно обратиться к лечащему врачу для получения высококвалифицированной консультации и лечебных рекомендаций.
источник
Бронхиальная астма (БА) и хроническая обструктивная болезнь легких (ХОБЛ) – два наиболее распространенных респираторных неинфекционных заболевания легких в практике пульмотерапии. Помимо того, что БА и ХОБЛ имеют некоторые общие клинические признаки, возможны случаи их сочетания. Хотя эти заболевания самостоятельные и не переходят друг в друга, но нередки случаи формирования ХОБЛ у больных БА и возникновение приступов астмы у больных хронической обструктивной болезнью легких. Надо полагать, при определенных обстоятельствах неконтролируемая бронхиальная астма может стать зоной риска ХОБЛ, а у больных ХОБЛ могут возникать приступы астмы. Сочетание БА и ХОБЛ, схожесть симптомов, формирование одной болезни по причине другой, создают определенные клинические трудности в практике врачевания, что и явилось поводом публикации настоящей статьи.
Целью публикации является, во-первых, довести до врачей первого звена ранние признаки формирования ХОБЛ у больных бронхиальной астмой; во-вторых, привлечь внимание руководителей медицинских учебных заведений на необходимость включения в программу усовершенствования семейных врачей, терапевтов, пульмонологов, педиатров циклов усовершенствования, по темам: «Алгоритмы ранней диагностики и лечения ХОБЛ больных с неконтролируемой астмой»; «Отличительные черты приступов астмы у больных ХОБЛ».
Эпидемиология сочетанного заболевания БА и ХОБЛ недостаточно изучена, но многие клиницисты уже обратили внимание на клиническую значимость проблемы. Авторы 1 публикации статьи «Сочетание астмы и ХОБЛ…» приводят цифры косвенных наблюдений сочетания БА и ХОБЛ, по частоте тяжелой астмы, больных резистентных к стандартным средствам, с нарастающими признаками дыхательной недостаточности и формированием легочного сердца – от 10 % до 25 %. По нашим данным практики спелеотерапии больных БА, за период 2005–2013 гг. (1658 больных), процент больных астмой с осложнением ХОБЛ равен проценту больных, трудно контролируемой астмой (40–60 %). Мы считаем, что это не случайное сочетание, но причиной ХОБЛ у больных БА, как и причиной приступов астмы у больных ХОБЛ, является некорректное врачевание. Такой вывод вытекает из результатов ретроспективного анализа медицинской документации контроля БА и ХОБЛ на местах. Эта проблема актуальна как для врачей первого звена – семейных и/или врачей поликлиник, так и для клинической респираторной медицины вообще.
На рисунке отображено соотношение количества больных БА по областям РА и процент больных, прошедших курс спелеотерапевтической рекреации. Наибольшее число от общего числа больных астмой поступило из Котайской области – 57,4 %, чуть меньше из Еревана – 47,4 %. Наименьшее число – из Лори – 12,0 %, Гегаркуника 16,3 % и Тавуша – 17,2 %. Из других областей поступило примерно одинаковое число – около 22 %, с разбросом до 3 %. Причин такого разброса много, от недостаточной информированности до финансовых возможностей больных той или другой области, но основной причиной, на наш взгляд, является уровень медицинской культуры на местах, как больных, так и врачей. Медицинская культура является основной причиной и тому, что все больные БА в прошлом принимали некорректное, а зачастую противопоказанное лечение. В Центр Астмы больные поступали после долгих лет мытарства. У большинства (более 60 % от общего числа поступивших на) формировалась хроническая обструктивная болезнь легких.
За период с 2005 по 2013 годы из 5552 больных БА, зарегистрированных в отчетах МЗ, только 1658 прошли курс рекреации в «Спелеотерапевтическом Центре». Все зарегистрированные больные находятся под контролем врачей центра. В результате ретроспективного анализа медицинских документов больных, поступивших на спелеотерапию установлено, что подавляющее большинство больных не обследовалось и/или нерегулярно контролировались. Больные обращались за медицинской помощью в различные медицинские центры, и только в случаях обострения астмы где, с легкой руки рентгенолога, диагностировали пневмонию. «Закономерно» больные принимали антибиотики, нестероидные противовоспалительные препараты, жаропонижающие и другое противоинфекционное лечение. Именно такое некорректное лечение способствовало формированию ХОБЛ. Нестероидные противовоспалительные препараты в настоящее время не рекомендуются ни при ХОБЛ, ни при бронхиальной астме. Более того, при аспириновом варианте БА, НПВП опасны для жизни. Предотвращение опасных для жизни деструктивных изменений в легких практически сводится к профилактике ХОБЛ.
Пример: больной Ваган, 1965 года рождения, в семейном анамнезе есть больные аллергией. Работает торговцем стройматериалов. Двадцать лет курит. Содержит канареек. Считает себя больным бронхиальной астмой около 10 лет. Ранее, вне приступа астмы, проблем с дыханием не было. Болезнь формировалась постепенно. В прошлом, во время ремиссии, чувствовал себя практически здоровым, а в последние 2–3 года, всплески нарушения дыхания сопровождаются признаками воспаления легких, по поводу чего принимал антибиотики, жаропонижающие, народные средства. Однако лечение было малоэффективным, более того, после каждого курса лечения симптомы нарушения дыхания нарастали, а в последнее время появилась одышка от привычной физической нагрузки. К сожалению, больному не проводились исследования функции внешнего дыхания, и не потому, что не было такой возможности, но потому, что врачу все было ясно: «У больного бронхиальная астма, пневмония, или ОРВИ». Неоднократно делали рентген-исследования, каждый раз диагностировали пневмонию.
Эта пагубная практика имеет место во всем мире. По этой причине 14 октября с 2010 года Международными Медицинскими организациями и ВОЗ объявлено Всемирным днем спирометрии, с целью привлечь внимание врачей, медицинских работников и больных зоны риска, ранней диагностике ХОБЛ. Надо заметить, что в любом медицинском учреждении на уровне первого звена медицинской помощи врач-ординатор (семейный врач) может путем не инвазивного метода спирометрии оценить состояние легких на данный момент. Спирометрия рекомендуется всем лицам:
● с многолетним стажем курения,
● вынужденным дышать загрязненным воздухом, на вредном производстве,
● с частым и длительным кашлем, после ОРВИ и/или простудного заболевания,
● с затруднением дыхания при быстрой ходьбе,
● с ощущением заложенности и/или хрипов в груди,
● страдающим частыми обострениями бронхита,
● обеспокоенным состоянием лёгких и/или имеет отягощенную наследственность,
● страдающим хроническими заболеваниями легких – БА, ХОБЛ, др.
Задачи настоящей работы: на материале клинических наблюдений разработать «Дорожную карту»2 диагностики, лечения и профилактики ХОБЛ и больных БА на уровне врача первой медицинской помощи. При этом критерием диагностики ХОБЛ у больных БА может считаться сниженный объем форсированного выдоха за первую секунду (ОФВ1), на фоне базового медикаментозного контроля астмы, при малой вариабельности пиковой объемной скорости выдоха. Не менее важным критерием дифференциации является одышка вне приступа астмы и отсутствие эффекта стероидной терапии.
источник
Выделяют контролируемую, частично контролируемую и неконтролируемую бронхиальную астму. Среди наиболее распространенных заболеваний хронического характера, присущих людям, бронхиальная астма занимает одну из ведущих позиций. Одной из сложнейших ее форм является неконтролируемая бронхиальная астма.
Бронхиальная астма (БА) представляет собой воспалительное заболевание, развивающееся в дыхательных путях. Оно отличается участием в воспалительном процессе разнообразных клеточных элементов и хронической природой. Это заболевание может проявиться у представителей любой национальности и пола, в любом возрасте. Согласно статистическим данным, этой болезнью страдает около 300 миллионов людей на планете.
Что же обозначает определение «неконтролируемая бронхиальная астма»? Это такое течение болезни, при котором отсутствует контроль над его симптоматикой. Еще не так давно специалисты использовали критерии оптимального контроля над этим заболеванием. Однако на практике они оказывались слишком расплывчатыми, тем самым не позволяя доподлинно определить степень контроля и своевременно перейти на следующую ступень с подходящим объемом терапии.

- не наблюдается обострений;
- определение минимального числа эпизодов бронхообструкции в течение дня;
- ночные симптомы полностью отсутствуют;
- больному требуется лишь одна ингаляция за сутки b2-агонистов короткого действия;
- значение ПСВ в среднем за сутки выше 80%;
- при терапии не наблюдается побочных эффектов;
- в течение суток показатель лабильности бронхов не превышает 20%.
На сегодня создана и активно применяется трехуровневая система определения контроля симптомов бронхиальной астмы. При этом указанный перечень относится ко второму уровню контролируемости.
Бронхиальная астма часто переходит в тяжелые формы. Это приводит к тому, что человек становится инвалидом, а при дальнейшем неоказании адекватной медицинской помощи — к ХОБ. Эта необратимая стадия проявляется в форме хронической инструктивной болезни легких. Лечение неконтролируемой бронхиальной астмы проводится гораздо дольше и с малой эффективностью. Это не только влияет на пациента, но и вызывает большие затраты времени и усилий врача.

В большинстве случаев пациенты подвергаются неадекватной терапии бронхиальной астмы, вследствие чего наблюдается отсутствие контроля. Впрочем, ряд типов неконтролируемой бронхиальной астмы получили отдельные названия из-за особенностей их формирования. Сложная, или как ее еще называют, терапевтически резистентная бронхиальная астма нередко определяется как неконтролируемая. Она не реагирует на оптимальную терапию. Также выделяют ряд разновидностей сложной астмы:
- Хроническая сложная — отличается постоянной бронхообструкцией. Она сильно влияет на качество жизни человека. При ней крайне важна системная терапия с применением кортикостероидов, имеющих неполный эффект. Однако тяжелые обострения наблюдаются нечасто.
- Хрупкая, также ее часто называют нестабильной. Существует в двух вариантах. В первом применяются высокие дозы ингаляционных кортикостероидов и наблюдается высокая вариабельность ПСВ. Вторая форма — интерпретирующая тяжелая бронхиальная астма. Она обладает внезапными острыми приступами, которые развиваются на протяжении 3 часов, при этом не имея объективной причины. Наблюдается практически нормальная функция легких.
- Фатальная форма — это обострение, угрожающее смертью или приводящее к летальному исходу. Его яркими признаками и одновременно обострениями являются пневмоторакс, гиперкапния или респираторный ацидоз. При нем крайне важно скорейшее применение реанимационных мероприятий.
Существует и ряд других форм неконтролируемых БА. Как показывает практика, под неконтролируемый тип этой болезни могут подпадать случаи любой степени тяжести.
Чтобы назначить адекватное лечение, для начала следует в каждом случае тщательно изучить причину, по которой возникло это состояние. Врач должен быть уверен в том, что диагноз «бронхиальная астма» верен. Нередко его сложно отличить от ХОБЛ. В таких случаях очень важно наблюдение за состоянием больного в динамике. Диагностику могут затруднять разнообразные патологии верхних дыхательных путей.
Часто бывает, что из-за недостаточной квалификации специалиста или его невнимательности назначается неадекватная базисная терапия. Это происходит и в случае, когда он недооценивает степень тяжести состояния больного. Иногда и сам пациент является причиной развития этого типа бронхиальной астмы: частично или полностью отказывается от назначенной врачом терапии, не соблюдает режим и т. п.
Причины отсутствия контроля над симптомами заболевания могут скрываться и в индивидуальных особенностях организма пациента: к примеру, наследственная склонность к развитию воспалений или бронхиальная гиперактивность неуправляемого характера. Зачастую применяется комбинированная терапия для лечения рассматриваемого типа БС. При этом выделяют такие ее этапы:
- приведение к ремиссии;
- переход на более щадящий тип терапии;
- произведение комплекса действий для поддержания состояния ремиссии.
На первом этапе важно максимально подавить воспаление, поскольку именно оно выступает ведущим патогенетическим механизмом этого заболевания. Начальная доза препаратов базовой терапии определяется врачом на основании тяжести течения заболевания. Период лечения на этом этапе может достигать полугода. Минимальный срок терапии — месяц.
После прохождения этого этапа начинается уменьшение дозы препаратов до такой, которая будет обеспечивать контроль над симптоматикой болезни и при этом будет минимальной. Коррекция объемов терапии проводится строго индивидуально и продолжается до полугода, но не меньше трех месяцев. В зависимости от успешности второго этапа принимается решение о начале третьего. Назначается комплекс препаратов и мер (в ряде случаев определенный препарат), направленный на сохранение состояния ремиссии.
С учетом широкого спектра действующих препаратов их подбор возможен лишь лечащим врачом исходя из индивидуальных особенностей пациента и течения болезни. Наличие симптоматики, свидетельствующей о развитии заболевания или его обострения, в частности, удушья, — это серьезный повод для срочного обращения к врачу.
Бронхиальная астма — смертельно опасное заболевание, подлежащие обязательному лечению с привлечением специалистов!
При неконтролируемой бронхиальной астме признаки обычно наблюдаются у пациента в дневные и ночные часы, ограничивают повседневную активность, требуют более частого использования ингаляторов. Если такое ухудшение сохраняется хотя бы неделю, состояние пациента расценивают как обострение бронхиальной астмы. При первом появлении признаков неконтролируемой астмы необходимо увеличить дозы, кратность применения или количество используемых препаратов для того, чтобы предупредить развитие обострения.
источник
В современной медицине классификация все больше становится прикладным инструментом, позволяющим достичь главной цели – избавить пациента от болезни или как можно сильнее уменьшить ее проявления с помощью лечения. Таким образом, деление заболевания на варианты, формы, степени во многом становится условным. В ходе лечения нередко один вариант заболевания сменяется другим, отличие которого заключается прежде всего в ином лечении.
Бронхиальная астма не стала исключением. Если в прежние годы врачи выделяли степени тяжести болезни, то в последней редакции всех отечественных и зарубежных руководств внимание переместилось на степень контроля заболевания, то есть на интенсивность и эффект лечения.
Классификация по степени тяжести сохраняет свое значение при первом визите пациента к врачу, когда он еще не получает никакого лечения, особенно ингаляционных глюкокортикоидов и других средств базисной терапии.
Классификация по степени тяжести определяет, насколько поражено бронхиальное дерево. Она помогает определить, какие препараты следует назначить и в какой дозировке, чтобы в дальнейшем добиться устранения симптомов болезни. Это деление проводится исключительно до начала лечения.
Тяжесть течения оценивается по наличию клинических проявлений в сочетании с показателями функции внешнего дыхания (ФВД), прежде всего объема форсированного выдоха за 1 секунду (ОФВ1) и пиковой скорости выдоха (ПСВ).
- Интермиттирующее течение, или I ступень, характеризуется нечастыми признаками (кашель, одышка), беспокоящими больного реже 1 раза в 7 дней и до 2 раз в месяц ночью; данные ФВД близки к нормальным.
- Астма легкой степени, или II ступени, сопровождается более частым появлением клинических признаков: днем чаще раза в 7 дней, но не ежедневно, ночью – чаще 2 раз в месяц. При обострении болезни может быть нарушен сон и снижена активность больного. Данные ФВД при этом остаются близкими к нормальным.
- Средняя степень (III ступень) сопровождается ежедневными проявлениями, ночью симптомы возникают раз в 7 дней и чаще. Пациент вынужден ежедневно пользоваться препаратами «скорой помощи» (сальбутамол) для устранения кашля или удушья. Функция внешнего дыхания ухудшается.
- Тяжелое течение (IV ступень) сопровождается ежедневными приступами и частыми симптомами в ночные часы. Заболевание протекает с частыми обострениями, во время которых ограничивается физическая активность пациента. Показатели ФВД меньше 60% от должных величин.
Если клиническая картина и данные спирометрии не совпадают, степень тяжести устанавливают согласно более тяжелым признакам.
Тяжесть заболевания можно охарактеризовать и у больных, уже получающих лечение. В этом случае легким считается течение болезни, которое можно контролировать с помощью небольшого количества лекарств и низких дозировок. Тяжелая астма в этом случае – состояние, требующее назначения комплексной терапии в больших дозах. Плюсом этой классификации является учет получаемой больным терапии, дающей представление об истинной тяжести болезни.
Таким образом, у больного с исходной IV степенью тяжести болезни на фоне лечения мы можем добиться такого контроля над астмой, что у него вообще не будет приступов ночью, а днем он лишь иногда будет пользоваться, например, сальбутамолом. Однако получится это у врача только при назначении соответствующей комбинированной базисной терапии, что соответствует астме тяжелого течения.
Задача врача при бронхиальной астме у пациента – добиться контроля заболевания, то есть предотвращения ее проявлений. Полное излечение при этом заболевании считается невозможным. Оценив на первом приеме тяжесть состояния пациента, врач назначает ему лекарственную терапию. В процессе дальнейшего наблюдения он оценивает уже не степень тяжести, а уровень контроля над заболеванием, при необходимости изменяя лечение.
Для оценки уровня контроля используются разнообразные опросники. Их можно применять начиная с возраста пациента 4 года. Для взрослых наиболее распространен «Тест контроля над астмой». Если при ответе на все вопросы сумма составила 25 баллов – контроль хороший;20 – 24 балла – недостаточный; менее 20 баллов – результат плохой, нужно срочно обратиться к врачу. Для детей создан детский вариант теста: если ребенок набрал 19 баллов и меньше – это говорит о плохом контроле над заболеванием.
На необходимость усиления терапии указывает частое использование средств «скорой помощи» (например, сальбутамола). При этом следует увеличить объем терапии до достижения контроля над признаками болезни. Если состояние полного контроля сохраняется более 3 месяцев, можно попробовать уменьшить интенсивность лечения до минимальных поддерживающих доз.
Различают три уровня контроля над болезнью:
- контролируемая астма;
- частично контролируемая;
- неконтролируемая.
При полностью контролируемой патологии в течение как минимум месяца:
- регистрируется меньше двух эпизодов ухудшения в неделю;
- ночные пробуждения из-за симптомов болезни отсутствуют;
- физическая активность не ограничена;
- необходимость пользоваться препаратами «скорой помощи» отсутствует или есть, но не чаще двух раз в неделю;
- ФВД в пределах нормы (для детей старше 5 лет).
При частично контролируемом течении болезни хотя бы один из перечисленных показателей наблюдается чаще или выражен сильнее. Показатели ФВД меньше 80% от нормы или наилучшего известного для данного пациента показателя.
При неконтролируемой патологии могут наблюдаться три и более из следующих признаков:
- более двух эпизодов ухудшения самочувствия в неделю;
- любые ночные симптомы;
- любое ограничение активности;
- потребность в препаратах «скорой помощи» чаще 2 раз в неделю;
- ФВД менее 80% от нормы.
Кроме того, учитывается риск осложнений. Он увеличивается при плохом контроле, частые обострения, госпитализация в отделение интенсивной терапии по поводу этой патологии, низкий показатель ОФВ1, курение, необходимость приема лекарств в большой дозировке.
Под обострением понимается 7 и более дней неконтролируемого течения болезни.
Некоторые пациенты считают, что частые приступы удушья, ежедневная потребность в ингаляциях сальбутамола, одышка – признаки тяжелого течения патологии. Однако такое мнение не совсем верно. Это признаки неконтролируемого течения заболевания, которое может быть как при тяжелой, так и при легкой астме.
С чем может быть связана невозможность полного контроля над болезнью? Прежде всего, необходимо узнать, насколько пациент выполняет требования по элиминации аллергенов, правильно ли он проводит ингаляции, выполняет ли все назначения врача. Затем нужно устранить провоцирующие факторы – гастроэзофагеально-рефлюксную болезнь, синуситы, хронический ринит. Примерно у четверти больных безуспешность терапии связана с неправильно поставленным диагнозом, когда за астму принимается другое заболевание. Если же все эти факторы устранены, нужно усилить терапию.
Однако у части пациентов, несмотря на интенсивное лечение, добиться полной ремиссии не удается. Чаще всего это связано с генетическими и анатомическими особенностями – изменчивостью рецепторов к интерлейкинам, смешанным типом воспаления, наличием внутриклеточных возбудителей, более толстой стенкой бронхов и другими особенностями. Изучение таких вариантов продолжается, оно позволит в будущем создать новые препараты для помощи людям с тяжелой неконтролируемой бронхиальной астмой.
источник
Дыхательная система, как и другие органы человека, подвержена интенсивному воздействию внутренних и внешних негативных факторов. При определенных условиях это может привести к возникновению бронхиальной астмы.
Наиболее опасной формой заболевания считается неконтролируемая астма. По статистике, она развивается у 20% населения.
Данную патологию вылечить полностью нельзя, но существует способы, позволяющие добиться полного или частичного контроля над течением заболевания, что позволит больному вести полноценный образ жизни.
Бронхиальная астма — распространенное заболевание нижних дыхательных путей с непосредственным участием клеточных элементов. Оно характеризуется гиперреактивностью бронхов, на что организм отвечает сужением их просвета.
При этом отмечается бронхоспазм, отек слизистой оболочки, скопление большого количества мокроты и как следствие, нарушение газообмена и возникновение приступов удушья.
Контролирование состояния больного в большинстве случаев позволяет снизить риск обострения болезни и развития астматического статуса.
Заболевание классифицируется не только по степени тяжести, особенностям протекания, наличию[М9] осложнений, но также по степени контроля.
Он определяется по следующим параметрам:
- симптоматические проявления болезни в разное время суток;
- ограничение активности;
- функциональное состояние дыхательной системы;
- частота астматических приступов;
- необходимость применения медикаментозных препаратов неотложной помощи.
Существуют три вида астмы, отличающиеся по степени контроля:
- Контролируемая бронхиальная астма — наблюдается отсутствие клинических проявлений в период лечения. Показатели диагностических исследований соответствуют норме. Препараты при контролируемой форме назначаются пациентам в минимальном количестве.
- Частично контролируемая — отмечается наличие отдельных симптомов заболевания. В этом случае рекомендуется смена терапевтических мероприятий для возвращения болезни в контролируемую форму.
- Неконтролируемая бронхиальная астма — наиболее опасная форма заболевания, при которой наблюдается ярко выраженная симптоматика и частые обострения с астматическими приступами, повторяющимися неоднократно в течение недели. В этот период требуется приложить все усилия для возврата болезни в контролируемую форму.
Контроль болезни заключается в продолжительном наблюдении за ее развитием (сопутствующие признаки, частота повторений приступов) и подборе индивидуального лечения. Комплексная терапия способна перевести болезнь в состояние длительной ремиссии.
Причинами развития неконтролируемой астмы являются:
- наследственная предрасположенность;
- неподходящие климатические условия;
- работа, связанная с воздействием химически активных веществ;
- ожирение;
- гормональные нарушения;
- особенности строения дыхательных органов;
- не полностью вылеченные инфекционные заболевания;
- ослабление иммунитета.
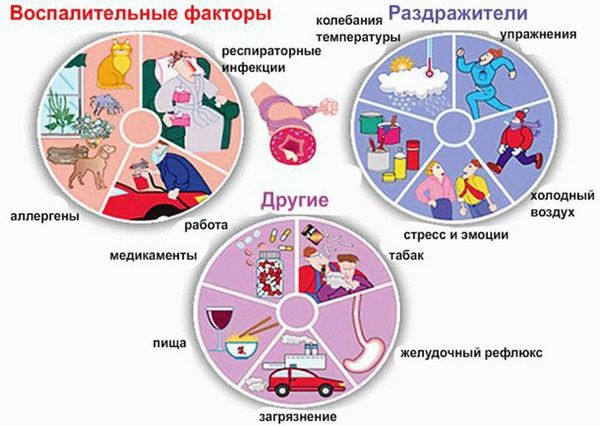
Триггерами (провоцирующими факторами), запускающими патологические процессы в организме и приводящими к обострению хронического заболевания, могут быть:
- лекарственные препараты;
- продукты питания;
- средства бытовой и строительной химии;
- пух и шерсть домашних питомцев;
- сухие корма для животных;
- домашняя пыль.
Астма может развиваться под влиянием одной или нескольких причин, но клинические проявления заболевания от этого не изменяются.
Для болезни характерна следующая симптоматика:
- спазм гладкой мускулатуры бронхов;
- нарушение дыхания (свистящее, хриплое, затрудненное);
- появление одышки;
- большое количество отделяемой слизи;
- возникновение приступов кашля.
При неконтролируемой астме возникает удушье, которое способно привести к летальному исходу. Чтобы избежать этого, необходимо своевременно обратиться к врачу и пройти назначенное обследование (для определения степени тяжести болезни, подбора соответствующего лечения и восстановления контроля над бронхиальной астмой).
Основные цели лечения астмы:
- уменьшить чувствительность к влиянию провоцирующих факторов;
- получить полный контроль над астмой;
- снизить частоту обострений;
- предотвратить состояния, угрожающие жизни больного;
- нормализовать дыхательные процессы;
- снизить потребность в лекарствах.
Одним из методов борьбы с бронхиальной астмой является базисная терапия.
Она включает применение следующих препаратов:
- кортикостероидов (в форме аэрозолей), способствующих купированию воспалительных процессов в дыхательных путях;
- бронхолитиков, улучшающих отхождение слизи;
- антихолинергических средств (при большом скоплении мокроты и ее плохом отхождении), вызывающих расширение бронхов, уменьшающих одышку и кашель;
- бета-2-адреномиметиков длительного и короткого действия, предупреждающих обструкцию бронхиальных ветвей, способствуют их расширению;
- системных глюкокортикостероидов, использующихся в качестве поддерживающей терапии и во время астматических приступов.
Лекарства данных групп применяются в течение продолжительного времени. Они способны приостановить процесс развития астмы, уменьшить ее проявления и снизить вероятность обострений.
Прием лекарственных препаратов корректируется в индивидуальном порядке (в зависимости от состояния пациента и проявления клинических признаков).
- соблюдать спокойствие;
- снять все, что мешает свободному дыханию;
- принять положение сидя или стоя, упереться руками, локти отвести в сторону;
- использовать ингалятор.
Если приступ невозможно снять самостоятельно, необходимо вызвать скорую помощь.
Лечение считается успешным, если астма взята под контроль,
Эффективность проведенной терапии оценивается по следующим критериям:
- не отмечается появления побочных действий от назначенных препаратов;
- нету обострений и отсутствует выраженная симптоматика болезни;
- не требуется приема препаратов быстрого действия;
- отмечается стабильное снижение дозировки принимаемых лекарств;
- стабилизируется дыхательная функция;
- улучшается общее состояние пациента в покое и при физических нагрузках.
Контролированная форма бронхиальной астмы — показатель успеха проведенной терапии.
При неконтролируемом течении заболевания увеличивается риск возникновения осложнений. Частые обострения приводят к нарушению газообмена (воздух поступает в легкие в недостаточном объеме).
Астма может стать толчком к развитию вторичных инфекций (пневмонии, гнойного бронхита), а также:
- эмфиземы (раздувание) легких — приводит к дыхательной недостаточности;
- дыхательной недостаточности;
- пневмоторакса — скопления воздуха в плевральной полости;
- ателектаза – спадения легкого из-за частичного или полного закрытия просвета бронхов;
- астматического статуса — тяжелого угрожающего жизни состояния, которое возникает в результате длительного приступа.
Неконтролируемая астма может привести к необратимым последствиям — инвалидности и даже смерти.
Чтобы уменьшить влияние неконтролируемой бронхиальной астмы на качество жизни человека, необходимо придерживаться некоторых рекомендаций:
- избегать тяжелых физических нагрузок;
- укреплять защитные силы организма;
- исключить воздействие аллергенов, способных вызвать обострение заболевания;
- контролировать эмоциональное состояние;
- не злоупотреблять алкоголем;
- избегать курения и вдыхания сигаретного дыма;
- использовать ингалятор в период обострения;
- проходить регулярные осмотры у пульмонолога, аллерголога и других специалистов.
Следует помнить, что бронхиальная астма нуждается в постоянном контроле. Каждый человек, страдающий астмой, должен иметь при себе ингалятор, который поможет в критической ситуации облегчить состояние и не допустить развития астматического статуса.
источник
Неконтролируемая бронхиальная астма — патология, при которой приступы удушья, сильная одышка и свистящий кашель сопровождаются ограничением повседневной активности. Такое состояние обязательно требует грамотного лечения, иначе может наступить летальный исход.
Внимание! При первых проявлениях данной патологии нужно повысить дозу лекарств.
Неконтролируемая экзогенная, эндогенная и смешанная бронхиальная астма развивается по следующим причинам
- неподходящий климат;
- специфическое строение органов дыхания;
- наследственная предрасположенность;
- лишние килограммы;
- нарушения гормонального характера;
- невылеченная инфекционная болезнь;
- слабая иммунная система;
- деятельность, которая связана с влиянием химически активных веществ.
И частично контролируемая, и полностью неконтролируемая БА может обостриться в результате воздействия таких факторов, как продукты питания, пыль, медикаменты, чистящие средства, строительные составы, шерсть и пух домашних животных, сухие корма для питомцев. Важно не допускать с ними контакта.
Внимание! Бронхиальная астма может развиться под воздействием одного либо сразу нескольких факторов. Симптоматика от этого не изменяется.
К основным симптомам БА относятся:
- одышка;
- спазм гладкой мускулатуры бронхов;
- сложное дыхание;
- хрипы и свист при выдыхании воздуха;
- много отделяемой слизи;
- сильные приступы кашля.
Внимание! Нужно своевременно обратиться к доктору. Он назначит необходимые анализы и обследования. По их результатам разрабатывается план лечения.
Очень важен самоконтроль при той или иной бронхиальной астме. Если этого не делать, то могут возникнуть серьёзные осложнения. Систематические обострения способствуют сбою газообмена — состояние, при котором в лёгкие поступает мало воздуха.
БА может привести к формированию вторичных инфекций (гнойный бронхит, пневмония). Также иногда возникают следующие патологические состояния: недостаточность дыхательная, раздувание лёгких, пневмоторакс, астматический статус, ателектаз.
Внимание! У отдельных пациентов неконтролируемая астма приводит к инвалидности. Поэтому крайне важно следить за своим состоянием.
Грамотная базисная терапия позволяет сократить чувствительность к воздействию факторов, которые провоцируют развитие патологии. Также удаётся уменьшить частоту обострений, получить контроль над болезнью, нормализовать дыхательные процессы, предотвратить состояния, которые угрожают жизни, и сократить нужду в препаратах.
Данное лечение предусматривает приём таких медикаментов, как кортикостероиды, бронхолитики, антихолинергические средства, бета-2-адреномиметики короткого и продолжительного действия, глюкокортикостероиды системные. Препараты нужно употреблять на протяжении продолжительного временного интервала. Они приостанавливают процесс развития заболевания, сокращают его проявления и минимизируют риск развития осложнений.
Доза лекарств устанавливается в каждом конкретном случае персонально. Во внимание принимается общее самочувствие больного.
При наступлении приступа нужно успокоиться, снять одежду, которая сдавливает горло и грудную клетку. Необходимо занять положение стоя либо сидя.
Внимание! Если снять приступ самостоятельно не удаётся, нужно вызвать скорую помощь. Малейшее промедление может стоить жизни.
Подходящее лечение позволяет взять под контроль любой тип бронхиальной астмы. Результативность терапии оценивается по таким параметрам.
- Дыхание стабильное, без хрипов и свистов.
- От принимаемых препаратов не возникают побочные явления.
- Симптоматика проявляется вяло.
- Не происходят обострения.
- Не возникает необходимости в употреблении лекарств быстрого действия.
- Можно уменьшать дозу применяемых препаратов.
- Общее состояние улучшается, повышается качество жизни.
В целях уменьшения воздействия неконтролируемой БА на качество жизни пациента нужно соблюдать такие советы:
- отказаться от спиртных напитков;
- не допускать серьёзных физических нагрузок;
- укреплять иммунитет;
- не допускать влияния аллергенов;
- следить за психическим здоровьем;
- не курить и стараться не вдыхать сигаретный дым;
- систематически посещать аллерголога, пульмонолога и иных специалистов.
Внимание! Пациент всегда должен иметь при себе ингалятор. В экстренной ситуации он поможет облегчить состояние и убережёт от возникновения астматического статуса.
Пожалуйста, поделитесь этой статьёй в социальных сетях. Так ещё больше людей узнает о том, что такое неконтролируемая астма и как с ней справляться.
источник
Бронхиальная астма – наиболее распространенное заболевание среди всех известных хронических болезней. Причем коэффициент смертности вследствие бронхиального недуга из года в год не уменьшается. Ведь качество диагностирования и терапии данного заболевания за последнее десятилетие значительно улучшилось. Поэтому перед современной медициной стоит важная задача. Нужно адекватно оценивать и контролировать симптоматику пациентов, которым оказывается базисная медицинская помощь.
С целью определения уровня эффективности терапии бронхиальной астмы в США и Европе проводились специальные исследования. Результаты показали, что практически у 70% астматиков симптоматика бронхиальной астмы является неконтролируемой. В большей степени это связанно с тем, что медики недооценивают степень тяжести заболевания, а пациенты считают любое лечение удачным.
В конце 90-х годов прошлого века E. Bateman разработал критерии «хорошо контролируемой» бронхиальной астмы. Это дало толчок для новых разработок и стратегий лечения пациентов. Данные критерии помогают сделать течение болезни более бессимптомным и оптимально контролировать ее.
Краткое содержание статьи
Неконтролируемым считается недуг, симптомы которого не могут четко контролироваться. При неконтролируемом течении болезни основные симптомы астмы, такие как: кашель, частая одышка, хрипы со свистом и приступы удушья, проявляются у пациента и днем и ночью.
Среди причин возникновения неконтролируемой бронхиальной астмы можно выделить несколько основных:
- Лечение было не полным или не довелось до конца.
- Больной не выполнял все рекомендации врача и не проходил регулярные осмотры.
- В жизни больного имел место переезд в другой город или страну.
Относительно последнего пункта можно сказать, что климатические условия и бронхиальная астма очень взаимосвязаны. Это значит, изменения климата может ощутимо ухудшить течение болезни.
Неконтролируемое течение заболевания снижает трудоспособность и повседневную активность больного. Ингалятор для расширения бронхов используется чаще, а показатель скорости выдоха воздуха снижается. Если больной остается в таком состоянии более недели, то врачи диагностируют обострение бронхиальной астмы.
ВАЖНО! Во избежании развития обострения, при первых проявлениях неконтролируемой формы астмы следует увеличивать дозировку и частоту применения используемых медикаментов. Также необходимо проконсультироваться с врачом на предмет увеличения количества препаратов.
Стоит отметить, что большая часть пациентов сталкивается с обострением из-за недостаточного контроля и неадекватной терапии.
Выяснив, что неконтролируемая бронхиальная астма проявляется более чем у 70% больных специалисты разных стран стали искать самую приемлемую базисную терапию этого недуга. Изначально стали оценивать результативность и безопасность использования ингаляционных кортикостероидов. Изучая этот вопрос, открыли эффект «плато», суть которого заключается в следующем. Превышение пороговых доз ингаляционных препаратов не улучшает клинико-функциональное состояние пациентов.
Также был обоснован подход step-down, согласно которому терапия должна начинаться с более жёстких препаратов, чем при начальном лечении. Данный подход способствует быстрой ликвидации бронхиального воспаления, однако противоречит эффекту «плато».
Все встало на свои места, когда открыли эффект синергизма противовоспалительного действия отдельного класса медикаментов. Данные средства стали включать в базисную терапию совместно с ингаляционными кортикостероидами. Более результативной, чем применение больших доз ИКС при неконтролируемой форме, стала терапия Сальметерола в ингалятор. Это отлично купирует бронхоспазм.
Совмещение Сальметерола с любыми дозировками Флютиказона пропионата оказалось намного результативнее. Значительное увеличение дозировки ИКС в меньшей степени улучшает функции легких. Кроме того для лечения неконтролируемой формы стали вводить теофиллиновые или антилейкотриеновые средства с пролонгированным действием. Они работают намного эффективней, чем двойная доза ИКС.
Также, в лечении неконтролируемой бронхиальной астмы стали опираться на концепцию комбинированной терапии. Согласно ей пролонгированные бета2-агонисты со своим аддитивным эффектом преобладают над удвоением дозировки ИКС. Комбинированная терапия имеет значимое достоинство – она влияет на 2 звена недуга:
- Воспаление (через ИКС);
- Бронхиальную гиперреактивность (через пролонгированные бета2-агонисты).
Первым лекарственным средством комбинированной терапии стал Серетид мультидиск. Он совмещается в одной ингаляции с Флютиказоном пропионатом и Сальметеролом. Является отличным препаратом базисной терапии, дозировку которого можно подобрать согласно нуждам пациента.
- Ослабление симптоматики заболевания – этого добиваются благодаря подавлению воспалительного процесса.
- Уменьшение объемов терапии, что подразумевает использование менее агрессивных препаратов.
- Поддержание ослабленной симптоматики.
Современное врачевание неконтролируемого течения недуга широко использует комбинированную терапию. Она на данный момент является в большей степени обоснованной и доказанной, если во внимание брать клиническую результативность.
Народные методы предлагают массу вариантов лечения недуга. Их можно также применять и при неконтролируемом течении заболевания. Народные способы лечения предлагают использование таких средств как:
ВАЖНО! Использование исключительно народных методов при неконтролируемом течении заболевания приведет только к обострению болезни. Поэтому для нормализации общего состояния здоровья необходимо придерживаться рекомендаций врача.
Кроме использования народных рецептов при неконтролируемой форме недуга, немаловажным является самостоятельно контролировать симптоматику. Для этого с лечащим врачом расписывается план самоведения, который основывается на значениях скорости выдоха воздуха (берутся пиковые показатели) и проявлениях болезни.
Разработав данный план, больной может самостоятельно корректировать лечение в рекомендованных рамках. Здесь все зависит от самочувствия и результатов наблюдения по выдоху, а обострение болезни не произойдет, если четко придерживаться предписаний.
Стоит также вести дневник самоконтроля, где будут перечислены индивидуальные рисковые показатели близкие к обострению, ежедневные дозировки профилактических средств пролонгированного действия, описаны признаки и симптомы ухудшения состояния, а также инструкцию по лечению обострения и случаи, при которых нужно срочно вызывать скорую помощь.
Очень важно также проходить регулярные осмотры у своего лечащего врача. Чтобы распознать неконтролируемое течение заболевания опытный специалист предложит больному пройти “Тест по контролю над астмой”. Он успешно позволяет провести самооценку и упрощает взаимоотношения пациента с врачом. Данное тестирование является очень простым и объективно в баллах отражает показатели оценки контроля.
Вылечить Астму можно без лекарств и прочего физического вмешательства. Современная медицина к сожалению очень часто борется только с последствиями заболевания, а на самом деле нужно искать причину. Полностью вылечить, исцелить Астму без последствий могут целители. При данном методе лечения воздействие идёт на энергетическом уровне как на сам больной орган, так и на причину болезни.
Никогда не верил в то, что нельзя пощупать собственными руками,а шарлатаны-“целители”,этим и пользуются:-Скажите,любезный,а почему я не чувствую никакого эффекта от Вашего лечения? -Ну, это и неудивительно, батенька,ведь,я лечил Вас на ЭНЕРГЕТИЧЕСКОМ уровне…не забудьте оплатить,пожалуйста.. И лох идёт платить “за воздух”…
источник
Публикации по теме:
ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ
Бронхиальная астма — это хроническое воспалительное заболевание дыхательных путей, в котором принимают участие многие клетки и клеточные элементы. Хроническое воспаление обусловливает развитие бронхиальной гиперреактивности, которая приводит к повторяющимся эпизодам свистящих хрипов, одышки, чувства заложенности в груди и кашля, особенно по ночам и ранним утром. Эти эпизоды обычно связаны с распространенной, но изменяющейся по своей выраженности обструкцией дыхательных путей в легких, которая часто бывает обратима, либо спонтанно, либо под действием лечения (GINA, 2006).
В последних международных документах развивается концепция о нецелесообразности выделения степени тяжести БА для обычной клинической практики и целесообразности перехода на деление БА по уровню контроля. Классификация БА по степени тяжести рекомендуется только для научных целей. Однако, по мнению экспертов РРО, учитывая важность первоначальной оценки тяжести БА, а также социальные и экспертные особенности нашей страны, целесообразно сохранение классификации по степени тяжести БА для РФ. Тяжесть БА традиционно определялась как внутренний индивидуальный уровень активности болезни. Наиболее правильная оценка тяжести БА может быть сделана только перед началом терапии или какого- либо вмешательства (элиминационные мероприятия). Итак, по степени тяжести БА делится на интермиттирующую, легкую, среднетяжелую и тяжелую персистирующую (табл.1).
В соответствии с последней номенклатурой аллергических болезней, астму, опосредованную иммунологическими механизмами, следует называть аллергической астмой. Аллергические механизмы имеют преобладающее значение почти в 80% случаев детской астмы и более чем в 50% случаев у взрослых. Если доказано участие 1дЕ антител в формировании астмы, то следует обозначать ее IgE — опосредованной аллергической астмой. В нашей стране эту форму бронхиальной астмы принято называть атопической. Термин атопия следует использовать только после документированного подтверждения IgE сенсибилизации: выявлением специфических IgE антител в сыворотке крови или положительными результатами кожных тестов с аллергенами, то есть проведения специфического аллергологического обследования, кото¬рое выполняется только врачом аллергологом- иммунологом.
В GINA, 2006 рекомендована классификация БА по уровню контроля с выделением контролируемой, частично-контролируемой и неконтролируемой БА (табл.2). Такой подход лучше описывает состояние болезни относительно проводимых лечебных мероприятий, отражает понимание того, что тяжесть БА зависит не только от выраженности симптомов заболевания, но и от ответа на терапию и что у конкретного пациента степень тяжести может изменяться в течение нескольких месяцев или лет. Контроль БА может достаточно быстро изменяться в ответ на воздействие триггеров или проводимую терапию, и хотя он частично определяется тяжестью болезни, он также включает оценку адекватности проводимой терапии.
Примеры формулировки диагноза БА:
Бронхиальная астма, атопическая форма, легкого персистирующего течения, частично- контролируемая. Интермиттирующий аллергический ринит, ремиссия. Аллергический конъюнктивит, ремиссия. Аллергия к клещу домашней пыли, шерсти домашних животных (кошка).
Классификация БА по степени тяжести.
| Характеристики | Интермиттирующая БА | Легкая персистирующая БА | Среднетяжелая персистирующая БП | Тяжелая персистирую- щая БА |
| Дневные симптомы | Реже 1 раза в неделю | Чаще 1 раза в нед., но реже 1 раза в месяц | Ежедневные | Ежедневные |
| Обострения | Кратковременные | Могут нарушать активность и сон | Могут нарушать активность и сон | Частые |
| Ночные симптомы | S 2 раз в месяц | Чаще 2 раз в месяц | >1 раза в неделю | Частые Ограничение физической активности |
| ОФВ1 или ПСВ | >80% от должных значений | 80% от должных значений | 60-80% от должных значений | 260% от должных значений |
| Вариабельность ПСВ или ОФВ1 | 30% | >30% |
Классификация БА по уровню контроля болезни (GINA, 2006)
| Характеристики | Контролируемая БА (все нижеперечисленное) | Частично- контролируемая БА (любое проявление в течение любой недели) | Неконтролируемая Б А | |||||||||||||||||||
| Дневные симптомы | Отсутствуют или S2 эпизодов в неделю | > 2 эпизодов в неделю | ||||||||||||||||||||
| Отсутствуют | Любые | Наличие трех или более признаков частично- контролируемой БА в течение любой недели | ||||||||||||||||||||
| Ночные симптомы/ пробуждения | Отсутствуют | Любые | Наличие трех или более признаков частично- контролируемой БА в течение любой недели | |||||||||||||||||||
| Потребность в препаратах неотложной помощи | Отсутствуют или S2 эпизодов в неделю | > 2 эпизодов в неделю | ||||||||||||||||||||
| Функция легких (ПСВ или ОФВ1) | Нормальная | 70% от должного, средняя: ОФВ, =50-60% , тяжелая: ОФВ, 12% (или >200мл) по сравнению с со значением до ингаляции бронхолитического препарата. В качестве бронходилятационных агентов рекомендовано использовать: 1) (32-агонисты короткого действия (сальбутамол, фенотерол — до 800 мкг, тербуталин — до 1000 мкг) с измерением бронходилатационного ответа через 15 мин. Положительная проба говорит об обратимости имеющих место нарушений показателей бронхиальной проходимости или о наличии скрытого бронхоспазма в случае неизмененных исходных показателей. Пиковая скорость выдоха (ПСВ) измеряется с помощью пикфлоуметра и является важным методом диагностики (при отсутствии возможности проведения спирометрии) и оценки эффективности терапии БА. Современные пик- флоуметры отличаются портативностью, сравнительно невысокой стоимостью, простотой в обращении и являются идеальным выбором для ежедневной оценки выраженности бронхиальной обструкции пациентами в домашних условиях. Следует рекомендовать пациентам измерять ПСВ утром, сразу после пробуждения и до приема препаратов; обычно при этом получают близкое к минимальному значение ПСВ. Вечернее измерение проводится перед сном, получая более высокий показатель ПСВ. Суточную вариабельность ПСВ определяют как амплитуду ПСВ (разность между максимальным и минимальным значениями в течение дня) выраженную в процентах от средней за день ПСВ [ и усредненную за 1-2 недели. Другой метод определения вариабельности ПСВ заключается в определении минимальной за 1 неделю ПСВ (утренней) в процентах от самого лучшего в этот же период показателя (Min%Max). Мониторинг ПСВ полезен в следующих | случаях: — Подтверждение диагноза БА (при отсутствии возможности проведения спирометрии): Е прирост ПСВ после ингаляции бронхолитика на 60 л/мин (или на 20%) по сравнению с ПСВ до ингаляции; либо изменение ПСВ в течение [ суток более чем на 20%. — Оценка контроля БА, особенно у больных f недооценивающих симптомы астмы. График или дневник пикфлоуметрии служат дополнительным s инструментом оценки эффективности терапии. — Выявление факторов окружающей среды (аллергены, профессиональные факторы, физическая нагрузка, другие триггеры), провоцирующих появление симптомов БА. Для этой цели рекомендуется проведение пикфлоуметрии несколько раз в день в течение периода предполагаемого воздействия факторов риска на работе или дома, а также в период их отсутствия. Выявление бронхиальной гиперреактивности (БГР). Наличие БГР является одним из важных критериев диагноза БА. Гипервосприимчивость дыхательных путей проявляется ; чрезмерной бронхоконстрикторной реакцией [ на различные раздражители. Основным методом измерения дыхательной гипервосприимчивости является бронхоконстрикторный тест с [ метахолином, гистамином, физической нагрузкой. Оценка результатов бронхопровокационного теста проводится по динамике ОФВг Тест считается положительным при падении ОФВ, на 20% и более (от исходного значения) после ингаляции бронхоконстрикторного агента или после физической нагрузки. Специфическое аллергологическое обследование проводится в фазу ремиссии БА врачом аллергологом-иммунологом. Оно включает в себя: проведение кожных проб с небактериальными аллергенами, провокацион¬ных тестов с аллергенами, лабораторных тестов для определения специфических lgE-антител. В настоящее время для диагностики аллергических заболеваний применяют аппликационные, скарификационные, внутрикожные тесты и тест уколом (prick-тест). Их постановка и оценка осуществляется на коже волярной поверхности предплечья или спины по общепринятым методикам. Выбор аллергенов для тестирования и вид проб определяются результатами аллергологического анамнеза и клинической картиной заболевания. За 3-7 дней до постановки аллер- гопроб отменяются антигистаминные препараты. Проведение провокационных (назального, бронхиального, орального) тестов с аллергенами осуществляется при наличии показаний. Учитывая высокую частоту атопической БА у детей и взрослых, каждый пациент с подозрением на БА или имеющий установленный диагноз БА должен быть проконсультирован врачом аллергологом-иммунологом, который определяет необходимость и объем специфического аллергологического обследования, а в дальнейшем — специфического лечения. СОВРЕМЕННЫЕ ПРИНЦИПЫ ТЕРАПИИ БРОНХИАЛЬНОЙ АСТМЫ У ВЗРОСЛЫХ К сожалению, на сегодняшний день мы не можем полностью излечить больного от бронхиальной астмы, однако мы можем добиться полного контроля над болезнью у большинства пациентов. Качество жизни этих больных может быть значительно улучшено, и не отличаться от здоровых лиц в том случае, если своевременно поставлен диагноз и назначена адекватная терапия, контролирующая астму. Контроль БА означает контроль клинических проявлений заболевания, критерии которого определены в международном документе GINA, 2006, как
В идеале полный контроль БА должен означать отсутствие не только симптомов болезни «нормальную функцию легких, но и отсутствие признаков воспаления в нижних дыхательных путях, ибо хорошо известно, что даже при отсутствии клинических симптомов, воспаление слизистой бронхиального дерева может сохраняться и приводить к бронхиальной гиперреактивности. Воспалительные изменения и ремодулинг (фиброзирующие изменения) бронхиальной стенки наблюдаются не только у пациентов со среднетяжелой и тяжелой астмой, но и у больных с легкой формой болезни, у которых они отличаются лишь меньшей интенсивностью. У пациентов с легкой БА могут развиваться тяжелые обострения болезни. 30-40% госпитализаций по поводу обострения БА приходится на долю пациентов с легкой формой болезни. Именно для этих пациентов характерна переоценка контроля своей астмы, использование симптоматического лечения и отсутствие адекватной противовоспалительной терапии. Основными составляющими контроля БА являются:
Обучение пациента Бронхиальная астма не однородное заболевание. Аллергические механизмы имеют преобладающее значение почти в 80% случаев детской астмы и более чем в 50% случаев астмы у взрослых. Поэтому меры по элиминации или сокращению аллергена (аллергенов) рассматриваются как первая линия терапии, и даже когда они не могут быть выполнены полностью, они существенно редуцируют необходимую фармакотерапию (Приложение). Как показали международные клинические исследования, на сегодняшний день достижение полного или хорошего контроля БА возможно у большинства пациентов, при условии правильной оценки тяжести, существующего уровня контроля БА и назначения адекватной противоастматической длительной базисной терапии. Фармакотерапия — неотъемлемая часть лечения любой бронхиальной астмы. Все препараты для медикаментозного лечения астмы делятся на два вида:
К препаратам первой группы относятся быстро действующие |3-адреномиметики (сальбутамол, фенотерол, тербуталин, формотерол), ингаляционные антихолинергические препараты (ипратропиума бромид), комбинированные препараты ингаляционных р2-адреномиметиков и ипратропиума бромида, теофиллин короткого действия. Ко второй группе относятся препараты, обладающие противовоспалительным действием: ингаляционные и системные кортикостероиды, кромогликат и недокромил натрия, длительно действующие β2-агонисты в комбинации с ингаляционными кортикостероидами, пролонгированные теофиллины, антагонисты лейкотриеновых рецепторов и антитела к IgE. Эквипотентные суточные дозы ИГКС у взрослых.
Препараты базисной поддерживающей терапии Среди препаратов этой группы безусловный приоритет имеют ингаляционные глюкокортикостероиды (ИГКС). Группу ИГКС, представленных на нашем рынке, составляют: беклометазона дипропионат (торговые названия: беклазон — эко, беклазон — эко легкое дыхание, бекотид, кленил), будесонид (бенакорт, пульмикорт), флутиказона пропионат (фликсотид) и мометазона фуроат. ИГКС, составляющие основу базисной противовоспалительной терапии астмы, предотвращают развитие симптомов и обострений болезни; улучшают функциональные показатели легких; уменьшают бронхиальную гиперреактивность и некоторые компоненты ремоделинга бронхиальной стенки, в частности утолщение базальной мембраны эпителия и ангиогенез слизистой бронхов. Раннее назначение ИГКС может улучшать контроль бронхиальной астмы и нормализовать функцию легких, а также предотвратить развитие необратимого поражения дыхательных путей. Они показаны для лечения персистирующей бронхиальной астмы любой степени тяжести (Рис. 3). Степень выраженности клинических проявлений астмы и степень нарушения функции легких определяют начальную дозу ИГКС. У большинства взрослых пациентов эффект достигается при применении сравнительно низких доз ИГКС, эквивалентных 400 мкг будесонида в сутки. В таблице 4 представлены эквипотентные суточные дозы ИГКС у взрослых. Вероятность системных эффектов ИГКС определяется их активностью и биодоступностью: при применении дозированных аэрозоле* без спейсера около 80% дозы проглатываете» и поступает в желудочно-кишечный тракт. Благодаря активной биотрансформации в печени, ИГКС обладают очень низкой системной биодоступностью (беклометазона дипропионат 20%, будесонид — 11%, флутиказона пропионат — 1%), что делает риск развития системны* эффектов незначительным. Что касается местных побочных эффектов, то они одинаковы дли всей группы ИГКС и заключаются в возможности развития кандидоза полости рта и горла, дис- фонии, возникновения рефлекторного кашля* парадоксального бронхоспазма. Предупредить возникновение этих нежелательных явлений помогают следующие мероприятия: использование спейсера, полоскание рта после ингаляции ИГКС; снижение кратности приема препарата, что существенно снижает риск развития кандидоза. Парадоксальный бронхоспазм необходимо немедленно купировать ингаляционными (β2-агонистами короткого действия. Иногда предварительное (непосредственно перед ингаляцией ИГКС) применение β2-агонистов оказывается эффективным способом профилактики рефлекторного кашля и бронхоспазма и может быть рекомендовано на начальном этапе лечения ИГКС, особенно при использовании высоких доз ИГКС и выраженной бронхиальной гиперреактивности. ИГКС в низких и средних дозах редко вызывают нежелательные побочные эффекты и обладают хорошим показателем «риск/польза». Для достижения контроля бронхиальной астмы необходим длительный постоянный прием ИГКС в адекватных для данного конкретного пациента дозах. После достиже* ния стабильного контроля астмы, поддерживающая доза ИГКС подбирается индивидуально. Если контроль бронхиальной астмы стабильно поддерживается на протяжении 3 месяцев и больше, возможно уменьшение дозы ИГКС но 50%. ИГКС позволяют добиться полного контроля бронхиальной астмы, однако они не излечивают астму и прекращение приема ИГКС зачастую приводит к возвращению симптомов болезни. Эффект ИГКС имеет дозозависимый характер и контроль болезни может быть достигнут быстрее при применении более высоких доз. Однако с повышением доз ИГКС увеличивается риск развития нежелательных побочных эффектов. Поэтому при отсутствии контроля бронхиальной астмы, добавление к ИГКС препаратов другого класса следует предпочесть увеличению доз ИГКС. Наиболее эффективной и перспективной является комбинация ИГКС и длительнодействующего β2-агониста. Это направление фармакотерапии астмы активно развивается в настоящее время: создаются и регистрируются новые комбинированные препараты. На Российском фармацевтическом рынке существуют 2-а таких препарата: саль- метерол/флутиказона пропионат (серетид) и формотерол/будесонид (симбикорт), ожидается регистрация еще одного комбинированного препарата — формотерол/беклометазона дипропионат. Создание этой группы препаратов имело строгое научное обоснование. Два разных класса препаратов, соединенные водном ингаляторе, обладают комплементарным действием на патофизиологию БА (Рис 2). ИГКС подавляет хроническое воспаление и уменьшает бронхиальную гиперреактивность |БГР), тогда как длительнодействующий (32- агонист (ДД(ЗА) не только вызывает расслабление гладких мышц бронхов, но и подавляет высвобождение бронхоконстрикторных медиаторов из тучных клеток дыхательных путей, уменьшает отек слизистой бронхов и может также подавлять активацию сенсорных нервных окончаний в бронхах. Комбинированная терапия ИГКС и длительно действующими β2-агонистами является эффективной в лечении БА, начиная с 3-й ступени (Рис.3). Однако, в последние годы активно изучается стратегия раннего назначения комбинированных препаратов при БА. В частности, в ряде исследований показано, что сальметерол/ флутиказона пропионат в качестве стартовой поддерживающей терапии обеспечивает пациентам дополнительные клинические преимущества (улучшение функции легких, контроль симптомов) по сравнению с монотерапией ИГКС при сравнимом профиле безопасности. В июле 2008 г зарегистрировано новое показание для препарата сальметерол/флутиказона пропионат в качестве стартовой поддерживающей терапии у пациентов с персистирующей бронхиальной астмой (ежедневное возникновение симптомов, ежедневное использование средств для быстрого купирования симптомов) при наличии показаний к назначёнию препаратов кортикостероидов для достижения контроля над заболеванием. Раннее назначение комбинированной терапии ИГКС и длительнодействующими (β2— агонистами имеет ряд преимуществ. Быстрое достижение эффекта увеличивает приверженность лечению со стороны пациента, профи- лактирует развитие обострений и формирование необратимых изменений бронхиальной стенки. Кроме этого, сочетание двух препаратов в одном ингаляторе удобно для пациента и является гарантией приема противовоспалительного препарата — ИГКС. Настоящий уровень знаний и опыт международных клинических исследований не рекомендуют использование длительнодействующих β2-агонистов в качестве систематической монотерапии при бронхиальной астме, ибо такое лечение может маскировать хроническое воспаление в нижних дыхательных путях и увеличивать риск развития тяжелых обострений бронхиальной астмы. Системные глюкокортикостероиды не рекомендуются для поддерживающей терапии БА из-за развития побочных эффектов. Эти препараты применяются для лечения тяжелых обострений БА. Терапевтический эффект системных ГКС начинает проявляться через 4-6 часов после применения и предупреждает дальнейшее прогрессирование обострения, способствуют более быстрому разрешению обструкции. Предпочтительнее использование пероральных (таблетированных) форм системных ГКС, которые также эффективны как парентеральные формы, но легче дозируются. Стандартный короткий курс лечения обострения БА: 30-50 мг преднизолона в сутки (в 1-2 приема) в течение 5-10 дней в зависимости от тяжести обострения. После купирования симптомов обострения и возвращения функциональных показателей к обычным значениям пациента возможна отмена или постепенное снижение дозы пероральных ГКС (до полной отмены) на фоне поддерживающей терапии ИГКС. Антилейкотриеновые препараты. Ци стеиниловые лейкотриены являются одними из важных медиаторов БА, продуцирующимися преимущественно тучными клетками и эозинофилами. Они способны вызывать бронхокон- стрикцию, повышать секрецию слизи в бронхах, сосудистую проницаемость и вызывать отек. Существует два пути угнетения активности этих медиаторов: подавление синтеза и блокада их эффектов на уровне клеток. На основании первого механизма основано действие ингибитора 5- липоксигеназы (зилеутон), второго — действие антагонистов рецепторов цистеиниловых лейкотриенов: зафирлукаста (аколат), монтелукаста (сингуляр) и пранлукаста. В России зарегистрированы: зафирлукаст и монтелукаст. Антилейкотриеновые препараты обладают слабым бронхолитическим действием, уменьшают выраженность симптомов БА, улучшают функциональные показатели, интенсивность воспаления в слизистой бронхов, снижают частоту обострений БА. Как видно из рисунка 3, они могут быть альтернативой ИГКС при легкой персистирующей БА для пациентов, категорически не желающих использовать ИГКС. Однако в качестве монотерапии, они безусловно уступают ИГКС по своей противовоспалительной активности, а стало быть и клиническому эффекту. Возможно использование антилейко— триеновых препаратов в дополнение к ИГКС, когда монотерапия ИГКС (низкими, средними или высокими дозами) недостаточна для контроля БА, хотя в ряде клинических исследований убедительно показана большая эффективность комбинации ИГКС с длительнодействующими β2-агонистами. Тем не менее, этот класс препаратов имеет свои преимущества, заключающиеся в системном противоаллергическом действии, эффективности при аспириновой БА и бронхоспазме, вызванном физической нагрузкой. Антилейкотриеновые препараты предназначены для приема внутрь, поэтому способны оказывать системные противовоспалительный, противоаллергический эффекты при сочетании БА и аллергического ринита. Они способны предотвращать развитие аспирининдуцировонного бронхоспазма у больных аспириновой БА, а также постнагрузочного бронхоспазма у больных с проявлениями бронхоспазма, вызванного физической нагрузкой. Достоинством препаратов антагонистов рецепторов цистеини- ловых лейкотриенов является их хорошая переносимость и низкая частота побочных эффектов. Взаимосвязь терапии антилейкотриеновы- ми препаратами и развитием синдрома Чердж- Стросс (системный гранулематозный васкулит), описываемая несколько лет назад ( с частотой 1 случай в год на 25000 — 150000 пролеченных пациентов ), объясняется прежде всего быстрым снижением дозы системных или ингаляционных ГКС у пациентов с тяжелой БА, что привело, по-видимому, к проявлению фонового заболевания. Однако у некоторых пациентов нельзя все же полностью исключить причинноследственной связи. Кремоны. Кромоны — это препараты ди- натриевой соли кромоглициевой кислоты: кромогликат натрия (интал, кропоз) и недокромил натрия (тайлед). Действие этих препаратов обусловлено стабилизацией клеточной мембраны тучных клеток и торможением процесса высвобождения медиаторов аллергической реакции, развивающегося после связывания аллергена со специфическими IgEна мембране тучных клеток. До конца механизм этого действия кромонов неизвестен. Предполагают, что они блокируют кальциевые каналы мембраны тучной клетки, ингибируют фосфодиэстеразу и окислительное фосфорилирование. Кромоны подавляют активность нейтрофилов, эозинофилов, моноцитов и макрофагов, а также снижают чувствительность афферентных нервов. Эффективность кромонов при БА у взрослых незначительная, они существенно уступают ИГКС, и поэтому могут быть использованы только при легкой персистирующей БА. Причем в случае отсутствия контроля БА на фоне терапии кромонами в течение 4-х недель, необходимо назначить больному ИГКС. Достоинство этих препаратов — в их безопасности. Кромо- гликат и недокромил натрия практически полностью лишены побочных эффектов, что дает им предпочтение при лечении детей с легкой персистирующей БА. Теофиллины длительного действия. Теофиллин является бронхолитиком и в низких дозах обладает слабым противовоспалительным действием. Теофиллины длительного действия (с замедленным высвобождением) можно принимать один или два раза в сутки внутрь. Имеющиеся на сегодняшний день данные, позволяют предположить незначительную эффективность теофиллина замедленного высвобождения в качестве первого препарата для длительного поддерживающего лечения БА. Теофиллины длительного действия могут быть использованы в комбинации с ИГКС, однако в данном случае они уступают по своей эффективности и безопасности длительнодей- ствующим р2-агонистам. Существуют следующие формы выпуска препарата теофиллина с замедленным высвобождением: теопэк (таблетки 300 мг), теотард (капсулы 200 и 350 мг), теофиллин-Н.С. (таблетки 300 мг) Средняя доза для взрослого составляет 300 мг 2 раза в сутки (из расчета 10-15 мг/кг/сут в 2 приема). К нежелательным эффектам, проявляющимся при применении высоких доз теофиллина (10 мг/кг/сут и более) относятся: тошнота, рвота, жидкий стул, нарушения ритма сердца, судороги. Побочные эффекты можно уменьшить путем тщательного подбора доз и мониторинга концентрации препарата в крови; при длительном применении побочные эффекты уменьшаются или исчезают. Антитела к IgE.В последние годы активно изучается эффективность применения ре- комбинантных человеческих анти- 1дЕ-антител (омализумаб, ксолар) у больных аллергическими заболеваниями, в частности, средне-тяжелой и тяжелой атопической бронхиальной астмой, устойчивой к терапии ингаляционными корти- костероидами. Омализумаб (Ксолар) зарегистрирован в России. Терапевтический эффект достигается с помощью нескольких типов воздействия омализумаба. Во-первых, омализумаб связывает IgE, препятствуя его взаимодействию с FceRI(высокоаффинные 1дЕ-рецепторы на клетках воспаления). После лечения омали- зумабом уровень свободного IgEв сыворотке снижается. Кроме того, омализумаб существенно уменьшает количество рецепторов FceRIна базофилах (возможно, потому что плотность рецепторов FceRIрегулируется уровнем свободного IgEв сыворотке) и тем самым снижает чувствительность клетки к действию аллергенов. Применение анти-lgEограничивается пациентами с повышенным уровнем IgEв сыворотке. Результаты клинических испытаний показали, что при лечении омализумабом снижается интенсивность ранней и поздней фаз аллергической реакции, уменьшается количество эозинофилов в мокроте. В ходе трех больших плацебо-контролируемых исследований доказано преимущество омализумаба в качестве дополнительной терапии при лечении атопической бронхиальной астмы среднего и тяжелого течения. Наибольшая эффективность препарата проявилась при лечении больных с тяжелыми формами заболевания. Анти-lgEтерапия включена в руководство GINA2006 на 5 ступени терапии (Рис.3) в качестве дополнения к лечению ИГКС, длительнодействующими (32-агонистами и другими препаратами аллергической формы БА. Применение омализумаба ограничено из-за высокой стоимости и возможности использования только инъекционных форм, а также отсутствия результатов длительных наблюдений. Решение о проведении данного вида лечения, а также и проведение собственно анти-lgEтерапии, находится в компетенции врача специалиста (аллерголога-иммунолога или пульмонолога). Препараты неотложной помощи Препараты неотложной помощи показаны всем больным БА, независимо от тяжести и уровня контроля болезни, для быстрого купирования бронхоспазма и сопутствующих ему симптомов. Ингаляционные (β2-агонисты короткого действия являются препаратами выбора для купирования острого бронхоспазма, а также для профилактики бронхоспазма, вызванного физической нагрузкой. На отечественном фармацевтическом рынке эти препараты представлены сальбутамолом (асталин, венто- лин, саламал эко, саламол эко легкое дыхание, сальгим) и фенотеролом (беротек Н). Бронхорасширяющий эффект ингаляционных короткодействующих (32-агонистов наступает в течение нескольких минут. Эти препараты рекомендуется применять только по потребности, которая должна быть минимальной или отсутствовать вовсе у больных с контролируемой БА. Растущее, особенно ежедневное, применение этих препаратов указывает на потерю контроля БА и требует пересмотра терапии. Наиболее распространенными побочными эффектами короткодействующих β2-агонистов являются: тахикардия, тремор, головная боль. Эти эффекты дозозависимые и проявляются обычно при использовании высоких доз препарата. Длительнодействующий β2-агонист формотерол, благодаря быстрому началу бронхолитического действия, также может использоваться для облегчения симптомов БА, но только у пациентов, получающих базисную противовоспалительную терапию ИГКС. источник |