Аптека нелекарственной оздоровительной продукции. Официальный сайт Витаминного центра Витамины для Вас
Аптека нелекарственной оздоровительной продукции
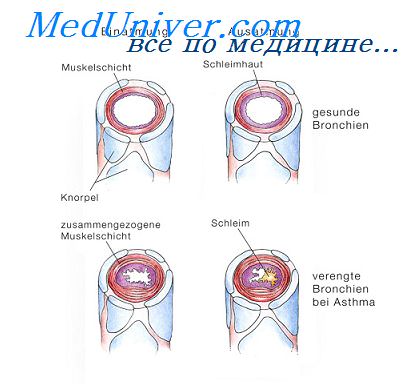
Если вы страдаете одышкой, у вас свистящее дыхание, напряженность в грудной клетке, хронический кашель с прозрачной или белой мокротой, вы, возможно, один из 3% людей, имеющих астму. Во время приступов астмы мелкие бронхи сужаются, возникает спазм, создавая трудности для доступа воздуха. Если спазм воздухоносных путей слабый, ощущается небольшое напряжение или посвистывание при дыхании. Небольшой кашель — это терпимое неудобство. Но иногда приступы приводят к жестокому спазму, и тогда астма может угрожать жизни, если не лечится правильно и вовремя. Любой астматик, у которого бывают приступы такого типа, должен находиться под бдительным наблюдением лечащего врача.
Именно потому, что существует много различных уровней тяжести астмы, у нее много разных причин возникновения. У некоторых людей астма развивается вследствие аллергии на пыльцу, домашних животных, пыль, те или иные виды пищи и некоторые лекарственные препараты. У одних людей свистящее дыхание возникает при физической нагрузке, у других — только при респираторных инфекциях. Могут ли помочь витамины и неорганические элементы при том, что рецепты врача все еще являются основой лечения астмы? Да, могут. Давайте рассмотрим, каким образом.
Кофеин в кофе и его родственник теобромин, найденный в чае, действуют как эффективные бронхорасширяющие средства (вещества, которые расслабляют и увеличивают просвет бронхиальных трубок). Действительно, в течение длительного времени при лечении астмы в качестве бронхорасширяющего средства прописывали теофиллин, являющийся в действительности не чем иным, как особой формой кофеина (но почти в два раза более сильной). Рекомендации: если кофеин не противопоказан по другим показаниям (проблемы с сердцем), можно снять легкий астматический приступ, выражающийся в затрудненном дыхании или одышке, с помощью кофеина, содержащегося в трех-четырех чайных чашках (по 160-180 г) обычного кофе, которые можно выпить в течение дня. Каждая чашка содержит около 150 мг кофеина. Предостережение: если постоянно использовать прописанные лекарства, содержащие теофиллин, кофеин может очень помочь, поскольку эти два вещества взаимосвязаны. Однако если их комбинировать, может возникнуть токсическая передозировка теофиллина. Симптомы токсической передозировки заключаются в треморе (дрожании) рук, тошноте и рвоте, раздражительности, бессоннице, избыточно повышенной активности.
Астматические хрипы усиливаются, если в рационе понижено содержание никотиновой кислоты. Если астматическая одышка имеет место главным образом вследствие аллергии, прием никотиновой кислоты помогает облегчать симптомы, вероятно, потому, что тучные клетки выбрасывают меньше гистамина (см. статью «Витамины против аллергии»). Рекомендации: принимайте 100 мг никотиновой кислоты ежедневно.
Уровень витамина В6 (пиридоксина) у астматиков может быть низким, особенно у людей, которые принимают лекарства-бронхорасширители на основе теофиллина. Применение витамина, по-видимому, помогает при астматической одышке, иногда значительно. Рекомендации: можно начать с дозы 50 мг один или два раза в день. Если после трех-четырех недель астматические приступы стали менее тяжелыми и появляются реже, следует придерживаться этой дозы. Если такая доза не дает результата, можно ее увеличить до 100 мг два раза в день. Но выше этого уровня дозу увеличивать нельзя, и нужно немедленно прекратить принимать дополнительную дозу витамина, если развивается онемение или покалывание в ступнях или кистях рук. Высокие дозы витамина В6 иногда вызывают нервное возбуждение, которое может стать постоянным, если продолжать прием витамина в высоких дозах. Доза в 200 мг, которую некоторые исследователи применяли даже в лечении детей, не должна вызвать осложнений, но с этим витамином лучше ошибиться в диапазоне безопасных доз. У некоторых людей возникает реакция на этот витамин, у других — нет, но невозможно предсказать наперед, будет ли она у вас или нет.
На основании большого числа исследований на людях всех возрастов, включая грудных младенцев, доказано, что витамин В12 является превосходным средством облегчения астматического дыхания. В точности неизвестно, как витамин помогает расслаблению бронхиальных трубок, но он весьма эффективен в повышении способности переносить физические нагрузки и аллергены, т. е. вещества, вызывающие симптомы аллергии. Рекомендации: если за вами будет наблюдать врач, наилучший способ применения этого витамина — еженедельные инъекции 1000 мкг препарата в течение четырех недель, а затем ежемесячные инъекции этого же количества витамина в течение трех-четырех месяцев, пока не наступит прекращение симптомов болезни. Несколько менее эффективно применение сублингуальной формы витамина (растворяющейся под языком) в той же дозе по той же схеме. Как показали исследования, одна и та же доза применяется для всех возрастов.
Дефицит витамина С может вызвать усиление астматических симптомов (стесненность дыхания), особенно если астма вызвана аллергией или физической нагрузкой. Эффективность применения витамина С, вероятно, обусловлена уменьшением высвобождения гистамина или стимуляцией тела производить «хорошие» эйкозаноиды (для получения более детальной информации см. статью о витамине С). У людей с соответствующим типом астмы приступы становятся менее частыми и менее сильными, хотя следует сразу добавить, что некоторые люди не подходят для этого типа терапии. Рекомендации: если вы задыхаетесь от физической нагрузки, примите перед ней от 500 до 1000 мг витамина С.
Комбинация витамина С и никотиновой кислоты, по-видимому, усиливает действие каждой компоненты в снижении астматической одышки. Используя эти препараты вместе, можно для получения того же эффекта облегчения астматических симптомов снизить их дозу. Рекомендации: принимайте от 90 до 110 мг никотиновой кислоты вместе с 250-300 мг витамина С в день.
Анализ крови, взятой у людей во время астматического приступа, часто показывает дефицит магния. Неясно, почему этот дефицит может влиять на развитие приступа затрудненного дыхания, но исследователи предполагают, что эти два фактора могут быть связаны. Несмотря на то что в медицинской литературе нет прямых рекомендаций для подобной ситуации, можно применять магний в больших количествах, чтобы предотвратить его дефицит. Рекомендации: принимайте аспартат магния в количестве 200 мг ежедневно. Обратите внимание на обсуждение этого элемента в статье, для того, чтобы понять, как он взаимодействует с кальцием. Для достижения наилучших результатов эти два элемента следует принимать вместе в ориентировочной пропорции 2 мг кальция на 1 мг магния. Нужно принимать ежедневно по крайней мере от 400 до 800 мг кальция с магнием.
Дефицит молибдена очень часто имеет место у людей, обладающих аллергической чувствительностью к сульфитам (встречаются в вине и яйцах). Именно молибден является тем веществом, которое необходимо для ослабления токсического действия сульфитов, и, испытывая недостаток в нем, вы становитесь еще сильнее подвержены действию аллергической чувствительности. Если у вас развивается астматический приступ при потреблении продуктов с сульфитами, вы можете стать более терпимы к ним, если добавите в свой рацион молибден. Рекомендации: начните с приема 250 мкг молибдена дважды в неделю, затем увеличьте дозу до 500 мкг дважды в неделю и, наконец, если это будет необходимо, для достижения максимального эффекта можно увеличить дозу до 750 мкг дважды в неделю. Остановитесь на минимальной дозе, которая, по вашим наблюдениям, достаточно ослабляет астматические симптомы.
Врачи полагают, что N-ацетилцистеин, модифицированная аминокислота, являющаяся составной частью белков, в форме, пригодной для вдыхания, разжижает густую, липкую мокроту пациентов, страдающих астмой. Применение препарата в виде ингаляций дает хорошие результаты. Его действие не всегда такое же эффективное, как таблеток или капсул, принимаемых внутрь, тем не менее он очень хорошо действует на некоторых людей, у которых густая мокрота. Несмотря на то что цистеин сам по себе не способен облегчить все астматические симптомы, если он вообще на вас действует, с его помощью вы можете снизить дозу тех бронхорасширяющих препаратов, которые необходимы вам по остальным показаниям. Рекомендации: начните с приема 200 мг дважды в день, затем через неделю принимайте эту дозу трижды в день. Если вы не почувствуете облегчения, можно увеличить дозу до 400 мг дважды в день. Если и эта доза не даст результата, ее можно увеличить до 500 мг два раза в день. Однако этот уровень превышать не рекомендуется, поскольку в данном случае вероятность хорошего результата от цистеина весьма мала.
Незаменимые жирные кислоты, играющие важную роль в регуляции воспалительных простагландинов в организме, могут помочь снизить набухание и спастическую гиперактивность бронхиальных трубок, особенно при аллергической астме. Рекомендации: полезно дополнить ваш рацион одной-двумя столовыми ложками растительного масла: кукурузного, канолового или оливкового, приготовленного методом холодного прессования, добавив его в легкую приправу для винегрета. Можно найти дополнительный источник омега-6 незаменимых жирных кислот в капсулах препарата Omega Max, содержащим катуральный жир хладноводных рыб , принимаемом по две капсулы в день. Чтобы получить максимальный эффект, следует насколько возможно снизить потребление рафинированного сахара и крахмала. Если вы по каким-либо причинам не сможете получить этот продукт, можно приготовить подходящий заменитель, — и капсулы с рыбьим жиром, добавив к ним витамин Е (который предохраняет эти необходимые жиры от окисления и порчи). Принимайте от одного до трех раз в день 500 мг масла энотеры (источника линолевой кислоты в капсульной форме), 1000 мг рыбьего жира и 100 ME витамина Е. (Опасность для больных диабетом: рыбий жир может вызвать у некоторых диабетиков колебания концентрации сахара в крови. Контролируйте содержание сахара в крови и прекратите принимать их, если уровень сахара в крови станет невозможно контролировать.)
У людей с бронхиальной астмой может вызывать спазмы бронхиальных трубок и усиление астматического дыхания L-триптофан, одна из незаменимых аминокислот, входящих в состав белков. Рекомендации: не принимайте сопутствующий триптофан (обычно запрещенный к продаже) и снижайте количество триптофана в пище до 300 мг в день в течение двух недель для того, чтобы посмотреть, не улучшится ли ваше состояние. В 60 г животного белка (в мясе, яйцах, молоке) содержится 600 мг триптофана. Это означает, что вы должны снизить потребление животного белка из указанных источников триптофана до уровня не более 30 г. Этот уровень слишком мал для взрослых людей. Но, добавляя белки неживотного происхождения, такие как тофу, соевый творог, наряду с малым количеством потребляемого триптофана, вы сможете получать достаточно хороший белок, чтобы удовлетворить потребность организма в восстановлении и сохранении мышечной работоспособности. Если на протяжении от двух до четырех недель вы не заметите улучшения своего астматического состояния, нет необходимости продолжать эту диету и вы можете вернуться к обычному питанию.
Алкоголь в чистом виде действует как мягкий бронхорасширитель и в этом смысле может до некоторой степени действительно помочь при астматических спазмах. Однако мы его очень редко пьем в чистом виде. Чаще всего он присутствует в виде добавок в напитках, таких как пиво, вино или различные спиртные напитки на основе дистиллированного спирта. Если вы страдаете от аллергии к пище и если астматические симптомы зависят от этой аллергии, у вас может развиться астматическое дыхание из-за других компонент в спиртных напитках — остатков хмеля, солода, винограда, ячменя, сульфитов в вине или кукурузы, из которой приготавливаются ликеры. Рекомендации: несмотря на то что умеренное количество алкогольных напитков (стакан вина или 30 г хорошего ликера или пива в день) может не причинить вам беспокойства или может даже помочь расслабиться во время перелета на самолете, применяйте их с осторожностью. Так же как с другими видами пиши, вам следует все время контролировать свою реакцию и избегать экспериментов, чтобы быть уверенным в том, что напитки не затрудняют ваше дыхание и не вызывают кашель.
Рацион с большим содержанием натрия может усилить спастическое сужение бронхиальных трубок, которое вызывается гистамином. Рекомендации: не добавляйте большого количества соли в пищу. Под этим подразумевается — не солите пищу. Это будет помощь вам. Однако вы можете снизить удержание соли в организме более радикальным способом, с помощью основной диеты, которая отучит ваш организм удерживать соль. Диета с большим содержанием крахмала и сахара способствует удержанию соли и жидкости.
источник
Клиническое значение дисбаланса минералов и микроэлементов при бронхиальной астме у детей Алексеева Ольга Владимировна
Данный автореферат диссертации должен поступить в библиотеки в ближайшее время
Уведомить о поступлении
480 руб. | 150 грн. | 7,5 долл. ‘, MOUSEOFF, FGCOLOR, ‘#FFFFCC’,BGCOLOR, ‘#393939’);» onMouseOut=»return nd();»> Диссертация — 480 руб., доставка 10 минут , круглосуточно, без выходных и праздников
240 руб. | 75 грн. | 3,75 долл. ‘, MOUSEOFF, FGCOLOR, ‘#FFFFCC’,BGCOLOR, ‘#393939’);» onMouseOut=»return nd();»> Автореферат — 240 руб., доставка 1-3 часа, с 10-19 (Московское время), кроме воскресенья
Алексеева Ольга Владимировна. Клиническое значение дисбаланса минералов и микроэлементов при бронхиальной астме у детей : диссертация . кандидата медицинских наук : 14.00.09 / Алексеева Ольга Владимировна; [Место защиты: Российский университет дружбы народов].- Москва, 2003.- 192 с.: ил.
Глава I. Современные представления о роли макро- и микроэлементов в развитии аллергии (обзор литературы) 10
1.1. Макро- и микроэлементы в организме человека 10
I 2. Роль отдельных элементов в развитии аллергии 12
1.3. Участие минералов и микроэлементов в основных звеньях патогенеза бронхиальной астмы 39
Глава II. Объем и методы исследования 42
II. 1. Объект исследования 42
ІІ.2. Методы исследования 44
IІ.2.1. Общеклинические методы 44
II.2.2. Специальные методы исследования 46
II.2.2.1. Выбор биологического субстрата 46
II.2.2.2.. Методика определения микроэлементов в волосах 48
II.2.3. Статистические методы обработки материала исследований 53
Глава III. Общая характеристика группы наблюдавшихся детей 55
III.1. Группа детей с бронхиальной астмой 55
Глава IV. Особенности дисбаланса минералов и микроэлементов у детей, больных бронхиальной астмой 68
IV.1. Сопоставимость результатов анализа волос, полученных у обследованных детей методами АЭС-ИП и НАА 68
IV.2. Характеристика макро- и микроэлементного состава волос детей, больных бронхиальной астмой 72
IV.2.1. Сравнительный анализ макро- и микроэлементного состава волос у больных бронхиальной астмой, здоровых детей и выборки из общей детской популяции России 72
IV.2.2. Отклонения в содержании макро- и микроэлементов в волосах у детей с бронхиальной астмой 79
IV.2.3. Клинико-функциональная характеристика дисбаланса макро- и микроэлементов у детей, больных бронхиальной астмой 86
1V.2.3.1. Макро- и микроэлементный состав волос больных бронхиальной астмой детей, в зависимости от тяжести заболевания, его продолжительности и степени нарушения функции внешнего дыхания 86
IV.2.3.2. Макро- и микроэлементный состав волос больных бронхиальной астмой детей, получающих современную патогенетическую терапию 97
IV.2.3.3. Макро- и микроэлементный состав волос детей, больных бронхиальной астмой, имеющих сопутствующую патологию органов пищеварения 102
IV.2.3.4. Сравнительное исследование элементного состава волос детей разного возраста, больных бронхиальной астмой 106
IV.3. Взаимосвязи содержащихся в волосах элементов с некоторыми биохимическими, иммунологическими и клеточными показателями крови у детей, больных бронхиальной астмой 123
Глава V. Обсуждение полученных результатов 137
Практические рекомендации 158
В настоящее время принята «кальциевая» гипотеза формирования синдрома гипереактивности бронхов при бронхиальной астме [178]. По этой гипотезе, ключевое значение отводится повышению концентрации кальция в цитоплазме иммунокопетентных, эпителиальных и мышечных клеток. Вход иона кальция внутрь клетки через специальные кальциевые каналы и выход его из клеточного депо, вызванные воздействием антигена, приводят к активации внутриклеточных систем и выбросу в межклеточное пространство медиаторов аллергии. Кальций-опосредованными процессами являются большинство известных сегодня механизмов, имеющих патогенетическое значение при бронхиальной астме: секреция слизистых желез, сокращение гладкой мускулатуры бронхов, передача нервных импульсов, изменение внутриклеточной концентрации цАМФ, некоторые гормональные воздействия [1, 3,18, 37, 75, 76,104, 178,222]. Однако значение многих из внутриклеточных событий, связанных с изменением внутрицеллюлярной концентрации кальция, остается неясным, в связи с чем «кальциевая» гипотеза бронхиальной астмы требует дальнейшего подтверждения.
Среди других макро- и микроэлементов при бронхиальной астме наиболее изучена патогенетическая роль магния. В первую очередь, она состоит в регуляции концентрации внутриклеточного кальция посредством воздействия на Са-АТФазу, удаляющую избыток кальция из цитозоля как во внутриклеточные депо, так и во внеклеточное пространство. Активность этого фермента снижается при недостатке в среде ионов магния [192]. Магний также вмешивается в метаболизм цАМФ, обеспечивает стабильность мембран. При недостатке минерала в организме создаются условия для избыточной активации перикисного окисления липидов ( ПОЛ) [39].
Существует достаточно тесная связь Mg с функционированием нервной системы. Стимуляция гидролиза ацетилхолина посредством воздействия на холинэстеразу лежит в основе снижения его соединениями гиперреактивности бронхов у больных бронхиальной астмой [37, 144]. Показано влияние Mg и на функционирование «третьего» звена вегетативной нервной системы, с нарушениями в котором связывают наличие нейрогенного воспаления тканей при аллергических заболеваниях: при недостатке минерала в организме у лабораторных животных было отмечено повышение субстанции Р в сыворотке крови [217].
Не вызывает сомнения участие Mg в различных иммунных процессах. Ингибирующее влияние минерала на процесс высвобождения гистамина и стимулирующее — на гистаминопексию, подтверждается во многих работах [141, 150, 217, 218]. Кроме того, экспериментально доказано существование связи между обменом Mg и синтезом IgE , активностью эозинофилов [144, 161]. Это свидетельствует о важном месте метаболизма минерала в основных звеньях патогенеза бронхиальной астмы.
Обнаруженное снижение кортизолпоглощения лимфоцитов у больных бронхиальной астмой при недостатке магния [33] может быть одним из механизмов развития недостаточной чувствительности к кортизолу иммуннокмпетентных клеток.
Степень влияния минерала на тонус мускулатуры и бронхов, как и на их гиперреактивность до конца не ясна, поскольку не выявлено зависимости большинства показателей гомеостаза магния в организме от выраженности бронхообструктивного синдрома [37] и снижения форсированного выдоха за первую секунду в тесте с метахолином у лиц с экзогенным дефицитом минерала в организме [202]. Однако об активном участии магния в нарушении секреторной и экскреторной функции эпителия бронхов свидетельствует наличие достоверной связи между снижением бронхиальной проходимости и недостатком магния в конденсате выдыхаемого воздуха у больных хроническими обстуктивными заболеваниями легких [5]. Сульфат магния оказывает бронхорасширяющее действие, хотя и значительно уступает по клиническому эффекту другим препаратам, в связи с чем его применение в клинической практике не рекомендуется [14]. Более перспективным оказалось свойство сульфата магния снижать гиперреактивность бронхов к ацетилхолину и физической нагрузке при введении ингаляционным способом [37].
На примере взрослых больных подтверждено значение недостатка магния для формирования бронхиальной астмы. Оказалось, что нарушения клеточного гомеостаза магния, как и кальция, проявляющиеся внутриклеточным дефицитом магния и избытком кальция, а также снижением концентрации магния в суточной моче и конденсате выдыхаемого воздуха, выявляются не только у больных, но и у их практически здоровых кровных родственников [37].
Ниже представлена схема участия магния в патогенезе бронхиальной астмы, предложенная автором. Дефицит магния сопровождает бронхиальную астму и у детей [3], однако эта возрастная группа исследована меньше.
Следует заметить, что наличие магнийдефицитного состояния в организме наблюдается при многих заболеваниях: сердечно-сосудистой, нервной и эндокринной систем, вследствие чего указанные выше изменения магния нельзя считать патогмоничными для бронхиальной астмы. Магнийдефицитные состояния широко распространены в популяции [27, 54, 89]. Однако, среди больных бронхиальной астмой они встречаются, вероятно, более часто, чем в общей популяции. Так, при исследовании гомеостаза магния недостаток минерала был выявлен у 40% больных бронхиальной астмой и только у 11 % клинически здоровых лиц [ 157].
Таким образом, результаты исследований доказывают, что нарушению обмена магния принадлежит значительная роль в патогенезе бронхиальной астмы. Тем не менее клинические проявления таких нарушений у детей остаются не изученными.
Широкая распространенность цинкдефицитных состояний у населения позволяет считать их «общественной проблемой» современности [2, 29, 54, 89,190, 196]. Необходимость разработки путей профилактики и лечения таких состояний, а также определения надежных критериев их диагностики неоднократно подчеркивалась в докладах ВОЗ [208].
Как установлено в настоящее время, причины дефицита Zn не имеют исключительной связи с неполноценным питанием. Недостаток микроэлемента в организме сопровождает развитие многих заболеваний (онкологических, аллергических, аутоиммунных, инфекционных) и патологических состояний (нарушении всасывания, разнообразные иммунодефициты). Достаточно часто цинкдефицитное состояние является следствием избыточного поступления ксенобиотков (Cd, Pb), чем обусловлено его широкое распространение среди населения в экологически неблагополучных регионах. Среди других причин можно выделить природный недостаток цинка в определенных географических местностях, например, в странах Средиземноморья. Низкое содержание этого элемента имеет место и в большинстве регионов России [2, 47,54, 89, 208].
Разнообразные проявления недостатка микроэлемента в организме обусловлены многогранностью эссенциальной роли цинка. Установлено, что цинк влияет на разные виды обмена веществ: белкового, углеводного, жирового, минерального, гормонального, нуклеинового. Он необходим для нормального функционирования иммунной системы, большинства ферментов, способен изменять генетический аппарат клетки, оказывать влияние на чувствительность рецепторов к гормонам и цитокинам. Однако, несмотря на кофакторную роль этого микроэлемента более, чем для 300 ферментов, его точные функции в организме до сих пор неизвестны [54, 190, 208].
Имеющиеся на сегодняшний день результаты экспериментальных и клинических исследований свидетельствуют об участии цинка в процессах, имеющих существенное значение в патогенезе аллергических заболеваний.
На уровне клетки цинк проявляет себя конкурентным антагонистом Са, взаимодействуя с белком кальмодулином, осуществляющим контроль за содержанием кальция в клетке [79, 122, 189, 193]. Посредством участия в регуляции циклазных систем [122] цинк способен влиять на активность клетки, антиоксидантную защиту, проницаемость мембран, состояние их рецепции, передачу генетической информации. Все это обеспечивает определенную роль цинка в стабилизации мембран и предотвращении программированной гибели клетки — апоптоза [54, 110,122, 208].
В результате проведения анализа семейного и личного анамнеза наблюдавшихся детей было установлено следующее.
В семейном анамнезе 79 больных детей ( 73,1% ) имелись указания на существование у близких родственников пробанда аллергических заболеваний. При этом по линии матери в 28 ( 25,93%) семьях, только по линии отца — в 13 (12,04%) семьях, по линии матери и отца — в 38 ( 35,2%) семьях. В структуре заболеваний преобладала бронхиальная астма ( 37,95% ), несколько реже имелись указания на кожные проявления аллергии ( 35,19%) и еще реже — полли-ноз (21,30%).
Наследственная отягощенность неаллергическими заболеваниями включала эндокринную патологию ( сахарный диабет II типа, нарушение функции щитовидной железы и дисфункции репродуктивной сферы у родственников женского пола ) в семьях 48 детей ( 44,4%). Несколько реже имелись указания на хронические заболевания органов пищеварения ( в семьях 32 детей, 29,63% ), заболевания ЛОР- органов ( в семьях 20 детей , 18,52 % ), онкологические заболевания ( в семьях 18 детей, 16,7 %).
Антенатальное развитие 77 ( 71,3%) наблюдавшихся детей протекало в неблагоприятных условиях. Сведения об особенностях течения беременности у матерей этих детей представлены в табл. 3. Настоящая беременность у большинства матерей наблюдавшихся детей чаще всего осложнялась поздним гес-тозом и/или угрозой прерывания беременности. Однако, несмотря на значительную частоту осложненного течения данной беременности у матери, 104 из 108 детей родились на сроке 38 — 40 недель гестации, недоношенными родились только 4 ребенка ( 3,7%). Средний гестационный возраст недоношенных детей был равен 36,88 ± 0,43 недели. Пятеро из наблюдавшихся детей родились в состоянии асфиксии. У всех остальных детей в раннем неонаталыюм периоде осложнений не отмечалось. Путем кесарева сечения родились 25 детей (23,15 % ). С применением акушерских пособий родился один ребенок ( 0,9% ). Таким образом, 26 детей ( 24 %) родились с помощью оперативного вмешательства.
У 74 (68,5%) из наблюдавшихся нами детей, больных бронхиальной астмой, помимо основного заболевания, были сопутствующие заболеваниями других органов и систем (табл. 4).
Результаты исследования свидетельствуют, что у детей 2-й подгруппы чаще, чем у детей 1-й группы встречались хронический гастрит и хронический гастродуоденит (р 0,01), хронический пиелонефрит (р 0,02) и была тенденция к уменьшению частоты возникновения эпизодов ОРВИ, что в целом сопоставимо с распространенностью этих заболеваний в популяции московских детей в возрасте 4 лет и старше.
Отсутствие органической патологии сердечно-сосудистой системы (за исключением вегетососудистой дистонии, наблюдавшейся у большинства детей) обусловлено специальной направленностью отбора больных. Помимо этого, нами был проведен анализ проявлений аллергии у наблюдавшихся детей (табл. 5).
Результаты исследования, приведенные в табл.5, свидетельствуют о значительной частоте внелегочных проявлений аллергии у детей с бронхиальной астмой. Последняя выявлялась у 3/4 наблюдавшихся пациентов. Статистически значимое различие, за исключением пищевой аллергии, у детей двух сравниваемых подгрупп отсутствовало.
В табл.6 представлены сведения об особенностях экологии жилища и других факторов, способствующих формированию бронхиальной астмы у наблюдавшихся детей.
Результаты анамнеза, представленные в табл.10, свидетельствуют, что 3/4 наблюдавшихся детей проживали в неблагоприятной обстановке ( нарушение микроэкологии жилища), 1/3 детей были пассивными курильщиками. У 18 детей ( 16,7 %) бронхиальная астма развилась на фоне перенесенной пневмонии, либо пневмония возникла на фоне бронхиальной астмы.
Обращает на себя внимание и тот факт, что у 19 детей (17,6%) до дебюта бронхиальной астмы были указания на возникновение осложнений вакцинации в виде повышения температуры, местных реакций в месте введения вакцин, преходящие неврологические расстройства. Если учесть, что вакцинация проводилась не всем наблюдающимся больным, а только 72 из них, то частота реакций на вакцинацию зарегистрированы у 1/4 детей с бронхиальной астмой.
Маловероятно, что во всех этих случаях причиной побочных реакций на вакцинацию явились качество вакцин или технические погрешности процедуры вакцинации. Скорее всего, возникновение осложнений обусловлено особенностями организма детей основной группы. На это могут указывать и данные анамнеза о высокой отягощенности семей наблюдавшихся нами детей аллергическими заболеваниями, и высокая частота внелегочных проявлений аллергии у самих пациентов. С учетом частоты возникновения пневмонии и побочных реакций на вакцинацию, можно полагать, что у детей наблюдавшейся группы имел место эндогенный неблагоприятный преморбидный фон, способствующий возникновению данного иммунологического состояния.
Распределение обследованных больных детей в зависимости от тяжести бронхиальной астмы представлено в табл. 7.
В данном исследовании у детей раннего возраста на момент обследования доля тяжелой формы бронхиальной астмы оказалась значительно выше, чем у более старших. Эта особенность учитывалась при проведении дальнейшего анализа.
Исследование волос детей проводилось двумя методами — АЭС-ИП и НАА. Данные об общем количестве обследованных этими методами детей и распределение детей основной группы по форме бронхиальной астмы представлено в табл. 8.
В табл.9, представлены сведения о возрасте начала и продолжительности заболевания у обследованных нами детей, больных бронхиальной астмой. С учетом средней арифметической и ее ошибки, можно констатировать, что большинство обследованных нами детей имели относительно непродолжительный «стаж» заболевания, что согласуется с их возрастом.
В приведенной ниже табл. 10 представлены сведения о факторах, которые провоцировали у наблюдавшихся больных приступы бронхиальной астмы. Приступы бронхиальной астмы провоцировались разными факторами, как причинно-значимыми, так и триггерами (в первую очередь, ОРВИ). У значительной части детей приступы бронхиальной астмы возникали после вдыхания измененного воздуха ( влажного, холодного ), эмоционального стресса, физической нагрузки, что свидетельствует о гиперчувствительности бронхов.
Состояние макро- и микроэлементного обмена в организме зависит от многообразных факторов, часть из которых до сих пор не определена. Помимо изменений, обусловленных развитием хронического заболевания, имеют значение особенности питания и бытовое микроокружение человека, биогеохмические особенности и индустриальное загрязнение местности его проживания. Вследствие вышеперечисленных причин, дисбаланс макро- и микроэлементного часто встречается у самых разных слоев населения современных городов [2, 27, 54, 74, 89, 196, 208]. Все это диктует необходимость сопоставления результатов исследования волос детей, больных бронхиальной астмой, с данными о частоте отклонений в макро- и микроэлементном составе волос среди детской популяции в целом с целью оценки специфичности обнаруженных изменений для бронхиальной астмы.
Мы сравнили имеющиеся показатели детской популяции 1 — 8 лет, проживающей в экологически благополучном административном округе г. Москвы [ 98 ], с данными больных астмой детей, обследованных нами методом АЭС-ИП. Отклонения в элементном составе волос и обеих группах были рассчитаны по одним и тем же нормативам. Результаты сравнения представлены в табл.7.
Мы также провели сопоставление результатов обследования детей, больных бронхиальной астмой с имеющимися данными Центра биотической медицины о распространенности накопления и недостатка отдельных элементов в детской популяции [89]. Результаты исследования представлены в табл. 8.
Исследование показало, что в отличие от детской популяиии г. Москвы, среди больных бронхиальной астмой был более широко распространен дисбаланс Zn, К, Si. В то же время, отклонения в содержании Са, Си, Fe чаще встречались в детской популяции в возрасте от 1 до 8 лет, что может быть обусловлено повышенным расходом указанных элементов в период роста ребенка и становления у него иммунной и кроветворной систем. Изменения в содержании Сг и Ni, способствующих развитию детской астмы [66], носили единичный характер (рис.2).
Обращало на себя внимание, что отклонений в минеральном и микроэлементном статусе волос не было выявлено только у двух 73 ( 2,7 % ) детей, обследованных нами методом АЭИ-ИП. Редко встречался и изолированный дефицит или избыток какого-либо элемента ( 3 ребенка, 4,2%). Подавляющее большинство больных детей имели отклонения в содержании от двух до десяти элементов (табл.8).
Данные о распространенности отклонений Au, Br, С1, Ей, La волосах детской популяции России в настоящее время отсутствуют, что не позволило провести сравнительный анализ по этим элементам.
Наиболее часто встречавшиеся сочетанные отклонения, иллюстрирующие характер минерального и микроэлементного статуса больных бронхиальной астмой, представлены ниже в табл. 9. и на рис. 3.
У детей раннего возраста, помимо представленных в табл.9 отклонений, отмечалась высокая частота сочетанного дисбаланса таких элементов, как марганца и магния (4- Mg— 4- Мп), достигающая 85%.
Сравнительное исследование элементного состава волос детей разного возраста, больных бронхиальной астмой
В литературе мы не обнаружили сведений об особенностях накопления макро- и микроэлементов в волосах детей разного возраста, больных бронхиальной астмой. Обнаруженные нами выше отличия в элементом составе волос больных детей 1—3 лет и 4 — 8 лет послужили предпосылкой для исследования возрастных особенностей макро- и микроэлементного дисбаланса при бронхиальной астме.
Поскольку группа детей первых трех лет жизни по тяжести бронхиальной астмы была однородной, а более старших — нет, мы сформировали из детей 4 — 8 лет новую подгруппу, сопоставимую с первой по клинической картине заболевания. Бронхиальная астма у детей обеих групп была среднетяжелой и тяжелой. Длительность заболевания составила в группе детей 1 — Зх лет 0,95 ± 0,21 лет, 4 — 8 лет — 2,78 ± 0,22 года. Все дети в последние 5 месяцев (среднее время роста пробы) проходили курсы стационарного лечения по экстренным показаниям в связи с приступом астмы.
Результаты сравнительного анализа элементных профилей при бронхиальной астме у детей разных возрастных групп представлены в табл.16.
Результаты исследования, представленные в табл.16, свидетельствуют, что у больных астмой детей в возрасте 1 — 3 лет, по сравнению с детьми 4 — 7 лет, достоверно чаще в волосах встречался недостаток Mg, Со, Fe, Мп и Si. Аналогичные результаты были получены и при сравнении частоты отклонений в макро- и микроэлементном составе волос у больных детей разных возрастных групп (рис. 8 ).
Проведенный анализ выявил существенное различие в макро- и микроэлементном профиле волос у детей разного возраста, больных бронхиальной астмы. У детей первых трех лет жизни наблюдался значительное снижение содержания в волосах Mn, Со, Fe, Mg при отсутствии различий с возрастной нормой в содержании Si. В то же время у детей старше 4х лет был выявлено существенное повышение Si в волосах. Следует заметить, что в норме у здоровых детей первых трех лет жизни, по сравнению с детьми более старшего возраста, содержание в волосах Со и Mg более высокое [89]. Таким образом, выявленное нами у детей младшей возрастной группы, по сравнению с детьми 4 — 7 — летнего возраста, сниженное содержание Со и Mg свидетельствует о более глубоком недостатке этих элементов у больных бронхиальной астмой в первые три года жизни.
Изменения макро- и микроэлементного состава волос при бронхиальной астме у детей разного возраста можно проиллюстрировать следующими тремя примерами.
Больная Маша С, 2,5 года, история болезни № 22305/ 99.
Клинический диагноз: Бронхиальная астма, средней тяжести, период обострения. Атопический дерматит, распространенная форма, непрерывно-рецидивирующее течение, круглогодичный аллергичекий ринит.Поливалентная аллергия.
Жалобы при поступлении: слизистое отделяемое из носа, высыпания на коже (в области щек, ягодиц), затруднение дыхания. Указанные явления появились за неделю до поступления.
Анамнез жизни. Ребенок из семьи с наследственной предрасположенностью к аллергии ( мать страдает с детства аллергодерматозом, у деда по линии отца бронхиальная астма).
Бытовые условия удовлетворительные.
Девочка от первой беременности, осложненной на всем протяжении угрозой прерывания , в конце данной беременности мать перенесла ОРВИ. Родилась в срок, роды протекали без осложнений.
Период новорожденности протекал без особенностей. Грудное вскармливание до 9 месяцев. В возрасте одного месяца впервые появились высыпания , сопровождающиеся мокнутием, сначала на лице, затем распространились по всему телу. Обострения экссудативно-катарального диатеза на первом году наступало после введения большинства новых продуктов. В дальнейшем периодически отмечались обострения заболевания , главным образом, в летнее время . Болела ОРВИ до 5 раз в год . Полного курса вакцинации провести не удалось После введения вакцин наблюдалось обострение экссудату то-катарального диатеза.
После года возникали проявления пищевой (после приема в пищу цитрусовых, орехов, любых продуктов с красителями, сладкой и жареной пищи), эпи-дермальной (на шерсть кошки ), пыльцевой ( преимущественно на луговые травы) и бытовой (на домашнюю пыль ) аллергии . Контакт с аллергеном вызывал обострение атопического дерматита, риноконъюнктивального синдрома и приступы бронхиальной астмы. Наиболее выраженные проявления аллергии отмечались в летний период, значительно реже — осенью.
Анамнез заболевания. Впервые приступ затрудненного дыхания возник в 2 года, на фоне ОРВИ. В дальнейшем частота приступов была около 2 раз в неделю, по экстренным показаниям госпитализировалась в стационар, во время первой из них был установлен диагноз: «Бронхиальная астма». На фоне лечения эуфиллином и ингаляционных бронхоспазмолитиков отмечался положительный эффект. Течение заболевания сопровождалось ночными обострениями, не нарушающими сна. Приступы возникают на фоне ОРВИ, после вдыхания влажного воздуха, нарушения диеты, контакта с шерстью кошки и или бытовой пылью, с пыльцой луговых трав. По продолжительности отмечаются как короткие, так и длительные (до 2 дней на фоне ОРВИ) обострения. За год до проведения исследования волос девочка получала кетотифен, на фоне которого не было отмечено сухцественных изменений в клинической картине болезни. Базисной терапии в течение этого времени не было ( из-за нежелания родителей ). В качестве бронхорасширяющей терапии применялся сальбу-тамол и эуфиллин.
При поступлении: состояние удовлетворительное, сознание ясное. Одышки, втяжения уступчивых мест, катаральных явлений в носоглотке не отмечено. Тахипное, тахикардия отсутствовала. В легких выслуишвачись единичные сухие хрипы с обеих сторон. Печень выступала из-под края реберной дуги на 1 см, болезненности при пальпации не отмечалось, все физиологические отправления были нормальными.
Данные лабораторных исследований. В общем анализе крови: НЬ 119 г /л, лейкоциты 13 xlO9 /л; и/я нейтрофилы 1% 109 /л , с/я 54% 109 /л, лимфоциты 29%- 109/л, моноциты б%- 109/л, СОЭ 3 мм/ ч. Эозинофилы 10 % 109 /л. Биохимический анализ крови: общий белок 70 г/л , серомукоид 0,140 ед., ЩФ — 276Ед/л , определялся СРВ, холестерин 4,7ммоль/л; АЛТ68 Ед/л, ACT66 Ед/л, ЛДГ 480 Ед/л; К 4,0 ммоль/л, Na 140 ммоль/л, Р 1,14 ммоль/л . Уровень иммуноглобулина класса А- 60, G — 895, М-106 мг %, что находится в пределах возрастной нормы.
В посеве со слизистых ротовой полости патогенной и кандидозной флоры не обнаружено.
При исследовании общего и специфических Ig Е выявлена сенсибилизация к пыльцевым аллергенам: тимофеевки, ежи, овсянннице, амброзии, домашней пыли (+ +); сенсибилизации к другим неинфекционным аллергенам не обнаружено. Из группы инфекционных аллергенов выявлена слабая сенсибилизация к грибковым аллергенам рода Penicillium и Altemarium ( ). Уровень общего иммуноглобулина Е в крови был повышен: 135 кЕд/л (при норме до 24 кЕд/л) .
При рентгенологическом исследовании органов грудной клетки выявлено усиление сосудистого рисунка в медиальных отделах легких при отсутствии очаговых и инфильтративных изменений.
При ультразвуковом исследовании органов брюшной полости обнаружены признаки реактивного изменения поджелудочной железы и уплотнение пе-рипортального тракта.
На элетрокардиограмме выявлялась выраженная синусовая тахикардия, вертикальное положение электрической оси сердца, высота и длительность интервалов зубцов соответствовала норме (РО — 0,14 ; QRS — 0,08 ; QRST -0,30%
Проба волос для исследования содержания макро и микроэлементного состава была взята спустя месяц после последнего обострения бронхиальной астмы. Результаты анализа методом АЭС-ИП в сравнение с данными исследования популяции г. Москвы в возрасте 1-3 лет и группы здоровых детей аналогичного возраста приведены в табл.17.
В волосах девочки было выявлено повышение содержания калия, умеренное снижение цинка, селена, железа, магния и значительное — марганца.
Таким образом, изменения макро- и микроэлементного профиля волос девочки характерны для выявленных нами особенностей элементного профиля волос детей раннего возраста, больных бронхиальной астмой.
Ниже приведены истории болезни и результаты исследования волос ( методы АЭС-ИП и НАЛ) двух детей 4 и 8 лет, больных бронхиальной астмой.
источник
Астма – это состояние, сопровождающееся удушьем вследствие спазма мускулатуры бронхов и сужения просвета бронхиального дерева. Причинами его развития может служить непосредственное воздействие аллергена, что наблюдается наиболее часто, эндогенных провоцирующих факторов или отдельно выделяемая патология левых отделов сердца. В последнем случае состояние называется сердечной астмой. Оно встречается довольно редко и в основном астматический приступ наблюдается при бронхиальной астме.
Одним из наиболее важных факторов, определяющих правильное лечение, является этиология, то есть причина, спровоцировавшая развитие болезни.
При бронхиальной астме имеют значение как внешние, так и внутренние обстоятельства. Именно их взаимодействие часто приводит к обострению заболевания.
Однако бывают ситуации, когда приступ начинается без видимого воздействия аллергенов извне. В тех случаях, когда внешний источник, вызвавший реакцию, не обнаружен, принято говорить об астме эндогенного генеза.

- резкие перепады температур – переохлаждение;
- острый или длительный стресс;
- сильные физические нагрузки;
- инфекционные заболевания.
На последнем факторе следует остановиться подробнее, так как именно его присутствие наблюдается наиболее часто при бронхиальной астме эндогенного характера. Особенно опасны вирусные болезни дыхательных путей как состояние, напрямую влияющее на иммунные реакции в области бронхов и часто на их нервную регуляцию. В случае атопического (аллергического) происхождения болезни реактивность иммунитета также играет основополагающую роль в механизме развития приступа.
Неудивительно, что важным аспектом борьбы с астмой является нормализация работы иммунной системы и повышение сопротивляемости к инфекционным агентам. Известно, что польза витаминов при астме огромна.

- аскорбиновая кислота;
- витамины группы В;
- витамины А и Е;
- группа витамина P;
- витамин D.
В таблице подробно расписано биологическое действие этих веществ для улучшения состояниях больных бронхиальной астмой.
Таблица – Значение витаминов при лечении астмы
| Витамин | Химическое название | Действие на симптомы бронхиальной астмы |
|---|---|---|
| С | Аскорбиновая кислота | Ослабление сезонных проявлений. Снижает риск возникновения анафилактического шока и отека Квинке. Некоторые данные свидетельствуют об уменьшении под действием этого витамина содержания гистамина (основного вещества, вызывающего аллергические реакции) в крови |
| В | Никотиновая кислота (B3) | Снижение интенсивности астматических хрипов и скорости развития аллергической реакции |
| Пиридоксин (В6) | Нормализует обмен гистамина. Может быть снижен у больных, длительно принимающих брохорасширяющие препараты | |
| Цианокобаламин (В12) | Облегчение дыхательных движений во время приступа. Способствует благоприятному преодолению контакта с аллергенами и физических нагрузок. Уменьшает проявление аллергии к яичному желтку | |
| Е | Токоферол | Снижает продукцию медиаторов воспаления. Способствует уменьшению кашля, выраженности свиста, затрудненности дыхания. Улучшает функционирование сердца. Употребляется в комбинации с витамином А (ретинолом) |
| Р | Рутин | Нормализует реактивность иммунной системы |
| D | Кальциферол | Уменьшает восприимчивость дыхательных путей к аллергенам, снижает воспалительные реакции |
Прежде чем начинать употреблять какие-либо витаминные препараты или комплексы при бронхиальной астме, необходимо проконсультироваться с врачом. Аллергические реакции весьма вариабельны, поэтому назначение витаминов рассматривается в каждом отдельном случае индивидуально.
Помимо вышеуказанных полезных соединений существуют определенные микроэлементы и химические вещества, которые также показаны, когда у больного может развиться астматический приступ.
В медицине известны следующие клинические данные о влиянии различных компонентов на течение заболевания:
- Цинк (Zn) снижает восприимчивость бронхов к воздействию раздражающих веществ-аллергенов. Его дефицит обнаруживается у многих людей с нарушениями в работе дыхательной системы.
- При приеме селена (Se) по 100-200 мкг в сутки наблюдаются значимые улучшения в состоянии больных.
-
Магний (Mg) обладает некоторыми спазмолитическими свойствами, расслабляет мышцы. Снижает восприимчивость организма к аллергенам. Его в некоторых случаях при бронхиальной астме даже назначают внутривенно.
- Молибден (Mo) специфически снижает реактивность организма при аллергических реакциях на сульфиты, которые содержаться, к примеру, в яйцах или вине.
- N-ацетилцистеин разжижает мокроту.
- Теобромин (содержится в продуктах из какао) может применяться в качестве бронхорасширяющего вещества.
Отдельно стоит сказать о применении незаменимых жирных кислот ввиду их выраженной противовоспалительной активности. Они препятствуют спазмированию бронхов и их набуханию. К данной группе веществ относятся:
- Линолевая кислота;
- Гамма-линоленовая кислота.

Известно, что олеиновая кислота, та самая, что входит в состав оливкового масла, оказывает тормозное действие на высвобождение гистамина. Данный биогенный амин вырабатывается особыми высокоспециализированными элементами иммунной системы – тучными клетками. Они содержаться в тканях, в крови же их роль играют другие клетки из лейкоцитарного ростка – базофилы.
Любые синтетические микроэлементы, как и витамины при астме, назначаются лишь врачом на основе опроса и осмотра больного, тщательной проработки анамнеза его жизни и анализа лабораторных данных.
Баланс всех компонентов человеческого организма весьма важен для поддержания здоровья и любое вмешательство должно быть обдуманным, главное – обоснованным.
Прием любых лекарственных средств неизбежно сопряжен с риском возникновения различных сопутствующих нежелательных эффектов. В связи с этим к приему аптечных, а иногда и употреблению в натуральном виде некоторых витаминов следует относиться с осторожностью. Организм, который страдает какой-либо из форм аллергии, в большей мере подвержен также развитию пищевой аллергии.
К применению различных витаминов существуют следующие известные противопоказания:
- болезни, связанные с патологией крови, и особенно эритроцитов (гемохроматоз, талассемия, сидеробластная анемия);
- повышенная экскреция с мочой оксалатов;
- наличие камней в почках;
- сахарный диабет.
- повышенное содержание в крови кальция;
- атеросклероз;
- мочекаменная болезнь;
- хроническая сердечная недостаточность;
- беременность и период кормления;
- повышенное содержание фосфора в крови.

- нежелательно употреблять детям до 12 лет;
- инфаркт миокарда, острая форма.
- беременность, первый триместр;
- не следует принимать детям до 3 лет.
Также противопоказанием для приема любых витаминов можно назвать индивидуальную непереносимость какого-либо из них. Здесь перечислены и те противопоказания, при которых можно употреблять препарат, но с осторожностью.
К побочным эффектам приема большинства из витаминов можно отнести:
- тошноту;
- повышение секреции желудочного сока;
- общую слабость или наоборот повышение возбудимости центральной нервной системы;
- головокружение;
- дерматит;
- местную реакцию в виде появления боли в области введения или инфильтрата;
- гипервитаминоз.
У каждого витамина имеются свои специфические побочные эффекты при несоблюдении прописанных дозировок:
- аскорбиновая кислота может вызвать серьезные изменения в показателях крови, обмене веществ и функциях сердца;
-
пиридоксин – онемение в области конечностей, уменьшение лактации у женщин, изредка судороги;
- никотиновая кислота при передозировке ударяет по желудочно-кишечному тракту и печени;
- при повышенном содержании в организме витамина В12 страдает сердце и головной мозг, увеличивается свертываемость крови;
- очень остро проявляется гипервитаминоз кальциферола: начиная от нарушений пищеварения и функции почек, заканчивая болями в костях и воспалительными процессами в поджелудочной железе.
Повышение иммунной сопротивляемости организма является одним из главных факторов успешного преодоления заболевания. Помочь в этом может прием витаминных комплексов, однако обязательно нужно учитывать противопоказания и индивидуальные особенности организма, чтобы получить максимальную пользу и избежать побочных эффектов.
источник
В клинике госпитальной терапии Санкт-Петербургского государственного медицинского университета им. акад. И.П. Павлова проводилось комплексное исследование метаболизма магния и его антагониста кальция у 133 больных БА. У обследованных пациентов было обнаружено достоверное снижение внутриклеточной концентрации Mg и увеличение Са наряду с уменьшением суточной экскреции магния с мочой. По данным нагрузочных тестов с сульфатом магния у больных отмечалась высокая задержка этого катиона (в среднем 54% от вводимой дозы). Полученные результаты свидетельствуют о том, что дефицит магния у пациентов с бронхиальной астмой имеет место не только в форменных элементах крови, но и в клетках, принимающих участие в развитии воспаления.
Соотношение внутриклеточных концентраций кальция и магния достоверно (р
Выполненные исследования послужили основанием для назначения больным бронхиальной астмой ингаляций аэрозоля сульфата магния. Было установлено, что препарат достоверно по сравнению с плацебо снижает неспецифическую гиперреактивность бронхов и секреторную активность тучных клеток, улучшая непосредственные и отдаленные результаты лечения больных бронхиальной астмой атопического генеза и физического усилия.
Таким образом, нарушения минерального обмена, по-видимому, являются одним из механизмов формирования синдрома гиперреактивности бронхов и бронхообструктивного синдрома у пациентов с бронхиальной астмой.
Помимо ионов калия, натрия, кальция и магния, в регуляции бронхиальной проходимости и различных фаз реакций гиперчувствительности принимают, вероятно, микроэлементы (МЭ).
В исследованиях, выполненых in vitro и in vivo, установлено, что наиболее чувствительны к дефициту меди и цинка Т-киллеры и Т-хелперы, макрофаги и нейтрофилы, в меньшей степени — В-лимфоциты. У экспериментальных животных, получавших диету с низким содержанием данных МЭ, и у больных с генетически детерминированными нарушениями обмена меди и цинка наблюдалось развитие Т- и В-иммунодефицитов, проявляющихся инфекционными поражениями внутренних органов, в том числе и легких. Селективный дефицит цинка приводил к гипоплазии тимуса, снижению активности тимолина и развитию Т-клеточного иммунодефицита. Полученные данные, вероятно, можно объяснить тем, что цинк регулирует синтез нуклеиновых кислот, активной формы тимолина и стимулирует Т-лимфоциты.
При изучении показателей обмена микроэлементов у больных затяжной пневмонией найдено снижение концентрации важнейших биоэлементов, в том числе меди и цинка, в сыворотке крови, сочетающееся с Т-и В-клеточным дисбалансом и депрессией ферментов метаболизма ксенобиотиков. Коррекция содержания МЭ с помощью препаратов растительного происхождения увеличивала эффективность действия иммуномодуляторов и способствовала более быстрому восстановлению иммуноэнзиматического статуса. На основании полученных результатов сделан вывод о том, что изменение микроэлементного состава крови является одной из причин формирования вторичных иммунодефицитных состояний при заболеваниях органов дыхания.
В серии исследований продемонстрировано дозозависимое торможение физиологическими концентрациями цинка Ig Е-опосредованного освобождения гистамина и лейкотриена С4 из тучных клеток и базофилов. По мнению авторов, ионы Zn, депонированные в гранулах мастоцитов, выделяются в процессе секреции медиаторов, выполняя роль регулятора по принципу отрицательной обратной связи. Полученные результаты обусловлены мембраностабилизирующим эффектом цинка, способностью этого катиона «маскировать» рецепторы для Ig E на поверхности тучных клеток, инактивировать фосфолипазу А2, а также его конкурентный антагонизм с кальцием. Последним объясняется устранение экспериментального аллергического бронхоспазма добавками солей Zn.
Таким образом, результаты цитируемых выше исследований свидетельствуют о том, что МЭ участвуют в регуляции клеточного и гуморального звеньев иммунитета, процесса сенсибилизации, интенсивности патохимической и патофизиологической стадий аллергических реакций немедленного типа, которым принадлежит существенная роль в формировании воспалительных изменений бронхов и легких.
Заслуживают внимания данные о способности МЭ контролировать активность перекисного окисления липидов (ПОЛ) и антиоксидантной защиты. Известно, что медь, цинк и марганец входят в состав супероксиддисмутазы, селен-глютатионпероксидазы. Эти ферменты являются компонентами внутриклеточной антирадикальной системы. Церулоплазмин, один из основных внеклеточных антиоксидантов, относится к классу медьсодержащих протеинов. Цинк, образующий химические связи с сульфгидрильными группировками белков, фосфатными остатками фосфолипидов и карбоксильными группами сиаловых кислот, обладает мембраностабилизирующим действием. Избыток ионизированного железа оказывает прооксидантное действие. Дефицит меди и цинка приводит к накоплению свободных радикалов в тканях.
Таким образом, нарушение обмена МЭ является одним из факторов, способствующих избыточной активации ПОЛ, участвующей в формировании воспаления бронхов и бронхиальной обструкции у больных бронхиальной астмой и хронической обструктивной болезнью легких.
источник
Бронхиальная астма – поражение верхних дыхательных путей, в основе которого лежит сужение бронхов. При астме отмечается их чрезмерная реактивность, выраженный воспалительный процесс, повышенная выработка слизи, что и приводит к нарушениям дыхательной функции и приступам удушья. Бронхиальная астма – хроническое заболевание, протекает длительно и, соответственно, наиболее эффективно корректируется приёмом специальных медикаментов на фоне коррекции образа жизни.
Астма часто (хотя и не всегда) связанас воздействием аллергенов (Morris, 2012).
Распространённость бронхиальной астмы зависит от многих факторов, в том числе природных, климатических. Известно, что это – болезнь индустриально развитых стран.
Болезнь поражает людей всех возрастов, но чаще начинается в детстве. У взрослых заболеваемость примерно 1%.
Средняя распространённость астмы у взрослых примерно 1%. И в нашей стране, и за рубежом отмечается рост заболеваемости. Этому есть ряд причин: рост хронических заболеваний лёгких, повышение аллергизации населения из-за индустриализации, расширением применения сельскохозяйственной, бытовой, промышленной химии, промышленность и быт, загрязнением окружающей, активное применение вакцин, сывороток, антибиотиков и т.д.
Бронхиальный спазм
При астме в бронхах отмечается повышенная чувствительность к активаторам воспаления (иммуноглобулинам, антителам, гистамину), что ведет к спазму и сужению бронхов (Miller, 2001).
Воспалительные явления в дыхательных путях
При астме воспалительная реакция в бронхах носит чрезмерный, выраженный характер иногда даже на безвредные в обычных условиях вещества. В бронхах отмечается отёк, повышенная выработка слизи, что приводит к сужению дыхательных путей (Lemanske, 2010). В результате развиваются характерные приступы удушья.
Аллергия и повышенная чувствительность
Аллергия представляет собой чрезмерную иммунную реакцию и часто лежит в основе астмы.В качестве аллергенов могут выступать, казалось бы, нейтральные вещества внешней среды. В последнее время всё большее значение придаётся пищевой аллергии и непереносимости (Young, 2011; Wang, 2011).
Табачный дым
У курящих риск развития астмы выше. У астматиков, которые бросают курить, отмечается уменьшение тяжести и частоты приступов астмы (Stapleton, 2011).
Профессиональные вредности
Профессии, при которых риск астмы выше:
— деревообработка
-производство моющих средств
— некоторые медицинские специальности
-пищевая промышленность (PubMed Health, 2011; Bakerly, 2008; Vandenplas, 2011).
Лекарства
Некоторые лекарства, в том числе нестероидные противовоспалительные (НПВП), антигипертензивные препараты (ингибиторы АПФ), могут провоцировать развитие астмы (Sanfiorenzo, 2011).
Хронические заболевания
Хронический ринит, синусит / риносинусит, гастроэзофагеальная рефлюксная болезнь (ГЭРБ), хроническая обструктивная болезнь лёгких (ХОБЛ), гормональный дисбаланс, ожирение, депрессия и нервозность провоцируют развитие астмы. Есть данные о том, что стресс утяжеляет течение астмы (Yonas, 2012).
Основные рекомендации при бронхиальной астме
Консультация аллерголога
Людям с астмой необходимо пройти тестирование на выявление аллергенов и, насколько возможно, ограничить контактирование с выявленными аллергенами.
Упражнения
Предварительные данные показывают, что йога и дыхательные упражнения облегчают течение астмы (Vempati, 2009; Mekonnen, 2010). Основной рекомендацией при бронхиальной астме является регулярность их проведения.
Лечение фоновой болезни
Рекомендацией при бронхиальной астме можно считать лечение фонового воспалительного заболевания (бронхолёгочного или ЛОР, других болезней, провоцирующих астму). Например, лечение гастроэзофагеальной рефлюксной болезни (ГЭРБ) уменьшает количество обострений и улучшает качество жизни астматика (Littner, 2005).
Противостояние стрессу
Полноценный отдых и противостояние стрессу также рекомендованы при бронхиальной астме. При частых приступах астмы развивается повышенная тревожность и депрессия у пациентов, в свою очередь тревожность, стрессы утяжеляют астму (Wright, 2011).
Питание и диета при бронхиальной астме. Что же при бронхиальной астме применяют и назначают
Было замечено, что люди (независимо от состояния здоровья), которые едят недостаточно фруктов и овощей, больше подвержены заболеваниям лёгких. Исследование показало, что у пациентов, у которых в питании при бронхиальной астме было меньше фруктов и овощей, приступы удушья возникали чаще (Gilliland, 2003). Поэтому при бронхиальной астме рекомендацией является сбалансированное питание с их достаточным количеством.
Кроме того, установлено, что здоровая, богатая антиоксидантами диета при бронхиальной астме облегчает течение болезни. Например, три исследования показали, что у детей, которые следуют средиземноморскому типу питания (преимущественно растительные продукты, такие как фрукты, овощи, цельные зерна, бобовые и орехи, морепродукты и ограниченное потребление красного мяса), меньше бронхолёгочных заболеваний, реже устанавливается диагноз бронхиальной астмы и аллергического ринита (Chatzi, 2009; Arvaniti, 2011; Grigoropoulou, 2011). Ещё одно исследование установило, что тяжесть заболевания снижается и у взрослых при переходе на средиземноморский тип питания при бронхиальной астме (Barros, 2008).
Ожирение связано с астмой (Boulet, 2011).У астматиков с избыточным весом его снижение приводит к улучшению дыхательной функции (Maniscalco, 2008). Таким образом, рекомендацией при бронхиальной астме является коррекция избыточного веса.
Несколько популяционных исследований показало, что любители яблок реже болеют астмой. По-видимому, полифенолы, антиоксиданты оказывают защитное действие на бронхолёгочную систему (Boyer, 2004; Hyson, 2011). Добавьте яблоки в свой рацион питания при бронхиальной астме.
Нутриенты, которые применяют при бронхиальной астме
Витамин D играет важную роль в регуляции работы иммунной системы и развитии воспалительной реакции. Данные лабораторных исследований на моделях астмы у животных показали, что витамин D снижает чрезмерную реакцию бронхов на аллергены, способствует снижению воспалительной реакции (Taher, 2008; Damera, 2009).
Исследования, проведённые среди больных, показали, что при низких уровнях витамина D в крови заболевание протекает тяжелее, приступы происходят чаще, по сравнению с пациентами, которые применяют при бронхиальной астме этот витамин (Chinellato, 2011; Sutherland, 2010; Searing, 2010).
Наблюдательные исследования показали, что если беременным женщинами назначают при бронхиальной астме витамин D, рождаются дети с более низкими рисками бронхолёгочных заболеваний и астмы по сравнению с женщинами с дефицитом витамина (Devereux, 2007; Erkkola, 2009; Miyake, 2010a).
Исследование детей с астмой различной степени тяжести (от лёгкой до умеренной) показало, что низкий уровень витамина D связан с повышенным риском утяжеления заболевания и повышением частоты обострений астмы в течение ближайших 4 лет (Brehm, 2010).

Для того чтобы окончательно установить, есть ли эффект от применения витаминаD при бронхиальной астме, в настоящий момент в Национальном институте здоровья (clinicaltrials.gov) проводятся два соответствующих исследования. Одно клиническое испытание у подростков и взрослых с астмой проверяет, снижает ли приём витамина D риск перехода инфекционных заболеваний в астму (NCT00978315). Второе исследование у взрослых изучает, помогает ли приём витамина D предотвратить приступы, если его назначают при бронхиальной астме по сравнению с плацебо (NCT01248065).
При бронхиальной астме применяют антиоксиданты
Ряд исследований показал, что, если применяют при бронхиальной астмеантиоксиданты, такие как витамины С, Е, флавоноиды и селен, степень бронхоспазма снижается.
Витамин Е обладает антиоксидантными и противовоспалительными свойствами, подавляет выработку активаторов воспаления (цитокинов, ингибирует экспрессию гена IL-4) (Li-Weber, 2002).
Исследования показали, что, если при бронхиальной астме назначают витамин Е, отмечается уменьшение таких симптомов, как свистящее дыхание, кашель и затруднённое дыхание (Litonjua, 2012).
Некоторые исследования показывают, что недостаток витамина Е у мамы опасен повышенным риском заболеваний лёгких у новорождённых и детей (Miyake, 2010b; Litonjua, 2006), повышенным риском развития астмы у детей в возрасте до 5 лет (Devereux, 2006).
Исследование особенностей питания населения, питания при бронхиальной астме и экспериментальные работы говорят о связи между низким уровнем витамина C и риском развития заболевания.
В экспериментах на животных установлено, что применение витамина С при аллергии снижает раздражение и повышенную чувствительность дыхательных путей, уменьшает количество воспалительных клеток в бронхах (Jeong, 2010).
Одно исследование продемонстрировало, что дети с бронхиальной астмой отмечают облегчение состояния при повышенном потреблении омега-3 жирных кислот, витамина С и цинка. Питательные вещества обладают более выраженным эффектом, если их применяют при бронхиальной астме все три одновременно, чем когда используются по отдельности (Biltagi, 2009).
Ещё одно исследование, в котором принимали участие 8 пациентов, показало, что, если при бронхиальной астме назначают 1500 мг витамина С в день в течение двух недель, значительно улучшается течение заболевания по сравнению с больными, получавшими плацебо (Tecklenburg, 2007).
Полиненасыщенные жирные кислоты применяют при бронхиальной астме
Выделяют две основные группы полиненасыщенных жирных кислот (ПНЖК):омега-3и омега-6. Источники омега-3 – жир тушки рыбы, масло семян льна. Омега-6 кислоты содержатся в растительных маслах (подсолнечном, кукурузном).
В питании современного человека отмечается недостаток противовоспалительных омега-3 жирных кислот и избыток омега-6 кислот, которые провоцируют и поддерживают воспалительную реакцию, что создаёт благоприятные условия для развития астмы (Black, 1997).
Экспериментальные исследования показывают, что высокое потребление рыбы может уменьшить риск астмы (Laerum, 2007; Miyamoto, 2007), а у любителей растительных масел и маргарина риск заболевания выше (Nagel, 2005).
Ряд исследований свидетельствует, что диета при бронхиальной астме с высоким потреблением омега-3 жирных кислот снижает тяжесть заболевания (Mickleborough, 2006; Schubert, 2009).
Селен в диете при бронхиальной астме
Исследования показали, что при астме отмечается дефицит селена (Qujeq, 2003; Allam, 2004; Rubin, 2004).
Проведено несколько исследований эффектов селена, если его назначают при астме.
Одно исследование показало, что приём 200 мкг селена в день позволяет снизить дозировку гормонов-кортикостероидов (если была необходимость их назначения) (Gazdik, 2002).
Другое исследование установило значительное клиническое улучшение, если при бронхиальной астме назначают даже 100 мкг селена в день (Allam, 2004).
В 2007 г. исследование 26 больных продемонстрировало, что, если при бронхиальной астме применяют 200 мкг селена в день в течение 16 недель, улучшаются функции лёгких и качество жизни (Voicekovska, 2007).
Ещё одно исследование показало, что добавление селена в питание при бронхиальной астме улучшает качество жизни, однако изменений в функционировании лёгких отмечено не было (Shaheen, 2007).
Цинк в питании при бронхиальной астме
Два исследования показали, что более высокое потребление цинка женщинами во время беременности может защитить ребёнка от лёгочных заболеваний и бронхиальной астмы (Litonjua, 2006; Devereux, 2006).
Ещё одно исследование показало, что у людей с эпизодами свистящего дыхания, астмой и тяжёлыми заболеваниями с нарушениями функций лёгких отмечаются низкие уровни цинка в мокроте (Jayaram, 2011).
Исследование лабораторных животных (мышей, предрасположенных к аллергиям) показало, что добавление цинка защищает дыхательные пути от раздражающего действия аллергенов (уменьшает выброс активаторов воспаления цитокинов, иммуноглобулинов Е), уменьшает чрезмерную раздражительность бронхов (Morgan, 2011).
Установлено, что магний снимает спазмы и помогает расслабить мышцы бронхов (Gourgoulianis, 2001).
У пациентов с астмой различной степени тяжести (от лёгкой до умеренной) при потреблении 340 мг магния ежедневно в течение 6,5 месяца значительно снизилась реактивность бронхов, улучшились функции лёгких, течение астмы, качество жизни по сравнению с группой, принимавших плацебо (Kazaks, 2010).
Два других исследования среди детей с астмой от лёгкой степени до умеренной показали такой же положительный эффект добавок магния на течение астмы (Bede, 2003; Gontijo-Amaral, 2007).
Магний назначается не только в виде добавок, но и внутривенно при астме. Недавний обзор 16 клинических испытаний подтвердили пользу и безопасность использования внутривенного введения сульфата магния при тяжёлых обострениях (Song, 2012).
Куркумин, жёлтый пигмент в куркуме (находится в высокой концентрации в соусе карри), оказывает мощное противовоспалительное действие (подавляет определённый фермент (так называемый ядерный фактор каппа-B), участвующий в производстве активаторов воспаления (цитокинов) (Оh, 2011).
В эксперименте на животных изучение этого механизма на модели астмы показало, что куркумин, таким образом, снижает чрезмерную чувствительность дыхательных путей, воспалительные явления, накапливание воспалительных клеток в лёгких (Оh, 2011).
Ликопин – красный пигмент, найденный в помидорах и некоторых фруктах. Убольных с астмой добавление в рацион ликопина более чем у половины пациентов предупреждает развитие приступа при физической нагрузке (Neuman, 2000).
В исследованиях у животных установлены многочисленные положительные эффекты ликопина на лёгкие при астме: снижает предрасположенность к аллергии и склонность к реакции бронхов, уменьшает воспаление и отёк (Hazlewood, 2011; Lee, 2008).
Флавоноиды, найденные в фруктах, овощах, красном вине, чае, обладают антиоксидантными и противовоспалительными свойствами. Установлено, что их потребление улучшает работу лёгких (Garcia, 2005). Некоторые из них были изучены при астме.
Установлено, что регионы, где больше потребляют флавоноидов, меньше заболеваемость астмой:
— чай и лук (за счёт кверцетина);
— апельсины и грейпфруты (основной флавоноид нарингенин);
— апельсины и лимоны (содержат защитный флавоноид гесперидин) (Knekt, 2002).
В одном исследовании установлено, что даже однократный приём кверцетина приводит к расслаблению бронхов и их расширению (Joskova, 2011).
В другом исследовании подтверждено, что кверцетин уменьшает выработку слизи и оказывает противовоспалительное действие (снижая выработку активаторов воспаления– цитокинов) (Rogerio, 2010).
Ещё в одном исследовании на животных выявлено, что кверцетин подавляет развитие астматической реакции при введении специального вещества-провокатора (Park, 2009).
Растение содержит флавоноиды, которые облегчают состояние при астме (Mahmoud, 2000; Li, 1997; Tang, 2007).
В одном исследовании экстракт гинкго билобы применялся в течение 2 недель у пациентов с астмой, которым были назначены гормональные препараты. Обнаружено, что в мокроте больных, получавших гинкго билобу, значительно меньше воспалительных клеток по сравнению с приёмом только гормональных препаратов или только пустышки-плацебо, что подтверждает, что растение уменьшает воспаление в дыхательных путях при астме (Tang, 2007).
В исследовании на животных было установлено, что гинкго снижает накопление воспалительных клеток в лёгочной ткани и уменьшает продукцию слизи в дыхательных путях (Chu, 2011).
Коллоидные фитоформулы ЭД Медицин содержат богатый набор полезных и научно 
— выпускаются в виде коллоидного раствора высокой биодоступности (до 98%)
— выпускаются на фабрике по фармакопейному стандарту cGMP
— отсутствуют потенциально опасные ингредиенты (аллергены, ГМО, НАНО)
— многокомпонентные препараты, то есть один продукт содержит весь комплекс научно обоснованных и полезных нутриентов, витаминов и минералов
Содержит богатыйнабор нутриентов, витаминов и минералов, которые применяют при астме и описаны выше, в виде коллоидного раствора высочайшей биодоступности (до 98%):
— строго стандартизованный экстракт гинкго билоба
— кверцетин
— витамин С
— витамин Е
— селен
— цинк
Содержит комплекс целебных растений и нутриентов, активно улучшающих функции внешнего дыхания, способствующих уменьшению бронхоспазма и воспалительных явлений и, таким образом, облегчающих течение бронхиальной астмы ( подробнее >> ).
источник
 Магний (Mg) обладает некоторыми спазмолитическими свойствами, расслабляет мышцы. Снижает восприимчивость организма к аллергенам. Его в некоторых случаях при бронхиальной астме даже назначают внутривенно.
Магний (Mg) обладает некоторыми спазмолитическими свойствами, расслабляет мышцы. Снижает восприимчивость организма к аллергенам. Его в некоторых случаях при бронхиальной астме даже назначают внутривенно. пиридоксин – онемение в области конечностей, уменьшение лактации у женщин, изредка судороги;
пиридоксин – онемение в области конечностей, уменьшение лактации у женщин, изредка судороги;