Иосиф Хусенский
Детский врач скорой помощи. Диагностика и лечение бронхиальной астмы у детей на дому.
-
- Определение, что такое БОС.
- Причины возникновения БОС у детей.
- Тактика родителей при БОС у детей.
- Тактика врача скорой помощи при БОС у детей.
- Влияние БОС на развитие бронхиальной астмы у детей.
- Основной метод профилактики БОС у детей.
- Определение, что такое БОС.
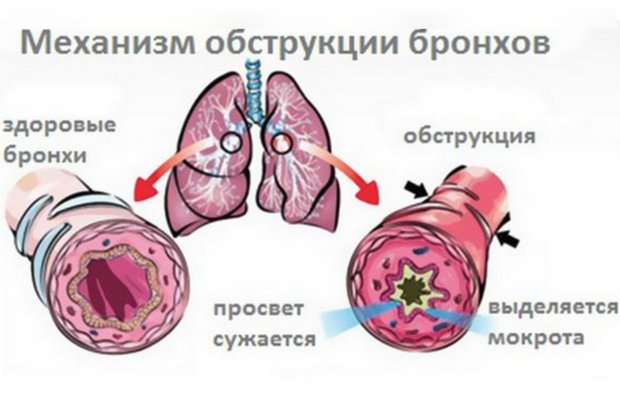
Бронхообструктивный синдром (БОС), синдром бронхиальной обструкции – набор клинических признаков, образующихся из-за тотального сужения просвета бронхов. Сужение просвета мелких бронхов и фосирование выдоха приводит к возникновению свистящих звуков. Клинические проявления БОС складываются из удлинения выдоха, появления экспираторного шума (свистящее дыхание), приступов удушья, участия вспомогательной мускулатуры в акте дыхания, малопродуктивного кашля. При выраженной обструкции увеличивается частота дыхания, развивается усталость дыхательных мышц и снижается парциальное напряжение кислорода крови.
Причины возникновения БОС у детей.
У детей первого года жизни БОС бывает:
- При аспирации инородным телом.
- При нарушении глотания (бешенство).
- Из-за врожденных аномалий носоглотки.
- При свище в стенке трахеи или бронхов.
- При гастроэзофагальном рефлюксе.
- При пороках развития трахеи и бронхов.
- При гипертензии в малом круге из-за недостаточности сердечно-сосудистой деятельности.
- При респираторном дистресс-синдроме.
- При легоной форме муковисцидоза.
- При бронхолегочной дисплазии.
- При иммунодефицитных состояниях.
- Вследствие внутриутробной инфекции.
- От пассивного курения.
- При приступе бронхиальной астмы.
- При рино-синтициальной респираторной вирусной инфекции (РСРВИ).
У детей 2-3 года БОС могут впервые возникнуть из-за:
-
- бронхиальной астмы,
- РСРВИ,
- аспирации инородного тела,
- миграции круглых гельминтов,
- облитерирующего бронхиолита,
- врожденных заболеваний сердца,
- наследственных заболеваний,
- пороков сердца с гипертензией в малом круге,
- ОРВИ с обструктивным синдромом.
У детей старше 3 лет основными причинами БОС являются:
- Бронхиальная астма,
- Врожденные и наследственные заболевания органов дыхания:
- муковисцидоз,
- синдром цилиарной дискинезии,
- пороки развития бронхов.
- Аспирация инородного тела.
- ОРВИ с обструктивным синдром.
Этот текст, предназначен для родителей и врачей скорой помощи. Поэтому можно отметить, что в вечернее время, когда поликлиника уже не работает, причин внезапного возникновения БОС, угрожающего жизни ребёнка в домашних условиях, по мнению автора текста, в 99% всего три:
1. Аспирация инородного тела — 2%.
2. Вирусный или инфекционный бронхит (бронхиолит) — 23%;
3. Приступ бронхиальной астмы — 74%.
Тактика родителей при БОС у детей.
1. При неожиданном, на фоне полного здоровья, во время еды ребёнка или во время игры ребёнка с мелкими игрушками возникновении асфиксии и БОС, нужно предпринять все меры, чтобы удалить предмет, которым мог подавиться ребёнок и параллельно срочно вызывать скорую помощь.
2. При неожиданном появлении признаков БОС у больного ОРВИ (высокая температура, насморк, кашель, интоксикация) ребёнка нужно думать об утяжелении течения инфекционного заболевания и вызывать скорую помощь, чтобы везти ребёнка в инфекционный стационар, где есть отделение интенсивной терапии.
3. При возникновении БОС на фоне навязчивого приступообразного сухого кашля, насморка и нормальной или субфебрильной температуре у ребёнка, больного бронхиальной астмой, нужно думать о приступе бронхиальной астмы. И если родителям не удаётся самим снять явления бронхоспазма и перевести сухой кашель из сухого кашля во влажный кашель с мокротой, то тогда нужно обращаться за помощью на скорую помощь, чтобы с помощью ряда инъекций устранить приступ бронхиальной астмы дома.
Если в течение нескольких дней не получается вывести ребёнка из обострения бронхиальной астмы, показана госпитализация в соматический стационар, где есть отделение интенсивной терапии.
Тактика врача скорой помощи на до госпитальном этапе при БОС у ребёнка.
1. При наличии асфиксии и крайне тяжелого состояния ребёнка, возникшего внезапно, на фоне полного здоровья, показана немедленная интубация, и перевод на искусственную вентиляцию лёгких. И экстренная госпитализация в ближайший стационар, где имеется в приёмном отделении реанимация.
2. Если признаков асфиксии и аспирации инородного тела нет, а диагноза бронхиальная астма у ребёнка тоже нет, — врачу надо быстро определить, какая причина вызвала БОС у ребёнка: инфекция или аллергия. После выяснения причины действовать по характеру установленного диагноза. При установлении аллергической причины, надо действовать, как при приступе бронхиальной астмы. При установлении инфекционной природы БОС – действовать соответственно.
Влияние БОС на развитие бронхиальной астмы у детей.
Бытует мнение, и не только у практикующих врачей, но и у многих учёных исследователей, занимающихся изучением проблем диагностики бронхиальной астмы у детей, что повторяющиеся БОС инфекционной природы, является фактором высокого риска заболеть бронхиальной астмой. Это, по мнению автора статьи, очень вредное заблуждение, которое опасно для здоровья ребёнка, уже больного бронхиальной астмой. Потому что, приступы бронхиальной астмой врачи ошибочно расценивают, как БОС инфекционной природы. Со всеми вытекающими от этого последствиями.
Методы профилактики БОС у детей.
Реальная возможность уменьшить количество БОС у одного ребёнка, а значит в целом у всех детей — своевременно распознать у ребёнка бронхиальную астму и принять такие меры, и организовать такое лечение, чтобы у него приступы стали возникать реже.
Что это может получиться в цифрах?
В Странах СНГ больных бронхиальной астмой около 8% — это 4-5 миллионов детей. У 80% болезнь возникает в возрасте до 3-х лет. И в течение какого-то длительного времени болезнь шифруется под БОС инфекционной природы. Если бы можно было в массовом порядке ускорить установление бронхиальной астмы у детей на 1 год. У миллионов детей, у каждого не было бы дополнительных 3-5 БОС. Эти приступы бронхиальной астмы были спровоцированы «плохими» бытовыми условиями и «неправильным» питанием.
источник
БРОНХООБСТРУКТИВНЫЙ СИНДРОМ У ДЕТЕЙ
Кафедра детских болезней N 1 РГМУ, Москва
Определение. Бронхообструктивный синдром (БОС) или синдром бронхиальной обструкции — это симптомокомплекс, связанный с нарушением бронхиальной проходимости функционального или органического происхождения. Клинические проявления БОС складываются из удлинения выдоха, появления экспираторного шума (свистящее, шумное дыхание), приступов удушья, участия вспомогательной мускулатуры в акте дыхания, часто развивается малопродуктивный кашель. При выраженной обструкции бронхов может появиться шумный выдох, увеличение частоты дыхания, развитие усталости дыхательных мышц и снижение РаО2. В англоязычной литературе этот клинический симптомокомплекс получил название wheezing — синдром свистящего дыхания [1,2], так как свистящие звуки, дистантные или выслушиваемые при аускультации, являются основным клиническим симптомом БОС.
Однако термин «бронхообструктивный синдром» не может быть использован как самостоятельный диагноз. Следует учитывать, что БОС является весьма гетерогенным по своей сути и может быть проявлением многих заболеваний.
Эпидемиология. БОС достаточно часто встречается у детей, особенно у детей первых 3 лет жизни. На возникновение и развитие БОС оказывают влияние различные факторы и, прежде всего, респираторная вирусная инфекция [3-7]. До настоящего времени нет четких данных о распространенности БОС при различной бронхолегочной патологии у детей, однако наибольшая частота БОС отмечается у детей дошкольного возраста, что связано е анатомо-физиологическими особенностями организма в этот период. Разноречивость сведений о частоте и структуре БОС обусловлена отсутствием единого подхода к дифференциальной диагностике, трактовке этнологии и патогенеза. Очевидно, что частота развития БОС зависит не только от возраста детей, но и от множества других факторов — экологических, эпидемиологических, социально-бытовых и др. Кроме того, БОС не всегда фиксируется в заключительном диагнозе и в этом случае не подлежит статистическому учету. В то же время наибольший интерес представляет частота тяжелых и/или рецидивирующих вариантов БОС, как правило, требующих госпитализации и проведения активной медикаментозной терапия.
Частота развития БОС, развившегося на фоне инфекционных заболеваний нижних дыхательных путей, у детей раннего возраста составляет, по данным разных авторов, от 5% до 40% [2, 3, 8-11]. У детей с отягощенным семейным анамнезом по аллергии БОС, как правило, развивается чаще (в 30 — 40% случаев). Это также характерно для детей, которые часто (более б раз в году) болеют респираторными инфекциями.
По нашим данным [4], частота БОС среди всего контингента бальных раннего возраста (от 3 мес до 3 лет), госпитализированных в соматические и инфекционные отделения 1000-коечной Морозовской детской городской клинической больницы (МДГКБ), за последнее десятилетие возросла с 9,7% до 16,1%. У детей с острым инфекционным заболеванием нижних дыхательных путей БОС встречался у 34% пациентов, причем при бронхите в 3 раза чаще, чем при пневмонии. Повторные эпизоды БОС имели чуть меньше половины госпитализированных детей, из них большинство были в возрасте старше 1 года. Учитывая, что МДГКБ является городской больли-цей, осуществляющей как плановую госпитализацию, так и госпитализацию детей, доставленных по «скорой помощи», выявленная тенденция, скорее всего, отражает общее увеличение частоты БОС среди детей раннего возраста.
Факторы риска развития БОС. Предрасполагающими анатомо-фнзиологическими факторами к развитию БОС у детей раннего возраста являются наличие у них гиперплазии железистой ткани, секреция преимущественно вязкой мокроты, относительная узость дыхательных путей, меньший объем гладких мышц, низкая коллатеральная вентиляция, недостаточность местного иммунитета, особенности строения диафрагмы.
Влияние факторов преморбидного фона на развитие БОС признается большинством исследователей. Это — отягощенный аллергологнчесхяй анамнез, наследственная предрасположенность к атопии, гиперреактивность бронхов, перинатальная патология, рахит, гипотрофия, гиперплазия тимуса, раннее искусственное вскармливание, перенесенное респираторное заболевание в возрасте 6—12 месяцев.
Среди факторов окружающей среды, которые могут приводить к развитию БОС, особо важное значение придается неблагоприятной экологической обстановке, пассивному курению в семье. Под влиянием табачного дыма происходит гипертрофия бронхиальных слизистых желез, нарушается мукоцилиарный клиренс, замедляется продвижение слизи. Пассивное курение способствует деструкции эпителия бронхов. Табачный дым является ингибитором хемотаксиса нейтрофилов. Количество альвеолярных макрофагов под его влиянием увеличивается, но уменьшается их фагоцитарная активность. При длительном воздействии, табачный дым оказывает влияние на на иммунную систему — снижает активность Т-лимфоцитов, угнетает синтез антител основных классов, стимулирует синтез иммуноглобулинов Е, повышает активность блуждающего нерва. Особенно ранимыми считаются дети первого года жизни.
Определенное влияние оказывает и алкоголизм родителей. Доказано, что у детей с алкогольной фетопатией развивается атония бронхов, нарушается мукоцилиаркый клиренс, тормозится развитие защитных иммунологических реакций.
Таким образом, в развитии БОС у детей важную роль играют возрастные особенности респираторной системы, свойственные детям первых лет жизни. Несомненное влияние на нарушения функционирования органов дыхания у маленького ребенка оказывают и такие факторы, как более длительный сон, частый плач, преимущественное пребывание на спине в первые месяцы жизни.
Этиология. Причины развития БОС у детей весьма разнообразны и многочисленны. В то же время дебют БОС у детей, как правило, на фоне острой респираторной вирусной инфекции и у подавляющего большинства пациентов является одним из клинических проявлений острого бронхита или бронхиолита. Респираторные инфекции являются самой частой причиной развития БОС у детей первых 3 лет жизни. В то же время необходимо учитывать, что развитие БОС на фоне ОРВИ может маскировать проявление основного заболевания. Так, по данным литературы, у детей раннего возраста бронхиальная астма (БА) является вариантом течения БОС в 30—50% случаев [1, 10, 13).
У младенцев причиной БОС нередко может стать аспирация, обусловленная нарушением глотания, врожденными аномалиями носоглотки, трахео-бронхиальным свищом, гастоэзофагеальным рефлюксом. Пороки развития трахеи и бронхов, респираторный дистресс-синдром, муковисцидоз, бронхо-пульмональная дисплазия, иммунодефицитные состояния, внутриутробные инфекции, наличие табачного дыма в воздухе (пассивное курение) также являются причинами БОС у детей первого года жизни. На втором и третьем году жизни клинические проявлениялшжшя БОС могут впервые возникнуть у детей с БA, при аспирации инородного тела, миграции круглых гельминтов, облитерятующем бронхнолите, у больных с врожденными и наследственными заболеваниях органов дыхания, у детей с пороками сердца, протекающими с легочной гипертензией и др.
Патогенез. Формирование бронхиальной обструкции во многом зависит от этиологии заболевания, ставшего причиной БОС. В генезе бронхиальной обструкции лежат различные патогенетические механизмы, которые условно можно разделить на функциональные или обратимые (бронхоспазм, воспалительная инфильтрация, отек, мукоцилиарная недостаточность, гиперсекреция вязкой слизи) и необратимые (врожденные стенозы бронхов, их облитерация и др.). Физикальные признаки при наличии бронхиальной обструкции обусловлены тем, что для производства выдоха требуется повышенное внутригрудиое давление, что обеспечивается усиленной работой дыхательной мускулатуры. Повышенное внутригрудное давление способствует сдавлению бронхов, что приводит к их вибрации и возникновению свистящих звуков. Некоторыми авторами высказывается мысль о защитной функции БОС при инфекции респираторного тракта. Считают, что сужение мелких бронхов сопровождается резким увеличением скорости воздуха в них, что способствует лучшему очищению бронхиального дерева и защите нижележащих отделов от проникновения микроорганизмов [9]. Однако эта точка зрения нам представляется спорной. Регуляция тонуса бронхов контролируется несколькими физиологическими механизмами, включающими сложные взаимодействия рецепторно-клеточного звена и системы медиаторов. К ним относятся холинергическая, адренергическая и нейрогуморальная (нехолинергкческая, неадренергическая) системы регуляции и, конечно, развитие воспаления [5, 14].
Воспаление является важным фактором бронхиальной обструкции у детей и может быть вызвано инфекционными, аллергическими, токсическими, физическими и нейрогенными воздействиями. Медиатором, инициирующим острую фазу воспаления, является интерлейкин1 (ИЛ1). Он синтезируется фагоцитирующими клетками и тканевыми макрофагами при воздействии инфекционных или неинфекционных факторов и активирует каскад иммунных реакций, способствующих выходу в периферический кровоток медиаторов 1-го типа (гистамнна, серото-нина и др.). Эти медиаторы постоянно присутствуют в гранулах тучных клеток и базофилах, что обеспечивает их очень быстрые биологические эффекты при дегрануляции клеток-продуцентов. Гистамин высвобождается, как правило, в ходе аллергической реакции при взаимодействии аллергена с аллерген-специфическими IgE антителами. Однако дегрануляцию тучных клеток и базофилов могут вызвать и неиммунные, в том числе инфекционные, механизмы. Помимо гистамина, важную роль в патогенезе воспаления играют медиаторы 2-го типа (эйкозаноиды), генерируемые в процессе ранней воспалительной реакция. Источником эйхозаноидов является арахидоновая кислота, образующаяся из фосфолипидов клеточных мембрая. Под действием циклооксигеназы (ЦОГ) из арахидоновой кислоты синтезируются простогландины (ПГ), тромбоксан и простациклин, а под действием липооксигеназы — лейкотриены. Именно с гистамином, лейкотриенами и провоспалительными ПГ связано усиление проницаемости сосудов, появление отека слизистой оболочки бронхов, гиперсекреция вязкой слизи, развитие бронхоспазма и, как следствие, формирование клинических проявлений БОС. Кроме того, эти события инициируют развитие поздней реакции воспаления, способствующей развитию гиперреактивности и альтерации (повреждения) эпителия слизистой оболочки дыхательных путей [5, 15. 16).
Поврежденные ткани имеют повышенную чувствительность рецепторов бронхов к внешним воздействиям, в том числе к вирусной инфекции и поллютантам, что значительно повышает вероятность развития бронхоспазма. Кроме того, в поврежденных тканях синтезируются провоспалительные цитокины (ИЛ8 и др.), происходит дегрануляция нейтрофилов, базофилов, эозинофилов, в результате чего повышается концентрация таких биологически активных веществ, как брадикинин, гистамин, свободные радикалы кислорода и NО, которые также участвуют в развитии воспаления. Таким образом, патологический процесс приобретает характер «замкнутого крута» и предрасполагает к продолжительному течению бронхиальной обструкции и суперинфекции.
Воспаление является основным патогенетическим звеном в развитии и других механизмов бронхиальной обструкции, таких как гиперсекреция вязкой слизи и отек слизистой оболочки бронхов.
Нарушение бронхиальной секреции развивается при любом неблагоприятном воздействии на органы дыхания и, в большинстве случаев, сопровождается увеличением количества секрета и повышением его вязкости. Деятельность слизистых и серозных желез регулируется парасимпатической нервной системой, ацетилхолии стимулирует их деятельность. Такая реакция изначально носит защитный характер. Однако застой бронхиального содержимого приводит к нарушению вентиляционно-респираторной функции легких, а неизбежное инфицирование — к развитию эндобронхиального или бронхолегочного воспаления. Кроме того, продуцируемый густой и вязкий секрет, помимо угнетения цилиарной активности, может вызвать бронхиальную обструкцию вследствие скопления слизи в дыхательных путях. В тяжелых случаях вентиляционные нарушения сопровождаются развитием ателектазов.
Отек и гиперплазия слизистой оболочки дыхательных путей также являются одной из причин бронхиальной обструкции. Развитые лимфатическая и кровеносная системы респираторного тракта ребенка обеспечивают ему многие физиологические функции. Однако в условиях патологии характерным для отека является утолщение всех слоев бронхиальной стенки — подслизистого и слизистого слоя, базальной мембраны, что ведет к нарушению бронхиальной проходимости. При рецидивирующих бронхолегочных заболеваниях нарушается структуpa эпителия, отмечается его гиперплазия и плоскоклеточная метаплазия.
Бронхоспазм, безусловно, является одной из основных причин БОС у детей старшего возраста и взрослых. В то же время в литературе имеются указания, что дети раннего возраста, несмотря на слабое развитие гладкомышечной системы бронхов, иногда могут давать типичный, клинически выраженный, брокхоспазм. В настоящее время изучено несколько механизмов патогенеза бронхосзазма, клинически реализующегося в виде БОС.
Известно, что холинергическая регуляция просвета бронхов осуществляется непосредственным воздействием на рецепторы гладких мышц органов дыхания. Общепризнано, что холинергические нервы заканчиваются на клетках гладких мышц, которые имеют не только холинергические рецепторы, но и H1-гистаминовые рецепторы, β2-адренорецепторы и рецепторы нейропептидов. Высказывается мнение, что клетки гладких мышц респираторного тракта имеют и рецепторы для ПГF2a.
Активация холинергических нервных волокон приводит к увеличению продукции ацетилхолина и повышению концентрации гуанилатциклазы, которая, в свою очередь, способствует поступлению ионов кальция внутрь гладкомышечной клетки, тем самым стимулируя бронхоконстрикцию. Этот процесс может быть усилен влиянием ПГF2a. М-холинорецепторы у младенцев развиты достаточно хорошо, что, с одной стороны, определяет особенности течения бронхообструктивных заболеваний у детей первых лет жизни (склонность к развитию обструкции, продукция очень вязкого бронхиального секрета), а с другой стороны, объясняет выраженный бронхолитический эффект М-холинолитиков у этой категории пациентов.
Известно, что стимуляция β2-адренорецепторов катехоламинами, так же как повышение концентрации цАМФ и ПГ-Е2, уменьшают проявления бронхоспазма. Наследственно обусловленная блокада аденилатциклазы снижает чувствительность β2-адренорецепторов к адреномиметикам, что достаточно часто встречается у больных БА. Некоторые исследователи указывают на функциональную незрелость β2-адренорецепторов у детей первых месяцев жизни.
В последние годы отмечается повышенный интерес к системе взаимоотношений между воспалением и системой нейропептидов, которые осуществляют интеграцию нервной, эндокринной и иммунной систем. У детей первых лет жизни эта взаимосвязь более выражена и определяет предрасположенность к развитию бронхообструкции. Следует отметить, что иннервация органов дыхания более сложна, чем это предполагалось ранее. Кроме классической холинергнческой и адренергической иннервации существует нехолинергическая неадрeнэргическая иннервация (НАНХ). Основными нейротрансмиттерами или медиаторами этой
Системы являются нейропептиды. Нейросекреторные клетки, в которых образуются нейропептиды, выделяют в отдельную категорию — «APUD»-систему (amino precursor uptake decarboxyiase). Нейросекреторные клетки обладают свойствами экзокринной секреции и могут обусловить дистантный гуморально-эндокринный эффект. Гипоталамус, в частности, является ведущим звеном системы нейропептидов. Наиболее изученными иейропептидамя являются субстанция Р, нейрокины А и В, пептид, связанный с геном кальцитонина, вазоактивный интестинальный пептид (ВИП). Нейропептиды могут взаимодействовать с иммуно-компетентными клетками, активировать дегрануляцию, увеличивать гиперреактивность бронхов, регулировать синтетазу NO, непосредственно влиять на гладкие мышцы и кровеносные сосуды. Было показано, что система нейропептидов играет важную роль в регуляции бронхиального тонуса. Так, инфекционные возбудители, аллергены или поллютанты, помимо вагусобусловленной реакции (бронхоконстрикции), стимулируют сенсорные нервы и выброс субстанции Р, усиливающей бронхоспазм. В то же время ВИП обладает выраженным бронхо-дилатирующим действием.
Таких образом, существует несколько основных механизмов развития бронхиальной обструкции. Удельный вес каждого из них зависит от причины, обусловливающей патологический процесс, и возраста ребенка. Анатомо-физиологические и иммунологические особенности детей раннего возраста определяют высокую частоту формирования БОС у этой группы пациентов. Надо отметить важную роль преморбидного фона в развитии и течении бронхообструкции. Важной особенностью формирования обратимой бронхиальной обструкции у детей первых 3 лет жизни является преобладание воспалительного отека и гиперсекреции вязкой слизи над бронхоспастическим компонентом обструкции, что необходимо учитывать в комплексных программах терапии.
Классификация. Известно около 100 заболеваний, сопровождающихся БОС (3, 8, 17 — 19). Однако до настоящего времени не существует общепринятой классификации БОС. Рабочие группировки, как правило, представляют собой перечисление заболеваний, протекающих с бронхообструкцией. На основании данных литературы и собственных наблюдений у детей раннего возраста можно выделить следующие группы заболеваний, сопровождающихся БОС.
Заболевания, сопровождающиеся БОС:
1. Заболевания органов дыхания:
1.1. инфекционно-воспалительные заболевания (бронхит, бронхиолит, пневмония);
1.3. аспирация инородных тел;
1.3. бронхолегочная дисплазия;
1.4. пороки развития бронхолегочной системы;
1.5. облитерирующий броахиолит;
2. Заболевания желудочно-кишечного тракта (холазия и ахолазия пищевода, гастроэзофагеальный рефлюкс, трахеопищеводный свищ, диафрагмальная грыжа).
3. Наследственные заболевания (муковисцидоз, дефицит α1-антитрипсина, мукополисахаридозы, рахитоподобные заболевания).
4. Паразитарные инфекции (токсокароз и др.).
5. Заболевания сердечно-сосудистой системы.
6. Заболевания центральной и периферической нервной системы (родовая травма, миопатии и др.).
7. Врожденные и приобретенные иммунодефицитные состояния.
8. Воздействие различных физических и химических факторов внешней среды.
9. Другие причины (эндокринные заболевания, системные васкулиты, тимомегалия и др.).
С практической точки зрения можно выделить 4 основные группы причин БОС:
По длительности течения БОС может быть острым (клинические проявления БОС сохраняются не более 10 дней), затяжным, рецидивирующим и непрерывно рецидивирующим.
По выраженности обструкции можно выделить легкую степень тяжести, среднетяжелую, тяжелую и скрытую бронхиальную обструкцию. Критериями тяжести течения БОС являются наличие свистящих хрипоз, одышки, цианоза, участие вспомогательной мускулатуры в акте дыхания, показатели функции внешнего дыхания (ФВД) и газов крови. Кашель отмечается при любой степени тяжести БОС.
Для легкого течения БОС характерно наличие свистящих хрипов при аускультации, отсутствие в покое одышки и цианоза. Показатели газов крови в пределах нормы, показатели ФВД (объем форсированного выдоха за 1-ю секунду и максимальная скорость выдоха) составляют более 80% от нормы. Самочувствие ребенка, как правило, не страдает.
Течение БОС средней степени тяжести сопровождается наличием в покое одышки экспираторного или смешанного характера, цианоза носогубного треугольника, втяжения уступчивых мест грудной клетки. Свистящее дыхание слышно на расстоянии. Показатели ФВД составляют 60—80% от нормы, КОС нарушено незначительно (РаО2 более 60 мм рт. ст., РаСО2 менее 45 мм рт. ст.).
При тяжелом течении приступа бронхиальной обструкции самочувствие ребенка страдает, характерны шумное затрудненное дыхание с участием вспомогательной мускулатуры, наличие цианоза. Показатели ФВД ниже 60% от нормы, РаО, менее 60 мм рт ст., РаСО, более 15 мм рт. ст.
При скрытой бронхиальной обструкции не определяется клинических и физикальных признаков БОС, но при изучении ФВД определяется положительная проба с бронхолитиком (увеличение ОФВ1 более чем на 12% после ингаляции с бронхолитиком и/или увеличение суммы прироста максимальных объемных скоростей выдоха (MOCI5_TS) на 37% и более).
Тяжесть течения БОС зависит от этиологии заболевания, возраста ребенка, преморбндного фона и некоторых других факторов. Необходимо учитывать, что БОС — не самостоятельный диагноз, а симптомокомллекс какого-либо заболевания, нозологическую форму которого следует установить во всех случаях развития бронхиальной обструкции.
Клиника. Классические клинические симптомы БОС, как упоминалось ранее, могут быть разной степени выраженности и складываются из удлинения выдоха, появления свистящего, шумного дыхания. Часто развивается малопродуктивный кашель. При тяжелом течении характерно развитие приступов удушья, которое сопровождается втяжением уступчивых мест грудной клетки, участием вспомогательной мускулатуры в акте дыхания. При физикальном обследовании аускультативно определяются сухие свистящие хрипы. У детей раннего возраста достаточно часто выслушиваются и влажные разнокалиберные хрипы. При перкуссии появляется коробочный оттенок звука над легкими. Для выраженной обструкции характерны шумный выдох, увеличение частоты дыхания, развитие усталости дыхательных мышц и снижение РаО,.
Диагностика. Диагноз бронхиальной обструкции у детей раннего возраста, как правило, ставится на основании клиническо-анамнестических данных и результатов физикального и функционального обследования [5, 8, 20]. Изучение ФВД методами спирографии и пневмотахометрии у пациентов первых лет жизни не проводится. Дети моложе 5 — 6 лет неспособны выполнить технику форсированного выдоха, поэтому проведение данных высокоинформативных исследований у них невозможно. В первые годы жизни ребенка проводят исследование периферического сопротивления дыхательных путей (техника прерывания потока) и бодиплетизмографию, позволяющие с определенной долей вероятности выявить и оценить обструктивные и рестриктивные изменения. Определенную помощь в дифференциальной диагностике у детей первых лет жизни могут оказать осциллометрия и бронхофонография. Однако до настоящего времени эти методы не нашли применения в широкой педиатрической практике.
С целью установления диагноза заболевания, протекающего с БОС, необходимо подробно изучить клинико-анамнестические данные, обратив особое внимание на наличие в семье атопии, перенесенные ранее заболевания, наличие рецидивов бронхообструкции.
Впервые выявленный БОС легкого течения, развившийся на фоне респираторной инфекции, не требует проведения дополнительных методов обследования.
При рецидивирующем течении БОС комплекс методов обследования должен включать: 1) Исследование периферической крови;
2) Серологические тесты (специфические IgM и IgG обязательно, исследование IgA — желательно) на наличие хламидийной, микоплазменной, цитомегаловирусной, герпетической и пневмоцистной инфекций [21]; при отсутствии IgM и наличии днагностических титров IgG необходимо повторить исследование через 2—3 недели (парные сыворотки)
3) Серологические тесты на наличие гельминтозов (токсокароза, аскаридоза)
4) Аллергологическое обследование (уровень общего IgE, специфические IgE, кожные скарификационные пробы); другие иммунологические обследования проводят после консультации иммунолога.
Бактериологические методы обследования и ПЦР диагностика являются высокоинформативными только при заборе материала при проведении бронхоскопии, исследование мазков характеризует преимущественно флору верхних дыхательных путей.
Рентгенография грудной клетки не является обяательным методом исследования у детей с БОС. Это исследование проводят при следующих ситуациях:
1) подозрение на осложненное течение БОС (например, наличие ателектаза); 2) исключение острой пневмонии;
3) подозрение на инородное тело;
4) рецидивирующее течение БОС (если ранее рентгенографию не проводили).
По показаниям проводят бронхоскопию, бронхографию, сцинтиграфию, ангиопульмонографию, компьютерную томографию и др. Объем исследования, безусловно, определяется индивидуально в каждом конкретном случае [22].
Тяжелые случаи бронхообструкции, а также все повторные случаи заболеваний, протекавших с БОС, требуют обязательной госпитализации для уточнения генеза БОС, проведения адекватной терапии, профилактики и прогноза дальнейшего течения заболевания.
источник

Особенно сложно протекает у детей младшего возраста. Почему развивается данный синдром, как его распознать и вовремя начать лечение — рассмотрим далее в статье.
Бронхообструктивный синдром (БОС) — это не самостоятельный медицинский диагноз или заболевание, БОС является проявлением отдельных нозологических форм. К примеру, у малышей до трех лет в половине случаев возникновения синдрома бронхиальной обструкции причиной является астма.
Также у малышей случаи БОС могут возникать по причине врожденных аномалий носоглотки, нарушений глотания, гастроэзофагеального рефлюкса и прочего.
Особенно часто синдром развивается у детей до 3 лет, которые имеют отягощенный семейный анамнез, склонны к аллергическим реакциям и часто переносят респираторные заболевания. В основе возникновения БОС лежит следующий механизм: возникает воспаление различной этиологии, которое влечет за собой спазм и дальнейшее сужение просвета (окклюзию) бронха. В результате происходит сдавливание бронхов.
Синдром бронхиальной обструкции классифицируется по форме, длительности протекания и степени тяжести проявления синдрома.
По форме протекания БОС бывает:
- Инфекционный (вирусный и бактериальный).
- Гемодинамический (возникает при сердечных патологиях)
- Обтурационный.
- Аллергический.
В зависимости от длительности протекания выделяют:
- Острый БОС. Сопровождается ярко выраженной клинической картиной, симптомы проявляются более 7 дней.
- Затяжной. Клинические проявления менее выражены, течение длительное.
- Рецидивирующий. Острые периоды резко сменяются периодами ремиссии.
- Постоянно-рецидивирующий. Периоды неполной ремиссии сменяются обострениями синдрома.
Среди заболеваний, которые могут сопровождаться возникновением БОС, выделяют:
- Патологии системы дыхания (аспирация, инфекционные болезни, астма, врожденные аномалии, дисплазия).
Функциональные изменения хорошо поддаются консервативному лечению, в то время как устранение органических изменений проводится только в некоторых случаях путем оперативного вмешательства и за счет адаптационных возможностей ребенка.
Среди функциональных изменений выделяют бронхоспазм, большое выделение мокроты при бронхитах, отек слизистой бронхов, воспаления и аспирации. К органическим изменениям относятся врожденные пороки развития бронхов и легких, стенозы и прочее.
БОС у малышей обусловлен особенностями физиологии в столь юном возрасте — дело в том, что бронхи ребенка существенно уже, и их дополнительное сужение в результате отека даже на один миллиметр уже окажет ощутимый негативный эффект.
Нормальное функционирование бронхиального дерева может быть нарушено в первые месяцы жизни из-за частого плача, пребывания на спине, длительного сна. 
К тому же у малыша до года еще не стабилизировались процессы иммунной защиты, что также играет роль в возникновении бронхиальной обструкции.
К клиническим проявлениям бронхообструкционного синдрома относятся следующие:
- удлиненный вдох;
- появление свиста и хрипа во время дыхания;
- затяжной непродуктивный кашель;
- увеличение дыхательных движений, участие вспомогательной мускулатуры в процессе дыхания;
- гипоксемия;
- появление одышки, нехватка воздуха;
- увеличение грудной клетки;
- дыхание становится громким, ослабленным или жестким.
Перечисленные симптомы свидетельствуют именно о возникновении сужения бронхиального просвета. Однако общие симптомы во многом определяются основной патологией, которая стала причиной БОС. 
При обращении к терапевту или неонатологу доктор проведет опрос мамы малыша на наличие аллергий, недавно перенесенных заболеваний, выявленных отклонений в развитии, о семейном анамнезе.
Помимо присутствия клинических признаков у ребенка, для постановки диагноза БОС необходимо провести специфические физикальные и функциональные исследования.
Важнейшим анализом для подтверждения диагноза является спирометрия — при этом исследуется объем вдыхаемого и выдыхаемого воздуха, емкость легких (жизненная и форсированная), количество воздуха при форсированном вдохе, проходимость путей дыхания.
Во время анализа проводится несколько циклов дыхания, чтобы вычислить достоверный результат. Также для диагностики БОС применяется пневмотахометрия, которая исследует скорость прохождения воздуха по дыхательным путям в момент вдоха и выдоха.
Если БОС возник вследствие инфекции дыхательных путей и имеет рецидивирующий характер, есть смысл провести дополнительные специфические исследования:
- Анализ крови.
- Анализ на наличие IgG/IgM при герпетической, хламидийной, микоплазменной инфекциях и ЦМВ.
- Исключение заражения токсокарозом и аскаридозом.
- Иммунологические тесты.
Если после перенесенной простуды рецидивы отсутствуют, надобности в проведении перечисленных анализов нет. Также в качестве дополнительных исследований назначают рентген, ПЦР, КТ, бронхоскопию, сцинтиграфию.
Во всех случаях возникновения БОС необходима госпитализация для выяснения первичной патологии и, при необходимости, проведения дифференциальной диагностики для отличия БОС от туберкулеза, астмы, пневмонии, ХОБЛ и коклюша.
Алгоритм оказания неотложной помощи при бронхообструктивном синдроме у детей состоит из следующих действий:
- Если вы заметили у малыша резкие приступы кашля во время игры или приема пищи по причине попадания стороннего предмета в дыхательные пути, необходимо срочно его устранить и обеспечить ребенку максимальный доступ воздуха.
- Если синдром обструкции возник на фоне осрой респираторно-вирусной инфекции, это может говорить о ее осложненном течении. В таком случае нужно как можно быстрее обратиться за скорой помощью.
- При внезапно возникшем удушье у здорового ребенка необходимо в срочном порядке проводить интубацию. В дальнейшем ребенку необходима ИВЛ, что возможно в условиях реанимации.
- Если ребенок не страдает астмой, а признаки удушья отсутствуют, значит причиной БОС стала инфекция или аллергическая реакция, чем и определяются дальнейшие действия врача.
Лечение бронхообструктивного синдрома у детей прежде всего должно быть нацелено на устранение патологии, которая стала причиной БОС.
Также следует восстановить проходимость и дренажную функцию бронхов, снять воспаление, при необходимости укрепить иммунитет и провести антибактериальную терапию. Лечение окажется более эффективным при комбинировании аптечных препаратов с проведением терапевтических мероприятий.
В терапии БОС применяются лекарства следующих категорий:
- Для улучшения отхождения мокроты применяются муколитики. Можно использовать как таблетированные формы, так и растворы для ингаляций. Часто назначаются такие препараты: «Амброгексал», «Амбробене», «Лазолван». Среди лекарств, созданных на основе растений, зарекомендовали себя «Бронхипрет», «Проспан». Также можно использовать «АЦЦ».
- Чтобы снять спазм, необходим прием бронхолитиков. В детской практике назначаются «Сальбутамол», «Фенотерол». Препараты используются при помощи ингалятора несколько раз в сутки, имеют выборочное действие, поэтому список побочных эффектов минимален. Уже через 5-10 минут после начала ингаляции отмечается выраженный положительный эффект.
Лечение БОС будет проходить более эффективно и быстро, если прием лекарств совместить с проведением иных терапевтических действий для укрепления здоровья малыша.
К терапевтическим процедурам могут относятся:
- Специальная дыхательная гимнастика.
- Использование дыхательных тренажеров.
- Дренаж.
- Вибрационный массаж грудной клетки.
- Санаторно-курортное оздоровление.
- Спелеотерапия.
- Бальнеологические процедуры.
- Лечебная физкультура.

Если ребенок удовлетворительно себя чувствует, не стоит заставлять его соблюдать постельный режим — физическая активность способствует лучшему отхождению слизи из бронхов.
Также обеспечьте малышу достаточное количество питья в день: это могут быть травяные чаи, настои, фруктовые соки и морсы, несладкие компоты.
Прогноз развития БОС зависит от первичной патологии и своевременного ее лечения. Также последствия и тяжесть протекания болезни определяются возрастом ребенка: чем меньше возраст, тем выразительнее проявления недуга и сложнее течение основной болезни.
При бронхитах прогноз положительный, однако при легочной дисплазии существуют риски перерождения БОС в астму (в 20% случаев). На фоне бронхиолита может возникнуть сердечная недостаточность, эмфизема.
Случаи частого непродуктивного, изнуряющего кашля могут приводить к тошноте, рвоте, отхаркиванию крови вследствие повреждения дыхательных путей. Потому важно как можно раньше обратиться за квалифицированной помощью и начать адекватную терапию, чтобы не допустить нежелательных последствий.
Соблюдение клинических рекомендаций по предотвращению развития бронхообструктивного синдрома у детей поможет родителям уберечь малыша от такого неприятного явления.
Основные правила профилактики включают следующие моменты:
- Во время сезонных эпидемий избегайте посещения с малышом непроветриваемых помещений со скоплением людей.
- Поддерживайте необходимую влажность воздуха и температуру в доме, не игнорируйте проветривания.
В 80% случаев БОС возникает от рождения до трех лет. Синдром доставляет немало хлопот как ребенку, так и родителям. Однако если вовремя выявить патологию и приступить к терапевтическим действиям, серьезных последствий для здоровья ребенка удастся избежать.
источник
Бронхообструктивный синдром у детей – комплекс симптомов, который характеризуется нарушением проходимости бронхиального дерева функционального или органического происхождения. Клинически он проявляется пролонгированным и шумным выдохом, приступами удушья, активацией вспомогательной дыхательной мускулатуры, сухим или малопродуктивным кашлем. Основная диагностика бронхообструктивного синдрома у детей включает в себя сбор анамнестических данных, объективный осмотр, рентгенографию, бронхоскопию и спирометрию. Лечение – бронхолитическая фармакотерапия β2-адреномиметиками, устранение ведущего этиологического фактора.
Бронхообструктивный синдром (БОС) – клинический симптомокомплекс, который характеризуется сужением или окклюзией бронхов различных калибров вследствие скопления бронхиального секрета, утолщения стенки, спазма гладкомышечной мускулатуры, уменьшения мобильности легкого или сдавливания окружающими структурами. БОС – распространенное патологическое состояние в педиатрии, особенно среди детей в возрасте до 3 лет. Согласно различным статистическим данным, на фоне острых заболеваний дыхательной системы БОС встречается в 5-45% случаев. При наличии отягощенного анамнеза данный показатель составляет 35-55%. Прогноз при БОС варьирует и напрямую зависит от этиологии. В одних случаях происходит полное исчезновение клинических проявлений на фоне адекватного этиотропного лечения, в других наблюдается хронизация процесса, инвалидность или даже летальный исход.
Основная причина развития бронхообструктивного синдрома у детей – инфекционные заболевания и аллергические реакции. Среди ОРВИ бронхиальную обструкцию чаще всего провоцируют вирусы парагриппа (тип III) и РС-инфекция. Другие вероятные причины: врожденные пороки сердца и бронхолегочной системы, РДС, генетические заболевания, иммунодефицитные состояния, бронхолегочная дисплазия, аспирация инородных тел, ГЭРХ, круглые гельминты, гиперплазия регионарных лимфатических узлов, новообразования бронхов и прилегающих тканей, побочное воздействие медикаментов.
Помимо основных причин бронхообструктивного синдрома у детей выделяют способствующие факторы, которые существенно повышают риск развития заболевания и ухудшают его течение. В педиатрии к таковым относятся генетическая склонность к атопическим реакциям, пассивное курение, повышенная реактивность бронхиального дерева и его анатомо-физиологические особенности в младенческом возрасте, гиперплазия вилочковой железы, дефицит витамина D, вскармливание искусственными смесями, дефицит массы тела, внутриутробные заболевания. Все они способны усиливать влияние друг друга на организм ребенка и усугублять течение бронхообструктивного синдрома у детей.
Патогенетически бронхообструктивный синдром у детей может быть обусловлен воспалительной реакцией бронхиальной стенки, спазмом гладкомышечной мускулатуры, окклюзией или компрессией бронха. Вышеуказанные механизмы способны вызывать сужение бронхиального просвета, нарушение мукоцилиарного клиренса и сгущение секрета, отек слизистой оболочки, деструкцию эпителия в крупных бронхах и его гиперплазию в мелких. Как результат – развивается ухудшение проходимости, дисфункция легких и дыхательная недостаточность.
В зависимости от патогенеза бронхообструктивного синдрома у детей выделяют следующие формы патологии:
- БОС аллергического генеза. Возникает на фоне бронхиальной астмы, реакций гиперчувствительности, поллинозов и аллергических бронхитов, синдрома Леффлера.
- БОС, вызванный инфекционным заболеваниями. Основные причины: острые и хронические вирусные бронхиты, ОРВИ, пневмонии, бронхиолиты, бронхоэктатические изменения.
- БОС, развившейся на фоне наследственных или врожденных заболеваний. Чаще всего это муковисцидоз, недостаточность α-антитрипсина, синдромы Картагенера и Вильямса-Кэмпбелла, ГЭРХ, иммунодефицитные состояния, гемосидероз, миопатия, эмфизема и аномалии развития бронхов.
- БОС, возникший в результате неонатальных патологий. Зачастую он формируется на фоне СДР, аспирационного синдрома, стридора, грыжи диафрагмы, трахеоэзофагеального свища и т.д.
- БОС как проявление других нозологий. Бронхообструктивный синдром у детей также может быть спровоцирован инородными телами в бронхиальном дереве, тимомегалией, гиперплазией региональных лимфатических узлов, доброкачественными или злокачественными новообразованиями бронхов или прилегающих тканей.
По длительности течения бронхообструктивный синдром у детей разделяют на:
- Острый. Клиническая картина наблюдается не более 10 суток.
- Затяжной. Признаки бронхиальной обструкции выявляются на протяжении 10 дней и дольше.
- Рецидивирующий. Острый БОС возникает 3-6 раз в году.
- Непрерывно рецидивирующий. Характеризуется короткими ремиссиями между эпизодами затяжного БОС или полным их отсутствием.
Клиническая картина бронхообструктивного синдрома у детей во многом зависит от основного заболевания или фактора, провоцирующего данную патологию. Общее состояние ребенка в большинстве случаев среднетяжелое, наблюдается общая слабость, капризность, нарушение сна, потеря аппетита, признаки интоксикации и т. д. Непосредственно БОС независимо от этиологии имеет характерные симптомы: шумные громкое дыхание, хрипы, которые выслушиваются на расстоянии, специфический свист при выдохе.
Также наблюдается участие вспомогательной мускулатуры в акте дыхания, приступы апноэ, одышка экспираторного (чаще) или смешанного характера, сухой или малопродуктивный кашель. При затяжном течении бронхообструктивного синдрома у детей может формироваться бочкообразная грудная клетка – расширение и выпячивание межреберных промежутков, горизонтальный ход ребер. В зависимости от фоновой патологии также может присутствовать лихорадка, дефицит массы тела, слизистые или гнойные выделения из носа, частое срыгивание, рвота и др.
Диагностика бронхообструктивного синдрома у детей основывается на сборе анамнестических данных, объективном исследовании, лабораторных и инструментальных методах. При опросе матери педиатром или неонатологом акцентируется внимание на возможных этиологических факторах: хронических заболеваниях, пороках развития, наличии аллергии, эпизодах БОС в прошлом и т. д. Очень информативным при бронхообструктивном синдроме у детей является физикальное обследование ребенка. Перкуторно определяется усиление легочного звука вплоть до тимпанита. Аускультативная картина характеризуется жестким или ослабленным дыханием, сухими, свистящими, в младенчестве – мелкокалиберными влажными хрипами.
Лабораторная диагностика при бронхообструктивном синдроме у детей включает в себя общие анализы и дополнительные тесты. В ОАК, как правило, определяют неспецифические изменения, указывающие на наличие очага воспаления: лейкоцитоз, сдвиг лейкоцитарной формулы влево, повышение СОЭ, при наличии аллергического компонента – эозинофилию. При невозможности установить точную этиологию показаны дополнительные анализы: ИФА с определением IgM и IgG к вероятным инфекционным агентам, серологические пробы, тест с определением уровня хлоридов в поте при подозрении на муковисцидоз и т. д.
Среди инструментальных методов, которые могут применяться при бронхообструктивном синдроме у детей, наиболее часто используют рентгенографию ОГК, бронхоскопию, спирометрию, реже – КТ и МРТ. Рентгенография дает возможность увидеть расширенные корни легких, признаки сопутствующего поражения паренхимы, наличие новообразований или расширенных лимфоузлов. Бронхоскопия позволяет выявить и удалить инородное тело из бронхов, оценить проходимость и состояние слизистых оболочек. Спирометрия проводится при длительном течении бронхообструктивного синдрома у детей с целью оценки функции внешнего дыхания, КТ и МРТ – при низкой информативности рентгенографии и бронхоскопии.
Лечение бронхообструктивного синдрома у детей направлено на исключение факторов, вызывающих обструкцию. Независимо от этиологии во всех случаях показана госпитализация ребенка и неотложная бронхолитическая терапия с использованием β2-адреномиметиков. В дальнейшем могут использоваться антихолинергические препараты, ингаляционные кортикостероиды, системные глюкокортикостероиды. В качестве вспомогательных препаратов применяются муколитические и антигистаминные средства, метилксантины, инфузионная терапия. После определения происхождения бронхообструктивного синдрома у детей назначается этиотропная терапия: антибактериальные, противовирусные, противотуберкулезные средства, химиотерапия. В отдельных случаях может потребоваться оперативное вмешательство. При наличии анамнестических данных, указывающих на возможное попадание инородного тела в дыхательные пути, осуществляется экстренная бронхоскопия.
Прогноз при бронхообструктивном синдроме у детей всегда серьезный. Чем младше ребенок – тем тяжелее его состояние. Также исход БОС во многом зависит от фонового заболевания. При острых обструктивных бронхитах и бронхиолитах, как правило, наблюдается выздоровление, редко сохраняется гиперреактивность бронхиального дерева. БОС при бронхолегочной дисплазии сопровождается частыми ОРВИ, но зачастую стабилизируется к двухлетнему возрасту. У 15-25% таких детей он трансформируется в бронхиальную астму. Непосредственно БА может иметь различное течение: легкая форма переходит в ремиссию уже в младшем школьном возрасте, тяжелая, особенно на фоне неадекватной терапии, характеризуется ухудшением качества жизни, регулярными обострениями с летальным исходом в 1-6% случаев. БОС на фоне облитерирующего бронхиолита часто приводит к эмфиземе и прогрессирующей сердечной недостаточности.
Профилактика бронхообструктивного синдрома у детей подразумевает исключение всех потенциальных этиологических факторов или минимизацию их воздействия на организм ребенка. Сюда относится антенатальная охрана плода, планирование семьи, медико-генетическое консультирование, рациональное применение медикаментов, ранняя диагностика и адекватное лечение острых и хронических заболеваний дыхательной системы и т. п.
источник
Бронхообструктивный синдром (БОС) – комплекс клинических симптомов, проявляющийся в ухудшении проходимости воздуха по бронхам в результате их сужения. При этом увеличивается сопротивление воздухоносной системы, и у больного развивается нарушение вдоха.
БОС возникает у детей и у взрослых под влиянием различных заболеваний органов дыхания и сердца. В острых случаях он всегда требует неотложной медицинской помощи. Бронхообструктивный синдром не является самостоятельным заболеванием Его код по МКБ 10 – «Хроническая обструктивная легочная болезнь неуточненная» не вполне соответствует тому состоянию, который врачи называют бронхообструктивным синдромом. Обычно он сопутствует бронхиальной астме и хронической обструктивной болезни легких. Первый приступ нередко возникает на фоне острого бронхита.
Наибольшее клиническое значение бронхообструктивный синдром имеет у маленьких детей. В этом случае он развивается внезапно, и родители часто не знают, как помочь ребенку. Частота БОС у взрослых напрямую связана с плохим контролем астмы и неправильным лечением ХОБЛ, что часто обусловлено экономическими проблемами и несоблюдением врачебных рекомендаций.
Частота БОС у детей по разным данным колеблется от 5 до 40% на фоне инфекций дыхательных путей, прежде всего бронхита. Если в семье есть случаи аллергии, или сам ребенок страдает таким заболеванием, то при обычной «простуде» частота БОС у него может достигать 30 – 40%. Это же относится и к детям, которые болеют ОРЗ чаще 6 раз в году.
92% случаев БОС у детей и взрослых связана с вирусной инфекцией:
- респираторно-синцитиальный – самый частый (до 70% случаев);
- парагрипп 1-го и 3-го типов – встречается в 15% случаев;
- аденовирус – встречается в 5% случаев, но вызывает самые тяжелые формы бронхообструктивного синдрома и больше чем в половине случаев приводит к развитию хронической обструкции бронхов;
- риновирус, возбудители гриппа, герпеса, паротита, вирус Коксаки, цитомегаловирус встречаются редко.
Другие причины развития бронхообструктивного синдрома:
- бронхиальная астма (об особенностях этой болезни у детей можно прочитать здесь);
- инфекция микоплазмами, хламидиями, патогенными грибками и пневмоцистами;
- пороки сердца и легких;
- муковисцидоз;
- сдавление бронхов, например, увеличенными лимфоузлами при туберкулезном бронхоадените.
Факторы риска бронхообструктивного синдрома:
- угроза прерывания беременности;
- ОРВИ у матери в 1-м триместре;
- гестоз;
- осложненные роды;
- асфиксия (удушье) ребенка во время родов;
- раннее искусственное вскармливание;
- нарушение роста и развития ребенка;
- увеличение вилочковой железы;
- нерациональное использование антибиотиков у детей;
- гастроэзофагеальный рефлюкс – заброс содержимого желудка в пищевод;
- генетически обусловленная бронхиальная гиперреактивность;
- плохие условия жизни ребенка, пассивное курение;
- проживание возле крупных заводов или автомагистралей.
Острый бронхообструктивный синдром у детей встречается значительно чаще, чем у взрослых, из-за особенностей строения их дыхательных путей:
- большое количество в стенке бронхов бокаловидных клеток, активно выделяющих слизистую мокроту;
- высокое содержание в слизи сиаловой кислоты, что повышает ее вязкость;
- относительно узкий просвет бронхов;
- слабо развития гладкая мускулатура бронхов, поддерживающая их в расправленном виде;
- недостаточно развитый местный иммунитет;
- податливость хрящей бронхиальной стенки;
- недостаточная прочность ребер.
Выделяют три фактора патогенеза: механический, иммунологический и нейрорефлекторный.
Это отек стенки бронха и избыточная секреция слизи. Отек возникает под действием биологически активных веществ, например, гистамина. В ответ на поражение в стенку бронха устремляются иммунные клетки, которые вызывают воспалительную инфильтрацию. Бронхи отвечают на раздражение спазмом своих стенок. Эти процессы обратимы.
Есть и необратимые механизмы бронхиальной обструкции, на которые практически невозможно повлиять лекарствами:
- изменение свойств (метаплазия) эпителия бронхов;
- разрастание и увеличение (гипертрофия) железистых клеток;
- спадение (коллапс) мелких бронхов.
Сужение бронхов связано с активацией парасимпатической нервной системы. Это часть вегетативной нервной системы, так же как и симпатическая. Ее роль в организме – регуляция усвоения питательных веществ, угнетение активность обменных процессов. Поэтому под действием парасимпатики бронхи сужаются, сердцебиение замедляется, активируется пищеварение.
Эффекты парасимпатической нервной системы реализуются через рецепторы в стенках бронхов:
- Н2-гистаминорецепторы усиливают секрецию слизи;
- Н1-гистаминорецепторы повышают проницаемость сосудов и приводят к отеку бронхиальной стенки;
- М-холинорецепторы в клетках гладких мышц в стенках бронхов вызывают их сокращение и спазм.
Симпатическая нервная система также участвует в развитии бронхообструктивного синдрома путем активации своих альфа-адренорецепторов, расположенных в гладких мышцах бронхиальных сосудов. При этом возникает сильный сосудистый спазм и нарушение кровоснабжения бронхов.
Для снятия признаков БОС используются лекарственные средства, действующие на перечисленные выше рецепторы.
Один из видов иммуноглобулинов – IgE – отвечает в организме за развитие аллергической реакции. При бронхиальной обструкции происходит бриджинг – прикрепление двух его молекул к особым тучным клеткам, в которых содержится много гистамина. Под влиянием цепной реакции мембрана тучной клетки повреждается. В результате дополнительно к механическим и нейрорефлекторным факторам присоединяется аллергический отек.
Вирусы участвуют в реализации всех трех патогенетических механизмов.
Они разрушают клетки бронхиального эпителия, в результате чего исчезают реснички, выводящие слизь наверх, и формируются пробки из мокроты. В тяжелых случаях в результате этого полностью нарушается вентиляция лежащего ниже легочного участка и возникает его спадение – ателектаз.
Разрушенный эпителий становится легко проницаем для жидкости, которая пропотевает из сосудов и усиливает отек слизистой оболочки.
Вирусы угнетают бронхорасширяющее действие бета-2-адренорецепторов и повышают содержание гистамина в мокроте. Это ведет к тому, что склонность к развитию БОС сохраняется даже через несколько недель после излечения самой ОРВИ. Наконец, эти возбудители угнетают местный иммунитет.
По характеру течения выделяют острый (до 10 дней), затяжной, рецидивирующий, непрерывно рецидивирующий, а также латентный (бессимптомный) бронхообструктивный синдром.
Степени тяжести бронхообструктивного синдрома:
| Степень | Симптомы | Дополнительные исследования |
| Легкая | Свистящие хрипы | Показатели в норме |
| Средняя | Одышка в покое с нарушением вдоха или смешанная, синюшность верхней губы, втяжение межреберных промежутков | ФВД составляет 60 – 80% от нормы. В крови незначительно снижено содержание кислорода (РаО2 более 60 мм рт. ст.), повышено содержание углекислого газа (РаСО2 менее 45 мм рт.ст.) |
| Тяжелая | Шумное тяжелое дыхание, участие вспомогательных мышц, диффузная синюшность | ФВД менее 60% от нормы, изменения газового состава выраженнее, чем при средней тяжести |
| Латентная | Нет | Определяется только положительная проба с сальбутамолом. |
Различают такие варианты бронхообструктивного синдрома:
- аллергический;
- при вдыхании инородных тел;
- аспирационный;
- гемодинамический
Бронхиальная астма у ребенка может появиться еще в возрасте до 1 года. Первый приступ возникает внезапно. Он сопровождается такими симптомами:
- вне приступа малыш активен, хорошо ест, не жалуется на головную боль;
- на расстоянии слышны хрипы или своеобразные звуки, напоминающие работу пилой;
- одышка с затрудненным, удлиненным выдохом, ребенок как бы выдавливает воздух;
- в дыхании участвуют мышцы межреберий, диафрагма, области вокруг ключиц;
- во время приступа больной «не находит себе места», беспокоится;
Экстренная помощь заключается в использовании препаратов для снятия приступа. Для длительного лечения необходимо подобрать базисную терапию у аллерголога.
Обычно дети вдыхают мелкие предметы в возрасте от 1 до 3 лет. В дальнейшем это может привести к осложнениям – пневмонии, бронхиту, ателектазу доли легкого, бронхоэктатической болезни. Чтобы их избежать, нужно срочно удалить инородное тело с помощью бронхоскопии, если домашние меры (кратковременное переворачивание вниз головой, похлопывание по спине) не приносят эффекта.
Основные симптомы при локализации инородного тела в гортани:
- одышка с затрудненным вдохом;
- отсутствие голоса или его осиплость;
- приступообразный кашель при смещении предмета в трахею;
- удушье.
Если инородное тело попадает в бронх, оно вызывает сильный приступ кашля, возможна рвота, после чего ребенок успокаивается. Однако в течение 1 – 2 дней у него развивается пневмония.
Он вызван попаданием чужеродного содержимого при забросе из желудка в пищевод и глотку, при трахеопищеводном свище, пороках развития внутренних органов, диафрагмальной грыже. Родителям нужно обратить внимание на такие симптомы:
- частое срыгивание у грудничка;
- отрыжка, тошнота, боль в груди, рвота после кашля;
- появление кашля или удушья по ночам;
- усиление кашля в положении лежа;
- длительное подкашливание после завершения приступа.
Основа терапии такого состояния – применение диеты и антирефлюксных средств (церукал, щелочная минеральная вода без газа и т. д.).
Различные болезни сердца и сосудов могут сопровождаться одышкой и приступами удушья. Родителям нужно обратить внимание на такие дополнительные признаки:
- выслушивание в легких влажных, не только сухих хрипов;
- слишком частое или медленное сердцебиение, не соответствующее возрастной норме;
- перебои в работе сердца;
- уплощение грудной клетки с одной стороны (признак недоразвития одной из легочных артерий).
При появлении бронхообструктивного синдрома важно определить, имеется ли у ребенка астма или обструктивный бронхит, а также другие, более редкие заболевания.
Для астмы более характерно:
- приступообразное течение;
- свистящее дыхание;
- положительные кожные пробы;
- повышение в крови уровня IgE;
- нормальный показатель ОФВ1 при исследовании ФВД вне приступа и его увеличение в 2 раза и более при пробе с сальбутамолом во время приступа.
- у детей старше 2 лет, если они перенесли как минимум 3 эпизода бронхообструктивного синдрома, купировавшихся бронхолитиками;
- у детей любого возраста, если имеется прямая связь с аллергеном (например, шерсть животного) и нет связи с ОРВИ;
- у детей любого возраста, если они перенесли хотя бы один эпизод свистящего дыхания, у них есть другие симптомы астмы и хотя бы частичный ответ на бронхолитики.
Для острого обструктивного бронхита более характерны:
- начало заболевания с развития эпизода бронхообструктивного синдрома;
- перед этим в течение нескольких дней были признаки ОРВИ;
- одышка с затрудненным выдохом (экспираторная) появляется постепенно, на 3 -4 дни болезни;
- преобладание влажных и жужжащих хрипов;
- ярко выраженные симптомы обструкции (кашель) на фоне общего хорошего состояния ребенка;
- отсутствие аллергии у ребенка и его родственников;
- отсутствие в крови эозинофилов в большом количестве;
- нормальные показатели IgE крови.
Признаки острого бронхиолита:
- ранее не было признаков ОРВИ;
- возраст до 6 месяцев;
- на момент приступа – симптомы ОРВИ;
- тяжелое состояние, частота дыхания во сне более 60 в минуту;
- мелкопузырчатые хрипы в легких;
- на рентгенограмме – признаки острого вздутия легочной ткани;
- полное выздоровление через 2 – 4 недели.
При пневмонии имеются такие признаки:
- постепенное начало после ОРВИ;
- стойкое повышение температуры;
- повышение СОЭ и уровня лейкоцитов в крови;
- рентгенологические признаки пневмонии.
Врожденные заболевания легких (недостаточность альфа1-антитрипсина, муковисцидоз, синдром Вильямса-Кемпбелла, поликистоз легких, бронхоэктазы) характеризуются такими признаками:
- кашель и одышка с первых месяцев;
- ранее появление гнойной мокроты;
- рецидивирующий бронхообструктивный синдром;
- отставание в развитии, деформация грудной клетки.
Другие редкие состояния, при которых возможен бронхообструктивный синдром:
- синдром Картагенера;
- хронический бронхиолит, синдром Мак Леода;
- пороки развития трахеи и бронхов;
- опухоли трахеи и бронхов;
- бронхолегочная дисплазия;
- болезни нервной системы, ДЦП, миопатии, энцефалопатии.
У детей до 5 – 6 лет диагноз ставится на основании клинических симптомов. Более старшие дети могут выполнить исследование функции внешнего дыхания.
При рецидиве бронхообструктивного синдрома назначается комплексное обследование:
- общий анализ крови;
- серологическая диагностика (ИФА) хламидийной, ЦМВ, герпетической, пневмоцистной инфекций, токсокароза, аскаридоза;
- уровень общего и специфических IgE, по показаниям – аллергопробы.
При упорном повторении бронхообструктивного синдрома исследование включает:
Показания для рентгенографии легких при бронхообструктивном синдроме:
- подозрение на осложнение БОС;
- исключение пневмонии;
- подозрение на инородное тело;
- рецидивирующий бронхообструктивный синдром.
В стационаре могут применяться более сложные методы диагностики:
Терапия проводится в зависимости от основного заболевания. Показан щадящий режим, полноценное питание, увеличение количества принимаемой жидкости. Все медикаменты должен назначить врач.
Неотложная помощь при обструктивном бронхите:
- ингаляция с эуфиллином, 2% раствором соды, физраствором;
- ингаляция увлажненного кислорода;
- чередовать каждые 2- 4 часа.
По назначению врача дают такие препараты: эуфиллин, лазолван, бромгексин, тавегил.
При инородном теле в бронхах: держать ребенка в вертикальном положении, вызвать «Скорую помощь».
- обеспечить доступ воздуха;
- успокоить ребенка;
- сделать теплую ножную ванну;
- ввести через ингалятор или небулайзер подобранные ранее бронхолитики (беродуал, астмопент);
- дать супрастин, бромгексин, ацетилцистеин, обильное питье;
- при неэффективности этих мер срочно вызвать «Скорую помощь».
При тяжелом состоянии больного не нужно тратить время на самостоятельные процедуры, лучше сразу вызвать врача, который может ввести необходимые препараты внутривенно.
источник