Реакцией организма на внешние раздражители становится отечность слизистой, покраснения и высыпания на коже. За это отвечает иммуноглобулин Е.
Выработка данных антител в ответ на появление чужеродных клеток (в том числе бактерий, грибков) происходит в подслизистых слоях системы пищеварения, кожного покрова, миндалин, аденоидов, дыхательных путей.
Показатель иммуноглобулина Е при бронхиальной астме имеет важное значение для диагностики. Данное заболевание связано с удушьем, одышкой и кашлем, вызванными воспалением и реакцией бронхов на раздражители.
Иммуноглобулин Е – это особая разновидность белков, производимых лимфоцитами В группы, которая отвечает за реакцию иммунной системы на проникновение в организм паразитов (токсоплазмы, трихинелл, аскарид) и обладает антигельминтным эффектом.
Также IgE участвуют в процессе развития воспаления при попадании в организм аллергенов.
Часто повышаются иммуноглобулины при атопическом дерматите, бронхиальной астме и крапивнице. У многих людей имеется генетическая расположенность к появлению аллергических антител, к которым и относятся иммуноглобулины IgE.
Различают раннюю и отсроченную фазу аллергии. В первой под воздействием активных веществ увеличивается проницаемость сосудистых стенок, развивается отек тканей , активизируется секреция желез, происходит раздражение нервных окончаний, сокращение мускулатуры в органах.
Под действием биологически активных веществ в область воспаления привлекаются кровяные клетки, выделяющие антивоспалительные медиаторы.
Уровень иммуноглобулина Е определяется в следующих ситуациях:
- при инфекциях, воспалениях или аллергических проявлениях;
- при первичных иммунодефицитах;
- при злокачественных опухолях;
- при симптомах бронхолегочного аспергиллеза;
- при назначении иммуно-специфической терапии. Ее можно проводить при показателях IgE 30-700 IU/ml.
При бронхиальной астме программа исследований начинается со сдачи анализов, после проведения которых определяется причина патологии и назначается правильная терапия.
Кроме общего анализа (на гемоглобин, СОЭ, содержание лейкоцитов и эритроцитов), проводятся иммунологическое и биохимическое исследования крови, анализ мокроты. При необходимости специалист назначает дополнительные обследования.
Перед сдачей анализа нельзя принимать пищу 8 часов, рекомендуется за сутки исключить из рациона жареное, жирное, алкогольные напитки.
Иммунологические исследования направлены на выявление повышения уровня IgE, что важно для дифференциации инфекционно-зависимой и аллергической формы астмы.
При этом также определяют в сыворотке крови объем иммуноглобулина и специфических антител.
Общий уровень иммуноглобулина не является основанием для постановки диагноза , потому что этот показатель может быть одинаковым у здорового и больного пациента.
Определение уровня специфического IgE осуществляется посредством кожных проб, а при высокой опасности анафилактических реакций – при помощи радиоаллергенного теста.
После определения в сыворотке крови специфических иммуноглобулинов выявляются возможные аллергены. Как правило, при этом уровень IgE превышает нормативные показатели, а Т-супрессорные лейкоциты снижены.
В нормальном состоянии уровень общего иммуноглобулина Е в кровяной плазме будет низким, так как нет необходимости в выработке защитного белка при отсутствии атопических антигенов.
У детей показатель общего IgE меняется с возрастом и отличается от норм для взрослых людей. К периоду полового созревания эти цифры устанавливаются и потом не меняются. В пожилом возрасте количество защитных антител снижается – это нормальное явление.
Если содержание IgE у взрослого человека — 3-423 МЕ/мл, то его уровень в норме. При бронхиальной астме эти показатели составляют 120–1200 МЕ/мл.
Но высокие показатели иммуноглобулина не являются основой для диагностических заключений, так как причин для его повышения много, например, поллиноз и аллергический ринит.
Необходимо провести углубленные исследования, чтобы точно определить, почему повышен аллерген-специфический IgE.
Атопическая бронхиальная астма, как и другие болезни аллергической природы, развивается при попадании в организм аллергенов (пищевых добавок, пыли, пыльцы, чужеродного белка, лекарств, химикатов и пр.).
При развитии аллергической реакции выделяются специфические иммуноглобулины. Они дают сигнал о начале воспаления.
С увеличением содержания иммуноглобулинов Е в крови повышается количество рецепторов к данным антителам на поверхности клетках, активирующих аллергические реакции.
В результате выбрасываются медиаторы воспаления, что приводит к развитию тяжелой симптоматики. У людей с тяжелой патологией бронхов намного больше рецепторов к иммуноглобулинам, чем при легкой форме или у здоровых.
Если особое внимание при лечении уделить уменьшению воздействия IgE, то можно исключить или снизить интенсивность воспаления, так как будет меньше выделяться веществ, его провоцирующих.
Также можно связать Е-молекулы в крови до их оседания на клеточных рецепторах с помощью антител, выделенных из организма животных.
Однако чужеродные белки сами могут приводить к развитию аллергических проявлений, особенно у астматиков, поэтому не всем и не всегда разрешена такая терапия.
При астме для выявления реакции, которую вызывает иммуноглобулин, применяют клинические тестирования. При этом на поврежденную кожу наносят аллергены или вводят их подкожно. Начинает выделяться иммуноглобулин, вызывающий воспаление в области контакта.
Получить направление на диагностику можно у аллерголога, который назначит правильное лечение. Раньше терапия бронхиальной астмы проводилась путем снятия сужения бронхов с помощью бронхорасширяющих лекарств. Но у астматиков только облегчались проявления приступа, но предотвратить обострения не удавалось.
В настоящее время врачи достигли прогресса в лечении благодаря изучению природы астмы. У пациентов стало возможным предотвращать обострения и приступы.
Бронхиальную астму часто лечат высокими дозами ингаляционных глюкокортикостероидов в сочетании с бета-2-агонистами или назначают гормональные препараты в форме таблеток.
Но даже при такой усиленной терапии не всегда удается контролировать симптомы. Поэтому ученые занимаются поиском лекарств, оказывающих воздействие на причину заболевания.
При астме тяжелой степени рекомендуется анти-IgE-терапия. Пациентам вводится особое вещество — омализумаб, блокирующее активность иммуноглобулина Е. В результате у астматиков снижается количество обострений, уменьшается необходимость в системных гормонах, улучшается качество жизни.
Препарат имеет высокую эффективность, при его приеме редко появляются признаки аллергии и не выявлены опасные последствия. Назначается омализумаб детям старше 6 лет и взрослым при подтвержденной атопической природе болезни после проведения аллергопроб, выявления повышенного содержания в сыворотке крови общего иммуноглобулина.
Препарат вводят под кожу раз в 2-4 недели, дозировка выбирается, исходя из уровня IgE.
Кроме того, в зависимости от причин заболевания, назначаются следующие препараты:
- Антигистаминные лекарства. Блокируют рецепторы, реагирующие на гистамин, участвующий в развитии аллергической реакции.
- Препараты местного действия (для уменьшения внешних проявлений патологии, предотвращения осложнений) – мази и капли с противовоспалительным действием.
- Противогельминтные средства для борьбы с паразитарной инвазией.
- Стимуляторы иммунной системы, уменьшающие аллергические проявления.
Медикаменты назначаются врачом с учетом особенностей течения бронхиальной астмы, степени тяжести и причин обострений.
Из народных средств часто применяют отвар из листьев зверобоя, травы золототысячника, хвоща полевого, кукурузных рылец, соцветий ромашки, корня одуванчика и ягод шиповника.
Также можно использовать смесь порошка из яичной скорлупы с лимонным соком или сделать отвар из корней лопуха и одуванчика.
До меня недавно докатился слух о том, что будто наши ученые разработали очередную «кремлевскую таблетку» и уже используют ее для лечения людей, болеющих бронхиальной астмой. Будто бы она позволяет справиться с самыми тяжелыми случаями бронхиальной астмы и буквально преображает жизнь людей с любой аллергией. В результате долгих поисков и разговоров с информированными людьми выяснилось, что это не очередная утка.
Новое лекарство действительно есть, и оно действительно помогает при бронхиальной астме, причем самой тяжелой. Правдой оказалось и то, что это лекарство эффективно и при некоторых других видах аллергии.
К сожалению, назвать это лекарство «кремлевской таблеткой» не получится по целым трем причинам. Во-первых, разработали его не отечественные специалисты, а швейцарские, во-вторых, оно вышло за рамки «придворных» медицинских учреждений, и, наконец, это не таблетка. Пожалуй, только последний факт несколько меня опечалил (хотя, конечно, жаль, что не нашим ученым принадлежит приоритет его изобретения), потому что вводят лекарство подкожно — в инъекциях. Впрочем, это не самое главное — лишь бы помогало.
Кстати, может, и к лучшему обойтись без вычурных названий типа «кремлевских таблеток» и громких эпитетов, от которых веет шарлатанством. Современное лечение бронхиальной астмы обрело название «анти-IgE терапия» и не содержит в себе ничего необъяснимого или паранормального, а опирается исключительно на достижения иммунологии и молекулярной технологии. Суть его в том, что ошибку иммунитета исправляют тоже с помощью иммунных механизмов. Но сначала вспомним, что такое иммуноглобулины класса Е (IgE) и зачем с ними надо бороться.
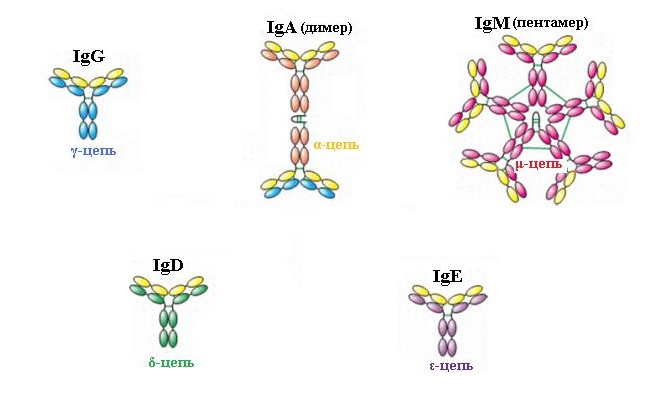
У большинства людей с бронхиальной астмой есть генетическая предрасположенность к выработке аллергических антител, которыми и являются IgE (в отличие от антител классов A, M и G, защищающих организм от различных микробов). Эти антитела вырабатываются лимфоцитами в ответ на определенный аллерген, поступают в кровь и доносятся до тучных клеток, где фиксируются на специальных рецепторах.
Тучные клетки расположены на «пограничных заставах» организма — в коже, конъюнктиве, слизистых оболочках бронхов, носа, желудочно-кишечного тракта, то есть там, откуда могут проникнуть аллергены. Если аллерген, к которому у человека выработались IgE, попадает в организм, эти фиксированные на тучной клетке антитела узнают его и дают клетке сигнал к запуску каскада аллергического воспаления. А в результате человек ощущает симптомы со стороны того органа, где «сидят» IgE, — бронхов (при бронхиальной астме), кожи (при атопическом дерматите или крапивнице), носа (при аллергическом рините) и т.д.
Чтобы не допустить запуска этого аллергического каскада, и были синтезированы специальные антитела для анти-IgE терапии, которые после подкожного введения связывают IgE в крови, не позволяя им «прилепиться» к тучным клеткам.
Кому же проводится анти-IgE терапия? Конечно, решение принимает врач-аллерголог, но и нам надо представлять, есть ли смысл задумываться о таком лечении (ведь средство сильнодействующее, а из пушки по воробьям не стреляют).
Анти-IgE терапия показана людям страдающим тяжелой и среднетяжелой бронхиальной астмой, у которых не удается добиться должного эффекта с помощью высоких доз ингаляционных гормонов и бронхолитиков длительного действия. Обязательно должна быть доказана аллергическая природа заболевания — повышенное содержание IgE в крови, а пациент должен быть старше 12 лет.
Если врач назначил анти-IgE терапию, то один раз в 2 или 4 недели человеку делают подкожную инъекцию (доза и частота введения препарата определяются в зависимости от массы тела пациента и исходного уровня иммуноглобулина Е в крови). Заметим, что бросать то лечение, которое проводилось раньше, нельзя, а можно лишь постепенно уменьшать его объем по рекомендации лечащего врача.
Эффективность анти-IgE терапии была изучена у пациентов с тяжелой и среднетяжелой бронхиальной астмой, у которых не удавалось контролировать заболевание с помощью наиболее действенных препаратов (ингаляционных гормонов и бронхолитиков длительного действия).
Как показали исследования, добавление к лечению анти-IgE уменьшает тяжесть симптомов и частоту обострений и даже позволяет снизить поддерживающую дозу гормонов у пациентов с гормонозависимой формой заболевания. Наряду с облегчением течения бронхиальной астмы анти-IgE терапия помогает справиться и с симптомами сопутствующих аллергических болезней (аллергического ринита, пищевой аллергии). Впрочем, этот «побочный эффект» был вполне предсказуемым — ведь IgE перестают поступать не только в бронхи, но и в другие органы, где возможны аллергические реакции. Побольше бы таких «побочных эффектов».
Вот видите, напрасно говорят: «Не верьте слухам!» Иногда бывает полезно и поверить. Но только — из достоверных источников.
источник
По данным эпидемиологических исследований, бронхиальной астмой (БА) страдает 5-10% детского населения. БА — хроническое воспалительное заболевание респираторного тракта, в котором участвуют многие клетки врожденной и адаптивной иммунной системы совместно с эпителиальными клетками, вызывая основные клинические синдромы, характерные для данного заболевания.
Существует мнение, что БА гетерогенна. Выделяют различные ее фенотипы и эндотипы, которые определяются особенностями взаимодействия генетических и средовых факторов, различаются возрастом начала заболевания, клиническими проявлениями, спектром биомаркеров, прогнозом и ответом на традиционные и новые терапевтические воздействия.
При этом продемонстрировано, что фенотипы астмы, диагностированные с учетом превалирования тех или иных воспалительных клеточных популяций в мокроте, в течение 12-месячного периода наблюдения не были стабильными.
Иммунологические механизмы, лежащие в основе БА, преимущественно опосредованы Т-лимфоцитами-хелперами 2-го типа (Th2), ассоциированы с гиперпродукцией иммуноглобулинов Е и формированием эозинофильного варианта воспаления в респираторном тракте.
Однако некоторые аспекты эозинофильного воспаления могут быть ассоциированы с активацией лимфоидных клеток 2-го типа врожденного иммунитета (innate lymphoid cells 2 — ILC-2), действующих совместно с базофилами. Кроме того, для некоторых фенотипов БА характерно преимущественно нейтрофильное воспаление, контролируемое подмножеством Th17 хелперных Т-клеток.
У большинства детей формирование БА связано с Тh2-вариантом иммунного ответа, атопией, врожденной склонностью к гиперпродукции общего и специфического IgE, снижением функциональной активности T-reg-клеток (Th3, Tr1, CD4-, CD25+) и дисбалансом Th1/ Th2.
Взаимодействие на поверхности тучных клеток и базофилов специфических IgE с причиннозначимыми аллергенами индуцирует высвобождение преформированных и синтезируемых de novo медиаторов, вызывающих развитие острого воспаления бронхов, сопровождающегося миграцией клеток в слизистую оболочку дыхательных путей и формированием клеточного инфильтрата, включающего эозинофилы, базофилы, Тh2-лимфоциты с участием макрофагов, моноцитов, дендритных, тучных и эпителиальных клеток, тромбоцитов, нейтрофилов, фибробластов.
Выделяемые тучными клетками, эозинофилами, базофилами, ТИ2-лимфоцитами провоспалительные цитокины способствуют формированию хронического воспаления. Миграция провоспалительных клеток из сосудистого русла в межклеточное пространство происходит под влиянием хемокинов и адгезивных молекул.
Персистированию аллергического воспаления в дыхательных путях при БА способствуют длительная экспозиция причинно-значимых аллергенов, наличие у больного высокого индекса атопии, высвобождение нервными клетками воспалительных нейрокинов (субстанции Р, нейрокинов А и В), наслоение вирусной, бактериальной или атипичной (хламидийной, микоплазменной) инфекций.
Так как астма характеризуется рецидивирующей вариабельной обструкцией дыхательных путей, уровень контроля данного заболевания можно оценить, опираясь на выраженность его симптомов, значения параметров внешнего дыхания, результаты функциональных тестов, отражающих вариабельность проходимости бронхов и бронхиальную гиперреактивность.
В связи с тем, что центральное место в патогенезе астмы занимает воспаление дыхательных путей, его мониторинг должен стать составной частью планов ведения пациентов. В настоящее время наиболее изученным биомаркером воспаления при БА является уровень оксида азота и его метаболитов в выдыхаемом воздухе.
Активно в этой связи изучаются также клеточный состав индуцированной мокроты, компоненты конденсата выдыхаемого воздуха (pH, лейкотриены, альдегиды и другие параметры). Новым аналитическим методом детекции биомаркеров в конденсате выдыхаемого воздуха является метаболомика.
Биомаркеры могут быть использованы также для диагностики основных фенотипов и эндотипов астмы. Так, например, уровни Feno, сывороточного периостина, эозинофильного нейротоксина и остеопонтина могут быть использованы для диагностики и мониторирования ТИ2-зависимого эозинофильного варианта воспаления при БА.
Персистирование аллергического воспаления в дыхательных путях лежит в основе неконтролируемого течения БА. Достижение у больного полного контроля над течением астмы является главной целью проводимого лечения при данном заболевании. В связи с тем, что воспаление дыхательных путей — это основное патогенетическое звено, определяющее течение БА, возникает необходимость проведения противовоспалительной терапии в качестве базисного лечения.
Для достижения и поддержания контроля над симптомами и течением БА в настоящее время используются следующие группы фармакологических средств:
- ингаляционные глюкокортикостероиды (ГКС),
- антагонисты лейкотриеновых рецепторов,
- кромоны,
- бета-2-агонисты,
- теофиллины длительного действия.
При тяжелой и резистентной к указанным фармакологическим препаратам астме применяются системные ГКС и анти-IgE-терапия. Кроме того, для патогенетической терапии БА в настоящее время разрабатываются и иные лекарственные препараты — антицитокинового и антимедиаторного действия.
Глюкокортикостероиды обладают высоким противовоспалительным и противоаллергическим действием, связанным с их способностью активировать противовоспалительные гены и подавлять многие из провоспалительных генов, которые были инициированы в процессе воспаления.
В результате наблюдаются ингибирование синтеза провоспалительных цитокинов, липидных медиаторов (лейкотриенов, простагландинов), торможение участия эозинофилов в развитии аллергического воспаления и экскреции эозинофильных медиаторов.
При БА назначаются прежде всего ингаляционные ГКС, что позволяет нивелировать возникновение системных побочных эффектов, свойственных этим препаратам. В результате лечения ими на 5-7-й день от начала терапии у большинства пациентов с недостаточным уровнем контроля БА отмечается исчезновение бронхообструктивного синдрома. К 3-й неделе лечения наблюдаются нормализация или значительное улучшение функции внешнего дыхания, снижение неспецифической бронхиальной гиперреактивности.
Терапия стартовой дозой ингаляционных ГКС проводится, как правило, в течение 3 мес и затем, при отсутствии симптомов, их суточная доза постепенно снижается до поддерживающей, предупреждающей обострение астмы. Поддерживающую дозу больные могут получать в течение нескольких лет. Применение ингаляционных ГКС повышает качество жизни больных БА.
Для проведения базисной противовоспалительной терапии при БА у детей в настоящее время используются следующие ингаляционные ГКС: беклометазона дипропионат, будесонид, циклесонид, флутиказона пропионат, мометазона фуроат. Эти препараты обладают высоким сродством к глюкокортикостероидным рецепторам, способны достигать высоких и длительно сохраняющихся терапевтических концентраций в тканях при местном использовании, быстро инактивируются за счет биотрансформации в печени после системной абсорбции. Наличие высокой местной противовоспалительной активности и низкой системной биодоступности является важным фактором эффективности и безопасности ингаляционных ГКС.
Беклометазона дипропионат — ингаляционный ГКС, обладающий значительной противовоспалительной активностью при наличии небольшого системного действия. Более 40 лет используется в терапии БА и продемонстрировал клиническую эффективность и благоприятный профиль безопасности у детей и взрослых с хронической персистирующей астмой.
Беклометазона дипропионат представляет собой пролекарство, которое в легких гидролизуется до беклометазона монопропионата, а он в свою очередь гидролизуется до беклометазона. Суточная доза беклометазона дипропионата составляет 200-1200 мкг и вводится в 3-4 приема.
Беклометазона дипропионат является действующей субстанцией в аэрозоли «Кленил с Джет-системой». Джет-система повышает депозицию аэрозоля в легких и снижает отложение его частиц в ротоглотке, что позволяет уменьшить риск развития орофарингеального кандидоза, кашля, осиплости голоса и системное воздействие препарата.
Одна ингаляционная доза содержит 200 или 250 мкг беклометазона дипропионата. Детям 6-12 лет назначается по 250 мкг 2 раза в сутки, у детей старше 12 лет при легкой БА суточная доза составляет 200-600 мкг за 2 ингаляции, при астме средней тяжести — 600- 1000 мкг за 2-4 ингаляции, при тяжелой астме — 1000-2000 мкг за 2-4 ингаляции.
Кленил УДВ представляет собой препарат на основе беклометазона дипропионата для небулайзерной терапии БА, выпускается в виде суспензии в ампулах, содержащих 800 мкг беклометазона дипропионата. Детям старше 6 лет препарат назначается по половине одноразовой ампулы для небулизации в дозе 400 мкг 1-2 раза в день.
Будесонид, уже 35 лет использующийся для терапии астмы, является единственным негалогенизированным ингаляционным ГКС. Препарат на 90% метаболизируется в печени и выводится из организма в виде неактивных продуктов обмена. В клетках при взаимодействии будесонида с жирными кислотами образуются комплексы, которые представляют собой внутриклеточные депо препарата.
Пульмикорт Турбухалер — это порошок будесонида, доставляемый в бронхи с помощью турбухалера. Одна ингаляционная доза Пульмикорта Турбухалера содержит 200 мкг препарата. Пульмикорт Турбухалер назначают детям старше 7 лет в суточной дозе 400-800 мкг в 2-4 приема.
Для лечения обострений БА у детей широкое применение находит суспензия Пульмикорта на основе будесонида, выпускаемая в небулах (для небулайзерной терапии). Используется также аналог Пульмикорта — Буденит Стери-Неб, дозированная суспензия. Для лечения детей с БА доза Пульмикорта в суспензии подбирается индивидуально, для детей в возрасте 6 мес и старше начальная доза этого препарата составляет 0,25-0,5 мг/сут. При необходимости доза может быть увеличена до 1 мг/сутки.
Бенакорт — отечественный глюкокортикостероидный препарат на основе будесонида. Препарат представляет собой порошок в ингаляторе циклохалер, содержащем 400 доз будесонида. В качестве наполнителя используется бензоат натрия, обладающий противогрибковой активностью. Другой формой Бенакорта является порошок для ингаляций в виде капсул (200 доз). Применяется у детей старше 7 лет в суточной дозе 400-800 мкг в 2-3 приема.
Флутиказона пропионат обладает выраженной противовоспалительной активностью. Терапия этим ингаляционным ГКС в течение 6 мес и более дает возможность добиться контроля над БА и достичь клинической ремиссии болезни.
Фликсотид — дозированный аэрозоль для ингаляций, выпускается во флаконах, 60 (120) ингаляционных доз по 125/250 мкг препарата, а также в виде порошка в ротодисках, в которых одна ингаляционная доза препарата может содержать 50, 100, 250 и 500 мкг флутиказона пропионата. В зависимости от тяжести течения БА Фликсотид назначается детям старше 4 лет в суточной дозе 100-500 мкг в 2 приема.
Циклесонид является экстрамелкодисперсным ингаляционным ГКС. Депозиция циклесонида происходит как в центральных, так и в периферических отделах бронхов. По своему механизму действия препарат является пролекарством, которое активируется в эндотелиальных клетках дыхательных путей с образованием активного метаболита дезциклесонида, имеющего в 100 раз большее сродство к глюкокортикостероидным рецепторам по сравнению с циклесонидом. Лечение циклесонидом способствует улучшению контроля БА, препарат обладает высокой клинической эффективностью.
Альвеско выпускается в виде аэрозольных упаковок с содержанием 40, 80 и 160 мкг в 1 ингаляционной дозе. Применяется при БА у детей с шестилетнего возраста. Доза препарата в зависимости от тяжести БА составляет 80-300 мкг.
Мометазона фуроат — ГКС, обладающий самой высокой аффинностью к глюкокортикостероидным рецепторам по сравнению с другими ГКС для ингаляционного применения при БА, что наряду с продолжительным периодом полужизни коррелирует с высоким уровнем терапевтической эффективности и безопасности.
Преимуществом Асманекса Твистхейлер является возможность применения препарата 1 раз в день, что способствует повышению приверженности больных лечению. Форма выпуска препарата в разных дозах (200 и 400 мкг) соответствует требованиям, предъявляемым к ступенчатой терапии БА, и позволяет повышать или снижать дозу в соответствии с характеристиками достигаемого контроля астмы.
Терапия низкими и средними дозами ингаляционных ГКС сводит к минимуму возможность возникновения системных побочных эффектов. Однако при терапии ингаляционными ГКС следует учитывать рост ребенка и рекомендовать использовать минимальные эффективные дозы препаратов у всех детей с БА.
Ингаляционные ГКС являются наиболее эффективными противовоспалительными препаратами, обеспечивающими достижение и поддержание контроля над симптомами и течением большинства случаев БА. Однако встречаются случаи стероидорезистентности, что требует увеличения доз препаратов и сопряжено с повышением риска формирования нежелательных побочных эффектов.
Понимание молекулярных механизмов действия ГКС позволяет детализировать причины формирования глюкокортикостероидной резистентности. В настоящее время установлено, что врожденная стероидорезистентность, связанная с мутациями в генах, кодирующих глюкокортикостероидные рецепторы, встречается при БА очень редко.
Чаще наблюдается приобретенная стероидорезистентность, которая при астме обусловлена главным образом модификацией глюкокортикостероидных рецепторов: под влиянием Тh2-провоспалительных цитокинов, продуктов нитрозилирующего и оксидативного стресса, микробных и грибковых суперантигенов, а также деградацией их под влиянием протеаз.
Проблему стероидорезистентности в настоящее время пытаются решить двояко. С одной стороны, продолжается интенсивное изучение фенотипов и эндотипов БА с целью определения когорт пациентов, у которых патогенетические особенности заболевания обусловливают исходную резистентность к ГКС (например, Тh17-опосредованные, преимущественно нейтрофильные варианты воспаления при БА). С другой стороны, интенсивно разрабатываются подходы к увеличению противовоспалительной активности ГКС, снижению вероятности нежелательных побочных эффектов данных препаратов. Эта работа осуществляется по трем направлениям.
- Комбинированная терапия — добавление к ингаляционным ГКС второго препарата для того, чтобы преодолеть стероидорезистентность и уменьшить дозы ГКС, необходимые для достижения клинического эффекта. Такими свойствами обладают пролонгированные бета-2-агонисты.
В настоящее время в клинической разработке имеются и новые препараты, такие как селективные ингибиторы р38-МАРК (митогенактивированной протеинкиназы). Ингибитор р38-МАРК оказывает влияние на транскрипцию генов, кодирующих синтез многих провоспалительных цитокинов, включая ФНО-а, ИЛ-4, ИЛ-5, ИЛ-8, RANTES и эотаксин, и тем самым на патогенез астмы.
Некоторые проявления стероидорезистентности могут быть нивелированы малыми дозами теофиллина. В качестве перспективных направлений рассматривается и применение антиоксидантов.
- Создание пропрепаратов (по типу цикпесонида, превращаемого в легких в его активную форму — С21 — деметилпропионил-циклесонид, что сопровождается низкой орально-глоточной абсорбцией), а также препаратов с высоким сродством к глюкокортикостероидным рецепторам, что позволяет вводить препараты 1 раз в день (циклесонид, флутиказона фуроат, мометазона фуроат).
- Разработка диссоциированных ГКС, которые оказывали бы различные по силе эффекты на процессы трансрепрессии и трансактивации генов, что позволило бы модулировать и нежелательные побочные эффекты данных препаратов.
Одним из способов повышения эффективности ингаляционных ГКС и преодоления стероидорезистентности при БА является использование комбинированной терапии. Наибольшее практическое применение в этой связи получили фиксированные комбинации ГКС и бета-2-агонистов длительного действия: флутиказона пропионат и сальметерола ксинафоат (Серетид, Тевакомб), будесонид и формотерола фумарат (Симбикорт), беклометазона дипропионат и формотерола фумарат (Фостер).
Комбинированная терапия сочетаниями препаратов такого рода является более эффективным методом лечения детей с тяжелым и среднетяжелым течением БА по сравнению с изолированным использованием ингаляционных ГКС.
Флутиказона пропионат + сальметерола ксинафоат (оригинальная комбинация — Серетид, GlaxoSmithKline, Великобритания) выпускается в форме порошкового ингалятора — Серетид Мультидиск, каждая доза которого содержит 50 мкг сальметерола ксинафоата и 100, 250 и 500 мкг флутиказона пропионата, и в форме дозированного аэрозольного ингалятора (без фреона), каждая доза которого содержит 25 мкг сальметерола ксинафоата и 50, 125 и 250 мкг флутиказона пропионата.
Применяется в режиме стабильного дозирования с четырех лет жизни. Доза Серетида определяется возрастом ребенка и тяжестью БА. Эффективность лечения проявляется уменьшением симптомов и обострений БА, достижением у ряда больных клинической ремиссии. Отмечается хорошая переносимость препарата.
Будесонид + формотерола фумарат (оригинальная комбинация — Симбикорт Турбухалер, Astra Zeneca, Швеция) — препарат для ингаляционного применения у детей с 6 лет жизни. Больным 6-12 лет препарат рекомендован в режиме 80/4,5 мкг/дозу по 2 ингаляции 2 раза в сутки, детям 12 лет и старше — 160/4,5 мкг/дозу по 1-2 ингаляции 2 раза в сутки.
При терапии Симбикортом Турбухалером возможен гибкий режим дозирования с увеличением дозы в период обострения (до 2 ингаляций 2 раза в сутки) и снижением до поддерживающей дозы (по 1 ингаляции 1 раз в сутки) при стабильном состоянии больных. Наблюдается хорошая переносимость препарата.
Беклометазона дипропионат + формотерола фумарат (оригинальная комбинация — Фостер, Chiesi, Италия) представляет собой фиксированную комбинацию 100 мкг экстрамелкодисперсного беклометазона дипропионата и 6 мкг формотерола фумарата в разовой дозе в дозированном аэрозольном ингаляторе технологии «Модулит». Препарат применяется у детей старше 12 лет по 1-2 ингаляции 2 раза вдень. Лечение способствует уменьшению частоты симптомов БА и количества ее обострений, отмечена хорошая переносимость препарата.
Флутиказона фуроат + вилантерола трифенатат— это комбинация ингаляционного ГКС и бета-агониста ультрадлительного действия (оригинальная комбинация — Breo Ellipta, GlaxoSmithKline, Великобритания) с введением один раз в день. Проведены клинические исследования III фазы у подростков в возрасте от 12 лет и старше и у взрослых пациентов с астмой. Эффективность однократного применения 100/25 мкг препарата вдень сопоставима с результатами применения 250/50 мкг флутиказона пропионата + сальметерол дважды в день у больных с персистирующей астмой, не контролируемой ингаляционными ГКС в средних дозах после 24 нед лечения.
Мометазона фуроат + формотерола фумарат — оригинальная комбинация Зенхейл, ЗМ Health Саге Ltd. (США); Organon (Ирландия). В дозировках 100/5 и 200/5 мкг 2 раза в день рекомендован для лечения БА у подростков и взрослых.
Флутиказона пропионат + формотерола фумарат— оригинальная комбинация Flutiform, SkyePharma (Швейцария). Продемонстрировано, что в дозе 250/10 мкг обеспечивает более высокую эффективность по сравнению с монотерапией флутиказоном пропионатом для контролирования среднетяжелой и тяжелой БА, с профилем безопасности, аналогичным монотерапии флутиказоном пропионатом.
Назначение ингаляционных ГКС и комбинированных препаратов целесообразно прежде всего при персистирующей среднетяжелой или тяжелой БА. Их применение при легкой персистирующей форме астмы эффективно, но не всегда является столь необходимым, поскольку достичь контроля течения можно и нестероидной противовоспалительной терапией (кромоны, антагонисты лейкотриеновых рецепторов).
Предполагают, что в некоторых случаях альтернативой бета-2-агонистам длительного действия при БА могут быть антихолинергические средства длительного действия, в том числе в сочетании с ингаляционными ГКС. Данная идея в настоящее время вызывает большой интерес. В этой связи активно изучаются антихолинергические средства длительного действия.
- Тиотропия бромид, в том числе в сочетании с ингаляционными ГКС, находится в III фазе клинических исследований возможностей применения для лечения детской и подростковой астмы. У взрослых пациентов с астмой введение в терапию данного препарата было связано со значительным снижением частоты развития обострений.
- Умеклидиниума бромид находится в настоящее время на этапе II фазы клинических исследований возможности использования для лечения астмы в качестве как монотерапии, так и варианта, комбинированного с ингаляционными ГКС лечения.
- Аклидиниума бромид — проводимые исследования свидетельствуют о бронходилатирующем и противовоспалительном эффекте.
Антагонисты лейкотриеновых рецепторов имеют широкое применение в лечении БА у детей.
Монтелукаст натрия (Сингуляр, Монтелар, Монте- ласт, Синглон) ингибирует цистеиниловые лейкотриеновые рецепторы, применяется у детей с 2 лет. Доза его в 2-5 лет составляет 4 мг в жевательной таблетке, в 6-14 лет — 5 мг в жевательной таблетке 1 раз в сутки, для детей 15 лет и старше — 1 таблетка, покрытая оболочкой, 10 мг в сутки.
Этот препарат предупреждает возникновение дневных и ночных симптомов БА, снижает частоту ее обострений приаспириновой, вирус-индуцированной астме и астме физического усилия, уменьшает проявления сопутствующего аллергического ринита, персистирующего и интермиттирующего.
Монтелукаст натрия используется в качестве монотерапии для контроля легкой астмы; в комбинации с ингаляционными ГКС может быть эффективным при среднетяжелой и тяжелой астме, позволяя снизить дозу ГКС. Препарат также применяется на этапе отмены или снижения дозы ГКС для сохранения достигнутого контроля БА. Переносимость монтелукаста натрия хорошая, сравнительно редко отмечаются головная боль, тошнота.
Теофиллин используется для лечения заболеваний дыхательных путей уже более 100 лет. Первоначально он применялся как бронхолитическое средство, но относительно высокие дозы, необходимые для купирования бронхиальной обструкции данным препаратом, вызывают нежелательные побочные эффекты, поэтому его использование с данной целью сократилось.
Однако при более низких концентрациях для теофиллина свойственны противовоспалительные эффекты, обусловленные ингибированием PDE4 и активацией гистондезацетилазы-2, в результате чего происходит выключение активированных воспалительных генов. Благодаря этому механизму теофиллин уменьшает стероидорезистентность, что может иметь особое значение у пациентов с тяжелой астмой.
Препараты метилксантинового ряда ингибируют А1-рецепторы к аденозину, вызывая бронходилатирующий эффект, тормозят высвобождение тучными клетками и базофилами медиаторов воспаления, усиливают апоптоз эозинофилов, ингибируя развитие воспаления в дыхательных путях.
В настоящее время в терапии БА используются преимущественно небольшие дозы медленно высвобождаемых теофиллинов (Неотеопек А, Теопэк, Вентакс, Теотард, Этифиллин и др.). У детей с БА пролонгированные теофиллины могут быть назначены с противовоспалительной целью в невысоких дозах как компонент базисной терапии в течение 1-2 мес.
Терапия дюрантными теофиллинами способствует урежению приступов астмы, повышению толерантности к физической нагрузке, снижению у некоторых больных дозы ингаляционных ГКС. Переносимость теофиллинов в данных дозах у большинства детей хорошая. В единичных случаях отмечаются нарушение сна, тахикардия, тошнота, рвота, головные боли из-за ингибирования фосфодиэстеразы, при более высоких концентрациях наблюдаются сердечные аритмии.
У детей с тяжелым течением БА при недостаточной эффективности лечения ингаляционными ГКС и длительного действия бета-2-агонистами дополнительное назначение монтелукаста натрия и дюрантных теофиллинов позволяет повысить эффективность терапии и достичь контроля заболевания.
Рофлумиласт — ингибитор фосфодиэстеразы 4 — одобрен для применения у пациентов с хронической обструктивной болезнью легких. Его потенциальные противовоспалительные эффекты были продемонстрированы в небольшом рандомизированном плацебоконтролируемом клиническом исследовании у пациентов с мягкой аллергической астмой.
Кромоны (кромоглициевая кислота и недокромил натрия) способны при экспозиции с причинно-значимым аллергеном предотвращать развитие бронхоспазма, ранней и поздней фазы аллергической реакции, тормозить повышение реактивности бронхов, эффективны преимущественно у детей с легким течением БА. Данная группа препаратов мало влияет на уже развившееся обострение заболевания.
Кромогликат натрия выпускается как в виде дозированных аэрозолей, так и в виде 2% раствора по 2 мл для ингаляций через небулайзер. Кратность ингаляций препаратов кромоглициевой кислоты составляет 4 раза в день. Для базисной терапии целесообразно длительное, не менее 3 мес применение препарата.
При легкой астме кромогликат натрия используют для профилактики сезонных обострений заболевания и для предупреждения обострений БА при физическом напряжении. Препарат хорошо переносится. Побочные явления редки, проявляются в основном местной реакцией в виде раздражения верхних дыхательных путей, кашля, редко — бронхоспазма.
Недокромил натрия (Тайлед) подавляет высвобождение медиаторов воспаления из тучных клеток, эозинофилов, нейтрофилов, моноцитов, макрофагов и тромбоцитов, тормозит развитие бронхоспазма, поздние аллергические реакции, снижает неспецифическую гиперреактивность бронхов и частоту обострений БА. Препарат выпускается в виде дозированного аэрозоля, применяется у детей старше 2 лет по 2 мг (1 ингаляционная доза) 2-4 раза в сутки.
При тяжелом, рефрактерном к традиционной фармакотерапии течении БА эффективной может быть анти-IgE-терапия, основанная на парентеральном введении анти-IgE-антител в виде препарата омализумаб (Ксолар).
Омализумаб связывает свободноциркулирующие в крови IgE, снижает продукцию высокоаффинных рецепторов на мембране тучных клеток и базофилов, что приводит к уменьшению экскреции медиаторов, выраженности аллергического воспаления и обратному развитию обострения БА.
Перед началом лечения рассчитывается индивидуальная доза омализумаба с учетом уровня общего IgE в периферической крови и массы тела ребенка, препарат вводится подкожно. Омализумаб способствует снижению частоты обострений БА, количества госпитализаций и обращений за неотложной помощью, уменьшению объема базисной терапии с достижением в большинстве случаев полного контроля болезни.
После начала терапии в отдельных случаях может отмечаться головная боль, а в месте его подкожного введения — возникновение отека, эритемы, зуда. Основным показанием к назначению омализумаба является тяжелая БА у детей 6 лет и старше, рефрактерная к проводимой фармакотерапии.
Основываясь на традиционных сведениях о Тh2-зависимом генезе астмы и эозинофильном воспалении дыхательных путей при данном заболевании, мишенями антицитокиновой терапии помимо IgE следует рассматривать также интерлейкины ИЛ-5, ИЛ-13, ИЛ-4, ИЛ-9.
Анти-интерлейкин-5-антитела. ИЛ-5 задействован в активации и созревании эозинофилов. Меполизумаб анти-ИЛ-5-антитела — в ходе III фазы клинического исследования DREAM, включавшем пациентов в возрасте 12-74 лет с рецидивирующим тяжелым течением БА и признаками эозинофильного воспаления, продемонстрировал эффективность терапии, в том числе в виде снижения обострений БА на 52% в год.
В настоящее время в рамках III этапа клинических исследований проводится изучение антител к рецептору ИЛ-5 (Benralizumab), эффекты истощения эозинофилов наблюдаются в течение нескольких месяцев после одной инъекции данного препарата.
Анти-интерлейкин-13-антитела. ИЛ-13 является важным медиатором БА и воспроизводит большинство ее характеристик в экспериментальных моделях, в том числе ремоделирование, гиперпродукцию слизи, синтез IgE, рекрутирование эозинофилов и базофилов.
Для оценки эффективности анти-ИЛ-13-терапии используется новый сывороточный биомаркер астмы периостин, который является компонентом внеклеточного матрикса, полученного из эпителиальных клеток дыхательных путей в ответ на воздействие ИЛ- 13 и ИЛ-4, высвобождение его подавляется ГКС. Содержание сывороточного периостина позволяет дифференцировать пациентов с «выраженным» и с «невыраженным» Тh2-фенотипом БА.
Специфические анти-ИЛ-13-антитела — препараты Lebrikizumab, Tralokinumab, Anrukinzumab Lebrikizumab вводят подкожно один раз в месяц. В рандомизированном многоцентровом исследовании (219 пациентов) препарат был эффективнее у пациентов с исходным более высоким уровнем периостина в сыворотке крови.
Анти-интерлейкин-4-антитела. ИЛ-4 участвует в дифференцировке ТЬ2-клеток, переключении на синтез IgE, рекрутировании эозинофилов и тучных клеток.
Altrakincept — растворимые рекомбинантные человеческие рецепторы к ИЛ-4, предназначенные для ингаляционной терапии. Данный препарат нейтрализует активацию иммунных и иных клеток, вызываемую ИЛ-4. Однократная ингаляция этого препарата у взрослых с умеренной астмой приводит к улучшению функции легких и снижению уровня выдыхаемого оксида азота.
Pitrakinra — антагонист гетеродимерного рецепторного комплекса — ИЛ-4R-ИЛ-13Ра — разработан для преодоления биологической избыточности ИЛ-4 и ИЛ-13, что, возможно, компенсирует неэффективность стратегий, направленных только на учет ИЛ-4. Pitrakinra ингибирует аллергениндуцированные аллергические реакции и обострение заболевания у взрослых с эозинофильной астмой. AMG 317 является моноклональным антителом, направленным на рецепторы к ИЛ-4, оно блокирует связывание ИЛ-4 с его рецептором, а также ингибирует сигнал трансдукции ИЛ-13. У взрослых с умеренной и тяжелой астмой AMG 317 производит значительное клиническое улучшение только в подгруппе с отсутствием контроля заболевания.
Dupilumab — одна из последних разработок анти-ИЛ-4-терапии, воздействует на альфа-субъединицу рецептора ИЛ-4. Его применение у больных с эозинофильной астмой вследствие ингибирования как ИЛ- 4 и ИЛ-13 сопровождается значительным сокращением обострений БА и улучшением функции легких у взрослых с персистирующей астмой, отменой бета-агонистов и уменьшением дозы ингаляционных ГКС.
ОС000459 — оральный антагонист CRTH2 (хемоаттрактант рецептор-гомологичной молекулы Th2-xeлпeров). В рандомизированном двойном слепом исследовании (фаза II клинических исследований) у взрослых с умеренной персистирующей астмой применение орального антагониста CRTH2 сопровождалось улучшением функции легких, купированием ночных симптомов и улучшением качества жизни по сравнению с плацебо.
MEDI-528 — анти-ИЛ-9-антитела. Применение данного препарата продемонстрировало тенденцию к улучшению показателей контроля у взрослых с легкой и умеренной астмой, а также протективный эффект против бронхоспазма.
Возможными мишенями при разработке новых подходов в лечении БА являются молекулы TSLP, ИЛ-25 и ИЛ-33, которые продуцируются эпителиальными клетками дыхательных путей в ответ на воздействие аллергенов или вирусных триггеров, поэтому рассматриваются в качестве возможных мишеней при создании новых подходов влечении астмы.
Терапия, ориентированная на нейтрофильное воспаление. Нейтрофильное воспаление при БА ассоциировано с интерлейкинами ИЛ-17 и ИЛ-23. Secukinumab — анти-ИЛ-17-антитела — в настоящее время проходит II этап клинических исследований.
Следует отметить, что национальные и международные согласительные документы рекомендуют ступенчатый подход для достижения и поддержания контроля БА. Переход на следующую или предыдущую ступень может быть осуществлен через определенное время в зависимости от тяжести БА, на фоне оценки уровня контроля заболевания при регулярном наблюдении врача.
Достижению контроля при атопической БА способствует проведение аллерген-специфической иммунотерапии причинно-значимыми аллергенами и снижение их уровня в окружении больного.
Осуществление мониторинга, выполняемого при БА у детей, включает исследование функций внешнего дыхания и концентрации оксида азота в выдыхаемом воздухе, оценку реактивности бронхов.
Достижению и поддержанию контроля астмы способствует реализация образовательных программ для родителей и больных астмой детей.
В случае возникновения приступов БА проводится ингаляционная терапия бета-2-агонистами короткого действия или комбинированными препаратами (Беродуал), дозированными ингаляторами или через небулайзер. При тяжелых приступах проводится лечение ингаляционными и системными ГКС (per os или парентерально). При астматическом статусе эффективна инфузионная терапия Эуфиллином и ГКС.
Несмотря на наличие широкого спектра препаратов для базисной противовоспалительной терапии и препаратов для неотложной помощи, сохраняется проблема неконтролируемого или плохо контролируемого течения бронхиальной астмы, что обусловливает потребность в разработке дополнительных диагностических и терапевтических подходов.
В этой связи для оптимизации патогенетической терапии бронхиальной астмы в настоящее время проводится работа по совершенствованию противовоспалительных препаратов имеющихся классов и их сочетаний. Кроме того, ведется поиск принципиально новых подходов к терапии астмы, в том числе с учетом фенотипов и эндотипов болезни, включая создание и внедрение в практику лекарственных препаратов антицитокинового и антимедиаторного действия.
Есть надежда, что по мере детализации знаний о молекулярных характеристиках эндотипов астмы и внедрения в практику биомаркеров, позволяющих диагностировать фенотипы и эндотипы болезни, а также мониторировать уровень контроля, будет реализован персонализированный подход в назначении индивидуальной терапии каждому конкретному пациенту.
источник
Бронхиальная астма в наши дни не считается жизнеугрожающей патологией, так как при своевременной диагностике и назначении лечения заболевание хорошо поддается контролю. Причем не всегда требуется массированное применение лекарственных средств, в профилактике развития приступов удушья огромное значение имеет здоровый образ жизни и предотвращение контакта с аллергенами, другими чужеродными веществами, триггерами.
Содержание статьи
В разных странах мира заболеваемость бронхиальной астмой достигает 18% (около 300 млн, практически каждый 20 человек в мире). В разных регионах России количество пациентов с этой патологией варьируется от 10 до 30%, причем в промышленных районах заболеваемость в несколько раз выше.
В последние десятилетия, в связи с нарастающей индустриализацией и возрождением собственной тяжелой промышленности, во многих крупных городах России наблюдается рост заболеваемости, с увеличением количества случаев тяжелого течения. В настоящий момент бронхиальная астма тяжелого течения зарегистрирована у 10% больных, средней тяжести — у 70%, легкого течения — у 20% пациентов с этим диагнозом.
Распространенность заболевания у детей достигает 15%. В детском возрасте нередко протекает тяжело, сочетается с другими патологиями дыхательной системы — аллергическим ринитом, атопическим дерматитом, хронической обструктивной болезнью легких. Высок риск получения инвалидности и десоциализации ребенка.
Бронхиальная астма развивается под воздействием многочисленных и разнообразных по своей природе влияний.
Основой для формирования заболевания являются генетическая (наследственная) предрасположенность в сочетании с агрессивным воздействием факторов окружающей среды, аллергической и неаллергической природы.
В соответствии с современными представлениями о заболевании, выделяют следующие его типы: аллергического, неаллергического характера, смешанного типа. В качестве провоцирующих приступы факторов могут выступать:
- аллергены — практически все группы чужеродных организму веществ могут вызывать развитие астмы, если они попадают в дыхательные пути во время вдоха или через кровь;
- летучие аллергены, в частности пыльца растений, частицы выхлопных газов и промышленных отходов и пр.;
- агенты инфекционного характера — вирусы, бактерии, простейшие, грибки;
- синтетические вещества — лекарственные препараты, например, ацетилсалициловая кислота (аспирин) и другие химические агенты;
- неспецифические стимулы (не аллергены): холодный воздух, табачный дым, физическая нагрузка, резкий запах, эмоциональный стресс.
Пациенты страдают от регулярно повторяющихся приступов удушья с затруднением и удлинением выдоха, которые сопровождаются свистящими сухими хрипами, слышными на расстоянии, непродуктивным кашлем, тяжестью за грудиной, выраженной одышкой. Иногда перед приступом удушья возникают першение в горле, зуд в носоглотке, чихание, слезотечение, зуд кожи. Приступ может возникнуть в любое время суток, но чаще всего развивается ночью или ранним утром.
Главная роль в развитии заболевания принадлежит высокой реактивности бронхов и склонности к спазму в ответ на воздействие различных стимулов и раздражителей, проявляющейся в виде резкого увеличения сопротивления дыхательных путей и обратимом сужении просвета бронхов.
Спазм гладких мышц вместе с образованием слизистых пробок, отеком и воспалением слизистой бронхов приводит к сужению их просвета. Из-за этого воздух, который попадает в легкие на вдохе, задерживается в ткани легкого, вызывает его перерастяжение и удлинение выдоха. Выдох делается с усилием, в помощь к дыхательным мышцам подключаются вспомогательные мышцы, появляется одышка.
У людей, склонных к развитию бронхиальной астмы, может наследоваться дефект в рецепторах бронхов, который проявляется в недостаточной выработке веществ, предотвращающих развитие спазма при попадании сильного раздражителя в дыхательные пути.
В зависимости от частоты возникновения приступов и их влияния на физическую активность, различают три степени тяжести болезни: лёгкая, средней тяжести и тяжелая. Осложнениями являются инфекционные процессы дыхательных путей (пневмонии), ателектазы (спадение легочных альвеол при закупорке бронхов), сердечно-сосудистые осложнения.
При появлении удушья нужно обратиться к врачу незамедлительно. Врач общей практики (терапевт) может поставить предварительный диагноз уже на первом приеме после осмотра пациента. Обычно больного направляют к пульмонологу — именно этот врач занимается полной диагностикой и лечением бронхиальной астмы.
Для постановки точного диагноза проводятся многочисленные обследования:
- в первую очередь оценивается функция внешнего дыхания (проводятся спирометрия и бронхомоторные тесты), исследуется мокрота;
- при подозрении на аллергическое происхождение астмы проводятся кожные пробы с экстрактами аллергенов, определяются уровни общего IgE и специфических IgE в сыворотке крови (их может быть довольно много);
- обязательно проводится рентгенография органов грудной клетки; в качестве дополнительных исследований изучается газовый состав артериальной крови.
Главной задачей лечения является уменьшение до минимума проявлений заболевания, а именно приступов удушья, в дальнейшем — достижение полного контроля состояния пациента. При полноценном, своевременной и адекватном использовании лекарственных и немедикаментозных методов лечения бронхиальная астма не оказывает влияния на уровень физической активности человека, профессиональную деятельность и качество жизни в целом.
Сегодня для коррекции и длительного контроля за течением заболевания используются разные группы лекарственных средств.
Медицинские препараты короткодействующие для купирования астматических приступов (по требованию):
- b2-агонисты короткого (фенотерол, сальбутамол) и пролонгированного (формотерол, сальметерол) действия для ингаляционного применения: распыляются на вдохе при помощи специальных устройств;
- антихолинергические средства (ипратропия бромид, тиотропий) также для ингаляционного использования;
- комбинированные средства на основе этих компонентов.
Препараты длительного действия для проведения базовой терапии:
- ингаляционные кортикостероиды (беклометазон, мометазон, будесонид);
- пероральные (для приема внутрь) антагонисты лейкотриенов;
- кромоны (кромоглициевая кислота, недокромил натрия) для ингаляций; выпускаются в виде растворов для проведения процедуры при помощи стационарных ингаляторов (в отличие от других средств, выпускаемых в готовой для применения форме);
- препараты анти-IgE-терапии (омализумаб).
При легком течении применяются короткодействующие b2-агонисты (по потребности), часто назначаются низкие дозы ингаляционных кортикостероидов или антилейкотриеновые препараты (реже). Кромоны используются в лечении астмы у детей и по особым показаниям — у взрослых.
При среднетяжелом течении используются b2-агонисты длительного действия в сочетании с гормонами (все препараты ингаляционные) в малых и средних дозах.
При тяжелом течении требуется применение высоких доз ингаляционных b2-агонистов и кортикостероидов, назначаются также препараты на их основе для перорального приема, антилейкотриеновые и анти-IgE-препараты.
Применение аллергенспецифической терапии при астме ограничено возрастом больных (старше 5 лет), вариантом течения заболевания (при доказанной ведущей роли аллергенов). АСИТ не может быть рекомендована как единственный метод лечения. Проводится на фоне гормональной терапии, при стабильных формах заболевания.
Доказано положительное влияние физиотерапевтических процедур на течение болезни, независимо от происхождения (аллергическая, неаллергическая, смешанная). Причем проведение показано на любом этапе развития заболевания.
В лечении астмы используются следующие физиотерапевтические методы:
- ингаляционная терапия с использованием лекарственных средств (бронхолитики, муколитики, антисептики, противовоспалительные и другие препараты в форме высокодисперсного аэрозоля). Многие лекарственные препараты выпускаются в виде ингаляторов, для некоторых необходим стационарный ингалятор. Особенно популярны ультразвуковые небулайзеры, позволяющие создать мелкодисперсный аэрозоль;
- применяется ультразвук, фонофорез и электрофорез с лекарственными веществами (кортикостероиды, препараты кальция), ультрафиолетовое облучение и электросон;
- особенного внимания заслуживает магнитотерапия: под воздействием импульсного магнитного поля активизируется обмен веществ; увеличивается скорость биохимических реакций, улучшается кровообращение и насыщенность тканей кислородом; нормализуется работа эндокринных желез, в частности надпочечников (что важно при астме). Во время сеансов магнитотерапии оказывается также противовоспалительный эффект, способствующий снижению повышенной реактивности бронхов и опосредованно — облегчению течения болезни.
Особенно эффективно комплексное лечение астмы, когда комбинируются лекарственные и немедикаментозные методы.
Так как астма обусловлена множественными факторами, полностью избежать ее развития удается редко. Однако при точном выяснении причин, инициирующих приступы удушья, можно ограничить контакт человека с определенными аллергенами или избегать ситуаций и условий, в которых развивается приступ. Мерой медикаментозной профилактики является постоянное применение лекарственных средств, назначенных врачом.
Задать вопрос врачу
Остались вопросы по теме «Возможности комплексного лечения и улучшения состояния при бронхиальной астме»?
Задайте их врачу и получите бесплатную консультацию.
источник
Моноклональные антитела против IgE (Ксолар) – новый препарат для достижения контроля бронхиальной астмы. Отбор пациентов и особенности лечения
- КЛЮЧЕВЫЕ СЛОВА: Ксолар, бронхиальная астма, омализумаб, bronchial asthma, monoclonal IgG1 antibodies, omalizumab, Xolair
Омализумаб (препарат Ксолар) относится к принципиально новому классу препаратов, используемых в лечении пациентов с неконтролируемой бронхиальной астмой (БА) аллергической природы. Препарат представляет собой рекомбинантные гуманизированные моноклональные антитела, относящиеся к группе иммуноглобулинов (Ig) G1, которые избирательно связываются с циркулирующим IgЕ – важнейшим медиатором аллергических реакций у пациентов с атопической (аллергической) формой БА. IgG1-каппа-антитело содержит человеческую структурную основу с определяющим комплементарность участком мышиного исходного антитела, который связывается с IgE. Омализумаб связывается с IgE и предупреждает его связывание с Fc-эпсилон-R1-рецептором, имеющим высокое сродство к IgE, снижая таким образом количество свободного IgE, способного запустить аллергический каскад.
В июне 2003 г. омализумаб был одобрен Управлением по контролю качества пищевых продуктов и лекарственных препаратов США (US Food and Drug Administration, FDA) для лечения пациентов с аллергической астмой (IgE-опосредованной) среднетяжелого и тяжелого течения при невозможности достижения контроля ингаляционными глюкокортикостероидами (ИГКС) и комбинированными препаратами, содержащими ИГКС и ингаляционные длительно действующие бета-2-агонисты (ДДБА). Омализумаб является первым, наиболее изученным и до настоящего времени единственным препаратом этого класса в лечении пациентов с БА. Его применение разрешено у взрослых и детей с 6 лет во многих странах мира, в том числе и в России. В 2011 г. в России был расширен способ дозирования препарата: верхняя граница исходного уровня IgE у пациента была изменена со значения 700 МЕ/мл до 1300–1500 МЕ/мл. Теперь диапазон использования препарата (уровень IgE) варьирует от > 30 МЕ/мл до 1300–1500 МЕ/мл [1].
Внедрение Ксолара (омализумаба) в практику российского здравоохранения позволило назначать препарат в условиях реальной клинической практики. Применение инновационного препарата довольно остро ставит вопрос о показаниях к его назначению, прежде всего, при неконтролируемой БА. В последние два десятилетия в лечении БА наблюдается значительный прогресс, тем не менее достижение контроля заболевания остается актуальной проблемой. Внедрение современной высокоэффективной базисной терапии привело к существенному улучшению качества медицинской помощи. Однако, по данным целого ряда наблюдательных исследований, у подавляющего большинства пациентов симптомы тяжелой БА не контролируются. Так, в исследовании INSPIRE (International Asthma Patient Insight Research – Международное исследование отношения пациентов к бронхиальной астме), включившем 3415 пациентов с БА в 11 странах мира, как минимум треть пациентов с тяжелым течением БА не достигали контроля заболевания при использовании наиболее эффективного стандартного лечения комбинированными препаратами [2]. Несмотря на проводимое лечение, 74% пациентов вынуждены ежедневно использовать препараты скорой помощи (бета-2-агонисты короткого действия). Важно понимать, что неконтролируемое течение БА сопряжено с высоким риском обострения БА и даже летального исхода.
Возможность достижения контроля тяжелой атопической БА очень часто осложняется не только течением самой БА, но и наличием ассоциированных с атопией сопутствующих заболеваний: аллергического ринита, синуситов, дерматита, каждое из которых приносит большие страдания пациентам.
Основными триггерами, не позволяющими достигать контроля заболевания, являются аллергены. Установлена прямая корреляционная связь между уровнем IgE и риском развития БА. В опубликованных данных клинических исследований ENFUMOSA (European Network For Understanding Mechanisms Of Severe Asthma – Европейская сеть по изучению механизмов тяжелой астмы) [3] и TENOR (Epidemiology and Natural History of Asthma: Outcomes and Treatment Regimens – Эпидемиология и течение бронхиальной астмы: исходы и схемы терапии) [4, 5] аллергия к различным аэроаллергенам была выявлена более чем у 50% и 90% пациентов с БА соответственно.
Было показано, что у пациентов, умерших от тяжелого астматического приступа, плотность рецепторов к IgE в подслизистом слое бронхов достоверно выше по сравнению с пациентами, умершими от других причин [6–9].
Омализумаб связывается с IgE и предотвращает его взаимодействие с высокоаффинным Fc-эпсилон-R1-рецептором, при этом происходит снижение количества свободного IgE, который является пусковым фактором для каскада аллергических реакций. Ксолар подавляет как раннюю, так и поздние фазы астматического ответа у пациентов. Общий уровень IgE (связанного и несвязанного) в сыворотке крови повышался после первой дозы препарата вследствие образования комплекса «омализумаб – IgE», характеризующегося более медленной скоростью выведения по сравнению со свободным IgE. На 16-й неделе после введения первой дозы омализумаба средний уровень общего IgE в сыворотке был в 5 раз выше по сравнению с таковым до лечения. После отмены Ксолара обусловленное его действием увеличение общего IgE и уменьшение свободного IgE были обратимыми. После полного выведения препарата из организма не наблюдалось увеличения концентрации IgE в сыворотке крови. При применении в рекомендуемых дозах среднее уменьшение свободного IgE в сыворотке составляло более 96%.
Кроме того, было обнаружено, что у пациентов с атопической астмой при лечении омализумабом снижается уровень циркулирующих эозинофилов и их количество в мокроте, полученной в результате стимуляции бронхов. Было также показано, что терапия Ксоларом снижает количество эозинофилов в мокроте и количество Fc-эпсилон-R1+-клеток в верхних дыхательных путях больных с аллергической астмой [10] и достоверно снижает число эозинофилов в подслизистом слое бронхов [11]. В исследовании O. Noga и соавт. наблюдалось более значительное увеличение апоптоза эозинофилов (относительно исходного показателя) к 12-й неделе терапии в группе, принимавшей омализумаб, по сравнению с группой плацебо [12]. В исследовании E.L. van Rensen и соавт. отмечено значительно более выраженное снижение количества эозинофилов (относительно исходного уровня) к 12-й неделе в группе, принимавшей омализумаб, по сравнению с группой плацебо [13].
Таким образом, Ксолар можно рассматривать как препарат, обладающим антиаллергическим и противовоспалительным действием.
- Исследование INNOVATE продемонстрировало, что у пациентов с неконтролируемой тяжелой персистирующей атопической БА добавление Ксолара к лечению (IV ступень терапии согласно рекомендациям GINA) приводит к следующим результатам:
- сокращению числа клинически значимых обострений БА на 26%;
- сокращению числа тяжелых обострений на 50%;
- значительному (на 44%) снижению числа экстренных обращений за медицинской помощью (число госпитализаций, включая госпитализацию в реанимационные отделения, незапланированных визитов к врачу) по сравнению с плацебо.
В подгруппе пациентов, ответивших на лечение омализумабом, частота клинически значимых обострений БА за 28-недельный период лечения снизилась на 60,5% по сравнению с группой плацебо (0,34 против 0,85, p 1/100 ÷ > 1/10) были боль, отек, эритема и зуд в месте введения препарата, а также головные боли. Они развивались чаще всего в течение первого часа от момента введения и сохранялись до нескольких дней, однако их выраженность значительно снижалась с каждым последующим введением.
источник